血管侵犯是肝細胞癌(HCC)肝內(nèi)轉(zhuǎn)移以及遠處轉(zhuǎn)移的主要途徑,也是一個強有力的負面預后因素。環(huán)狀 RNA(circRNA)在腫瘤發(fā)生和轉(zhuǎn)移中發(fā)揮著重要作用。然而,circRNAs 在 HCC 血管侵襲發(fā)展過程中的調(diào)控功能和內(nèi)在機制尚不清楚。
今年十月份,四川大學華西醫(yī)院在Molecular Cancer上發(fā)表了一篇名為circPSD3 is a promising inhibitor of uPA system to inhibit vascular invasion and metastasis in hepatocellular carcinoma的文章,通過體內(nèi)體外的實驗證明circPSD3是uPA系統(tǒng)一種很有前景的抑制劑。circPSD3是HCC血管侵襲和轉(zhuǎn)移的重要調(diào)節(jié)因子,可作為預后生物標志物和治療靶點。

研 究 結(jié) 果
circPSD3是PVTT形成的潛在調(diào)節(jié)因子
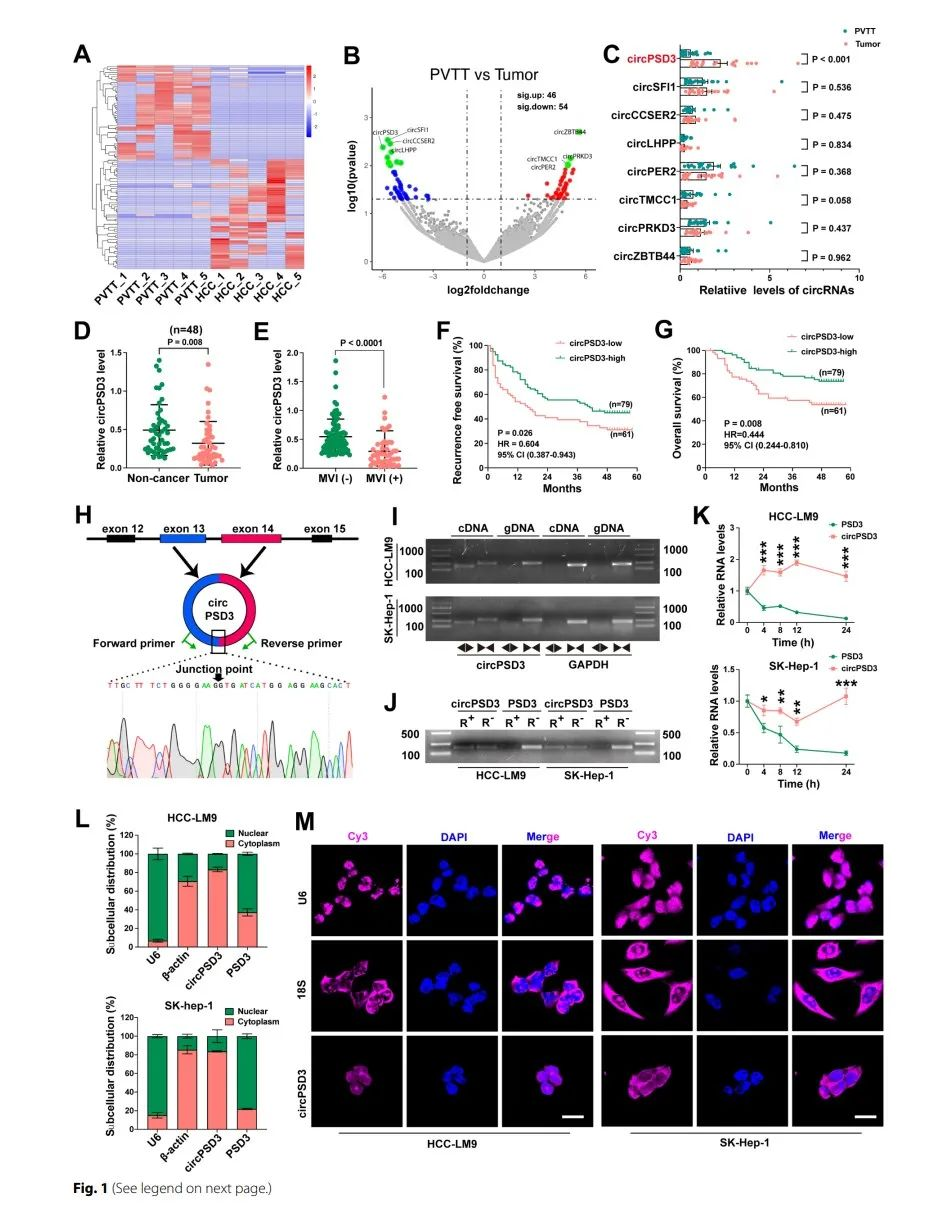
為了篩選出在HCC細胞中參與到血管侵襲的circRNA,針對5個配對的PVTT和HCC組織研究人員做了相關(guān)的circRNA-seq。一共檢測到13238個circRNA,通過一定的篩選標準由100個circRNA被識別出來。在PVTT組織中,有46個上調(diào),有54個顯著的下調(diào)。結(jié)果表明,PVTT組織中存在高度的異質(zhì)性。
為了進一步確認circRNA參與到血管侵襲,研究人員針對19組PVTT和HCC配對的組織中選擇了8個顯著下調(diào)的circRNA,通過qpcr,利用不同的引物擴增了目標circRNA,結(jié)果表明只有circPSD3在HCC組織中顯著下調(diào)。在circRNA-seq中也是circPSD3顯著下調(diào)(fog1C)。之后通過癌和癌旁組織中circPSD3在HCC組織中明顯下降(fig1D)。對于MVI組circPSD3的水平比non-MVI組低(fig1E),并且生存曲線表明,circPSD3和生存相關(guān)(figF、G)。因此,circPSD3被選為調(diào)控血管侵襲和轉(zhuǎn)移的候選circRNA,并且進一步對其做了深入研究。
通過fig1H表明,circPSD3是由PSD3基因的13、14號外顯子剪切形成的。為了確認環(huán)狀circPSD3的性質(zhì),研究人員做了一系列的實驗。首先,通過對HCC細胞的circPSD3進行接頭處的桑格測序。通過對cDNA和gDNA的檢測,證實了circPSD3的存在(figI、J)。最終,通過核質(zhì)分離和FISH實驗表明:circPSD3優(yōu)先表達于細胞質(zhì)中。
TDP43抑制了HCC中circPSD3的生物合成
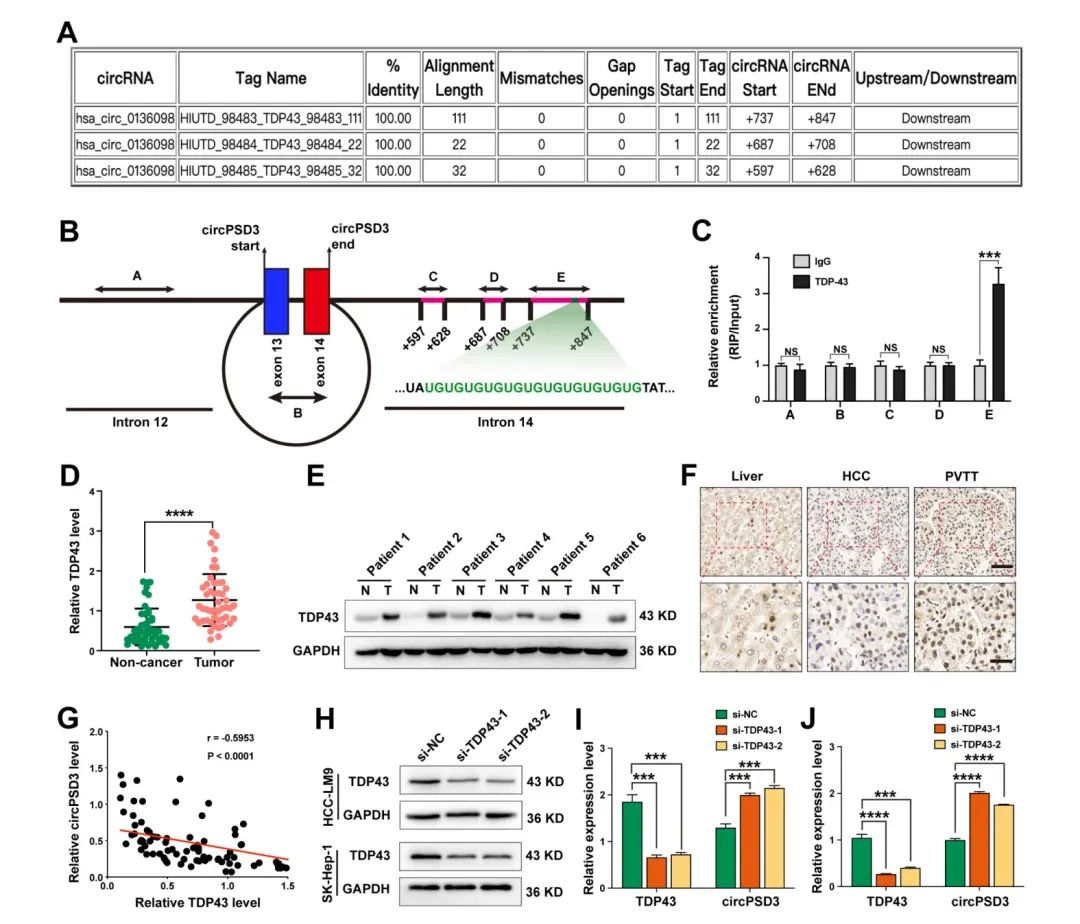
很多RNA結(jié)合蛋白會調(diào)節(jié)circRNA的生物合成,通過circInteractome工具,研究人員找到了circPSD3 pre-mRNA下游內(nèi)含子TDP43三個假定的結(jié)合位點(fig2A)。TDP43介導RNA代謝的多個方面。為了證實TDP43和mRNA的相互作用,設(shè)計了五對引物(fig2B)。之后,通過RIP實驗,使用TDP43的抗體,結(jié)果表明TDP32只富集了引物E的目的序列,表明TDP43通過引物E形成了蛋白-RNA復合物(fig2C)。通過癌和癌旁組織的比較,在HCC組織中circPSD3顯著上調(diào),通過WB也驗證了這個結(jié)果(fig2E、F)。通過Pearson相關(guān)性分析表明在PVTT組織中TDP43和circPSD3呈現(xiàn)負相關(guān)(fig2G)。在HCC細胞中,TDP43的減少會顯著降低circPSD3的表達(fig2H-J)。這些結(jié)果都表明,TDP43會抑制circPSD3的生物合成,circPSD3可能會介導TDP43對于HCC細胞的侵襲和轉(zhuǎn)移的調(diào)節(jié)作用。
circPSD3會抑制體內(nèi)HCC細胞的遷移和侵襲
為了探究circPSD3在HCC形成中的作用,在這里研究人員使用了兩個過表達的慢病毒以及針對circPSD3的接頭處的干擾的慢病毒。通過qpcr實驗表明在HCC細胞中circPSD3被成功的過表達或者敲低(fig3A-D)。在傷口愈合的實驗中,對于circPSD3的過表達會顯著降低HCC細胞的遷移,circPSD3的敲低會顯著增強HCC細胞的遷移(fig3E、F)。在劃痕實驗中,circPSD3的過表達會使得HCC的遷移和侵襲消失(fig3G、H)。3D的侵襲實驗模擬了HCC細胞在體內(nèi)的侵襲。在SK-Hep-1細胞中,circPSD3過表達會耗竭細胞的侵襲面積以及突起數(shù)量。但是CCK8實驗表明,circPSD3對細胞的增殖沒有影響(fig3I、J)。

circPSD3抑制HCC細胞中遠處轉(zhuǎn)移、肝內(nèi)轉(zhuǎn)移和血管侵襲
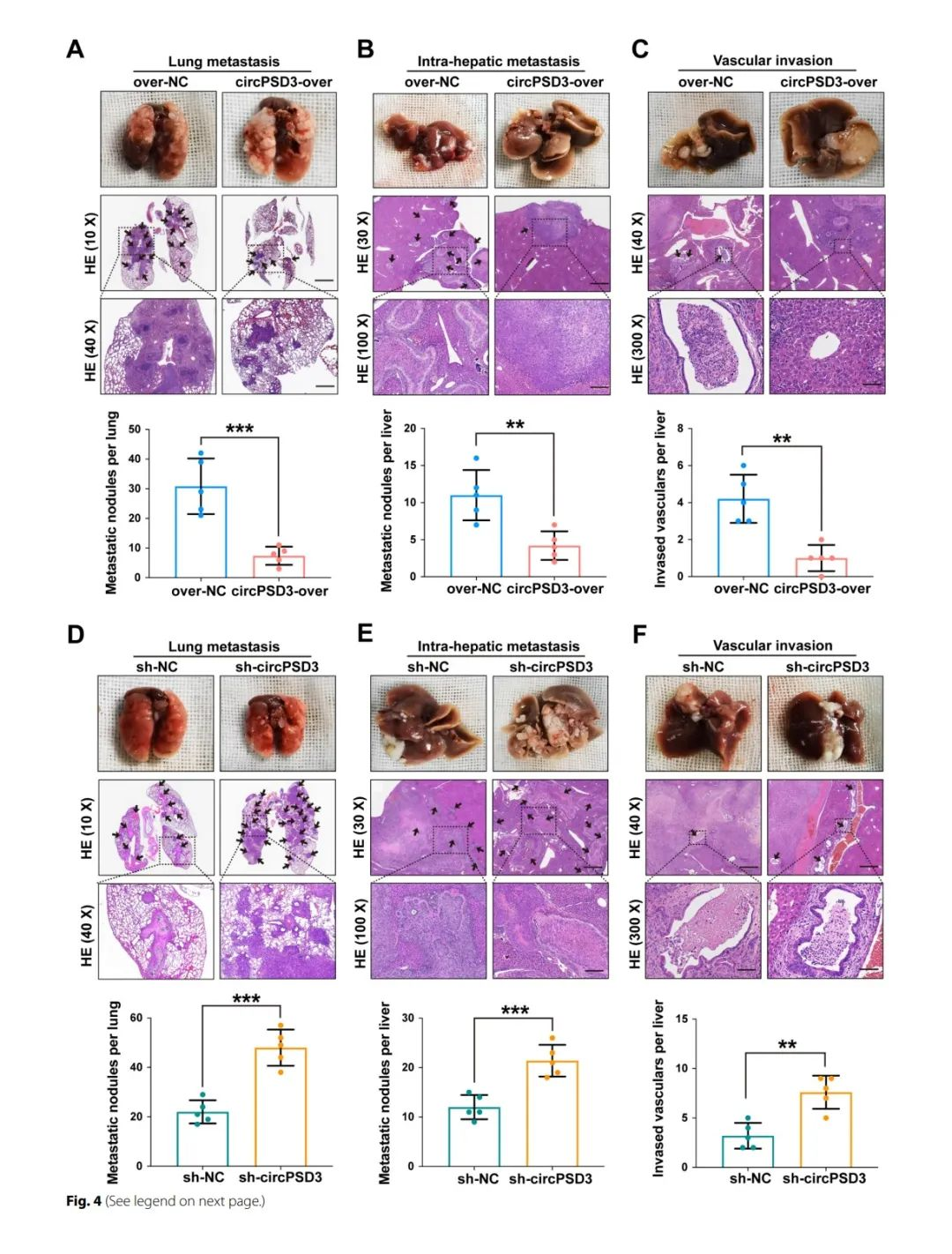
為了進一步加深體內(nèi)的研究,建立了肺轉(zhuǎn)移以及肝臟原位模型。HE染色表明circPSD3的過表達顯著減少了肺部轉(zhuǎn)移灶的數(shù)量(fig4A)。過表達circPSD3可以顯著減少肝內(nèi)轉(zhuǎn)移(fig4b)。為了評估circPSD3對肝內(nèi)血管侵襲的影響,對肝組織進行切片和HE染色,結(jié)果表明過表達circPSD3會顯著降低細胞的血管侵襲能力,相反敲除circPSD3會增加肺轉(zhuǎn)移以及肝內(nèi)轉(zhuǎn)移(fig4C、D)。綜上,這些結(jié)果表明circPSD3在抑制癌細胞和血管侵襲和轉(zhuǎn)移中起著重要的作用。
circPSD3調(diào)節(jié)uPA系統(tǒng)
為了探究circPSD3在HCC細胞中的調(diào)節(jié)機制,研究人員在轉(zhuǎn)染了過表達circPSD3d的HCC細胞上用RNA-seq進行了檢測,通過不同的篩選標準,RNA-seq共鑒定出240個失調(diào)基因,其中42個基因明顯上調(diào),178個基因明顯下調(diào)(fig5A)。富集分析發(fā)現(xiàn)這些基因和很多腫瘤相關(guān)的通路相關(guān),包括PI3K-AKT, MAPK、ECM-受體等通路。通過qPCR驗證了5個上調(diào)以及下調(diào)的基因和RNA-seq結(jié)果一致(fig5B、C)。在這些變化的基因中,SERPINB2是circPSD3過表達引起最大上調(diào)的基因。uPA系統(tǒng)在ECM和基底膜的降解中起著關(guān)鍵作用,SERPINB2 與uPA相互作用,誘導內(nèi)吞uPA-uPAR復合物。為了進一步確定circPSD3在SERPINB2的表達中的調(diào)節(jié)作用,在HCC細胞中SERPINB2穩(wěn)定表達同時circPSD3被敲低。這些結(jié)果表明circPSD3被刪除會降低HCC細胞中SERPINB2的表達(fig5D、E)。circPSD3對于SERPINB2以及uPA系統(tǒng)其他組分的調(diào)節(jié)作用被WB驗證(fig5F)。這些結(jié)果表明SERPINB2和它調(diào)節(jié)的uPA系統(tǒng)是circPSD3的下游。
為了探究Upa系統(tǒng)在HCC進程中的作用,SERPINB2,uPA和uPAR的mRNA通過qpcr檢測,結(jié)果表明SERPINB2顯著下調(diào),uPA和uPAR顯著上調(diào)(fig5G、I)。Pearson相關(guān)性表明在HCC組織中,SERPINB2的表達和circPSD3呈正相關(guān)(fig5J),加強了SERPINB2和circPSD3的相關(guān)性。免疫組化表明在非腫瘤的HCC和PVTT中SERPINB2逐漸減少,但是在uPAR中觀察到一個相反的趨勢(fig5K)顯示了uPA促進HCC中的血管侵襲的潛在作用。體內(nèi)的研究表明SERPINB2的敲除可以顯著促進HCC的遷移和侵襲。WX-671,作為uPA系統(tǒng)的抑制劑,顯著降低被circPSD3敲除所引起的細胞的遷移和侵襲(fig5L、M)。這些結(jié)果都表明,SERPINB2以及它所調(diào)節(jié)的uPA系統(tǒng)會抑制在HCC細胞遷移和侵襲中circPSD3的調(diào)節(jié)作用。
circPSD3直接和HDAC1結(jié)合
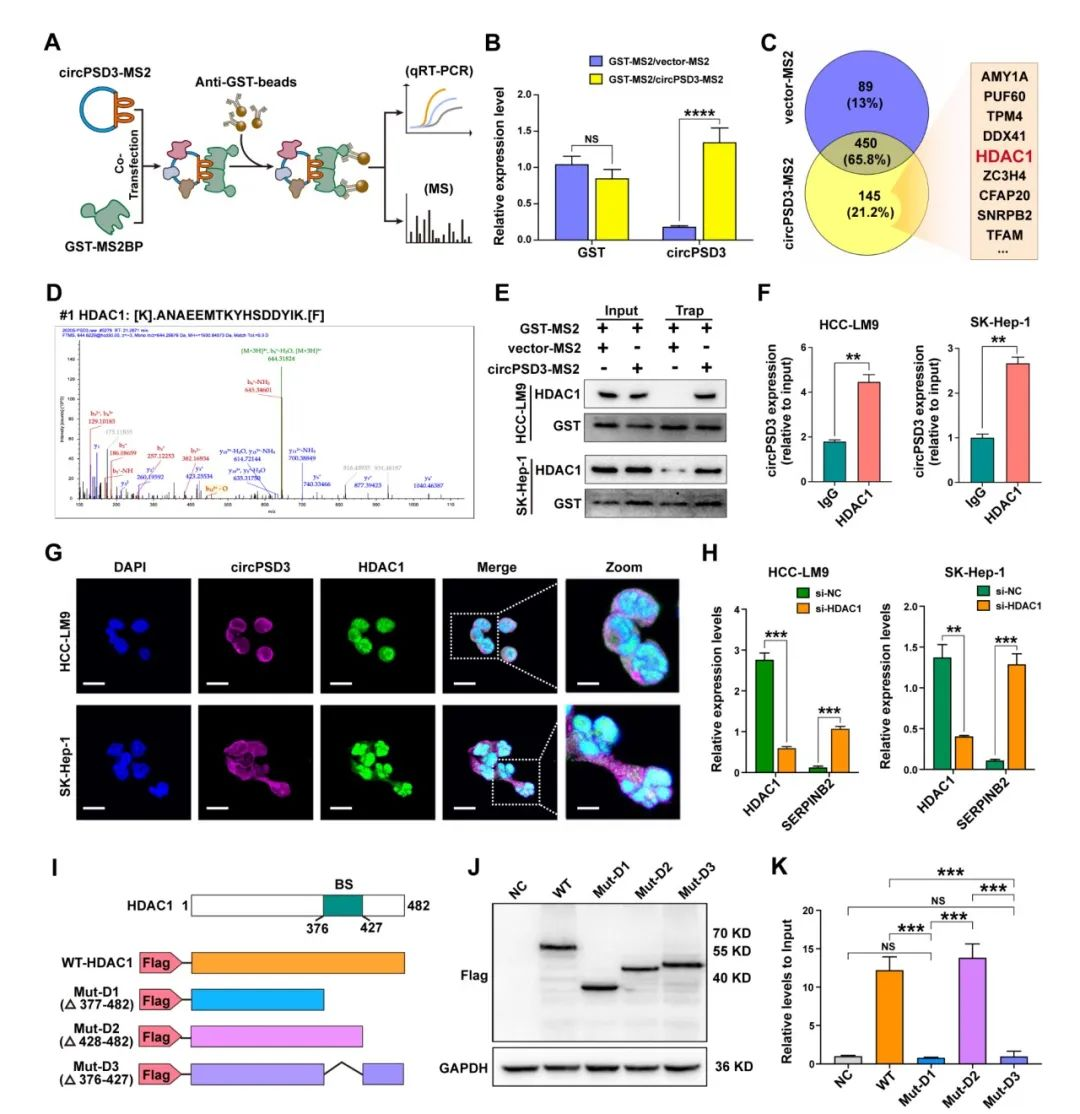
蛋白質(zhì)之間的相互作用在circRNA的功能上也發(fā)揮著重要的作用。在之前的研究中,circRNA相互聯(lián)系的蛋白通過RNA-pulldown通過生物素標記識別,針對circRNA的接頭處。然而,由于在接頭處GC的含量太高,針對circPSD3設(shè)計一個探針比較困難。所以,研究人員使用了一個MS2-標記的TRAP來識別和circPSD3結(jié)合的蛋白質(zhì)。CircPSD3-MS2和GST-MS2載體一起轉(zhuǎn)染進HCC-LM9細胞。circPSD3潛在結(jié)合的蛋白通過GST抗體檢測(fig6A)。接下來通過LC-MS識別了145個蛋白,這些蛋白在circPSD3-MS2中富集,其中16個有超過三個獨特的肽段(fig6C)。
circPSD3對于SERPINB2有調(diào)節(jié)作用,影響它的mRNA和蛋白水平。除此之外,RNA-seq結(jié)果表明circPSD3顯著上調(diào)SERPINB10的mRNA水平,是SERPINB2的下游。因此,研究人員推測circPSD3和一個調(diào)節(jié)SERPINB2的蛋白結(jié)合。在circPSD3-MS2富集的蛋白中,HDAC1是組蛋白去乙酰化酶家族的成員,通過組蛋白去乙酰化參與轉(zhuǎn)錄抑制(fig6D)。TRAP檢測表明circPSD3 和 HDAC1 之間的相互作用(圖 6E)。RIP試驗也表明,HCC 細胞中的 circPSD3 在HCC細胞中被 HDAC1 沉淀(圖 6F)。FISH 和 IF 分析顯示,內(nèi)源性 circPSD3 和 HDAC1 在 HCC 細胞胞質(zhì)中的共定位(圖 6G)研究結(jié)果表明HDAC1敲低顯著上調(diào)了在HCC細胞中SERPINB2的表達(fig6H)。因此,研究人員將HDAC1作為circPSD3結(jié)合的蛋白。隨后,研究人員試圖確定 HDAC1 與 circPSD3 相互作用的區(qū)域。根據(jù) catRAPID,HDAC1 的 376-427 氨基酸序列是最有可能與 circPSD3 發(fā)生相互作用的部位。為了驗證這一假設(shè),研究人員構(gòu)建了野生型和一組截短的 HDAC1 突變質(zhì)粒,每個質(zhì)粒都在 NH2 末端標記了三份 FLAG(3 ×FLAG)(圖 6I)。這些載體在 HEK-293T 細胞中成功表達(圖 6J)。RIP 實驗表明,刪除 HDAC1 的 376-427 氨基酸序列會取消 HDAC1 與 circPSD3 之間的相互作用。
circPSD3抑制uPA系統(tǒng)
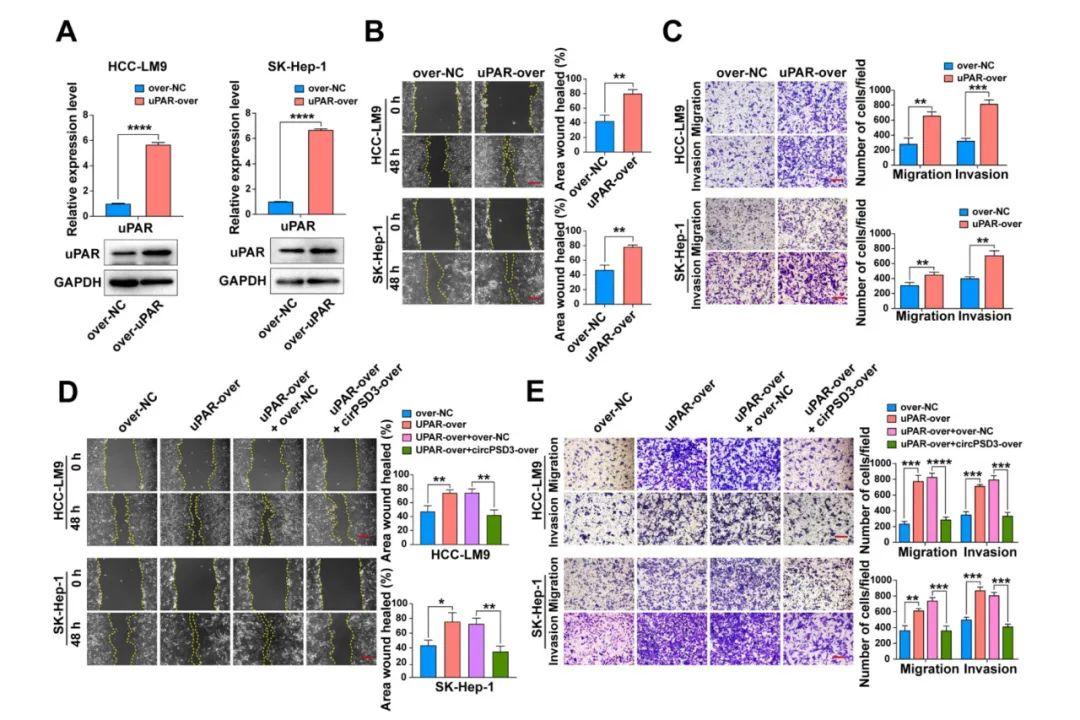
鑒于uPA系統(tǒng)在促進多種惡性腫瘤的侵襲和轉(zhuǎn)移方面發(fā)揮作用,所以被作為是癌癥的潛在治療策略。研究表明,人工過表達circPSD3可能是抑制uPA系統(tǒng)的一種新方法。為了驗證這一假設(shè),上調(diào)uPAR的表達,以模擬活化的uPA系統(tǒng)。傷口愈合和 Transwell 試驗表明,uPAR 過表達會明顯增加 HCC 細胞的遷移和侵襲(圖 7A)。這種效應被circPSD3的過表達所消除(圖 7D、E)。這些結(jié)果在肺轉(zhuǎn)移和肝臟原位植入和肝臟正位植入模型進一步證實。在這些模型中,circPSD3的共表達明顯減輕了肺轉(zhuǎn)移病灶和肝內(nèi)轉(zhuǎn)移結(jié)節(jié)(圖 7F、G)。然而體外合成的 circPSD3 對腫瘤血管侵襲和轉(zhuǎn)移的抑制作用對 HCC 血管侵襲和轉(zhuǎn)移的抑制作用還需要進一步研究。
討論:
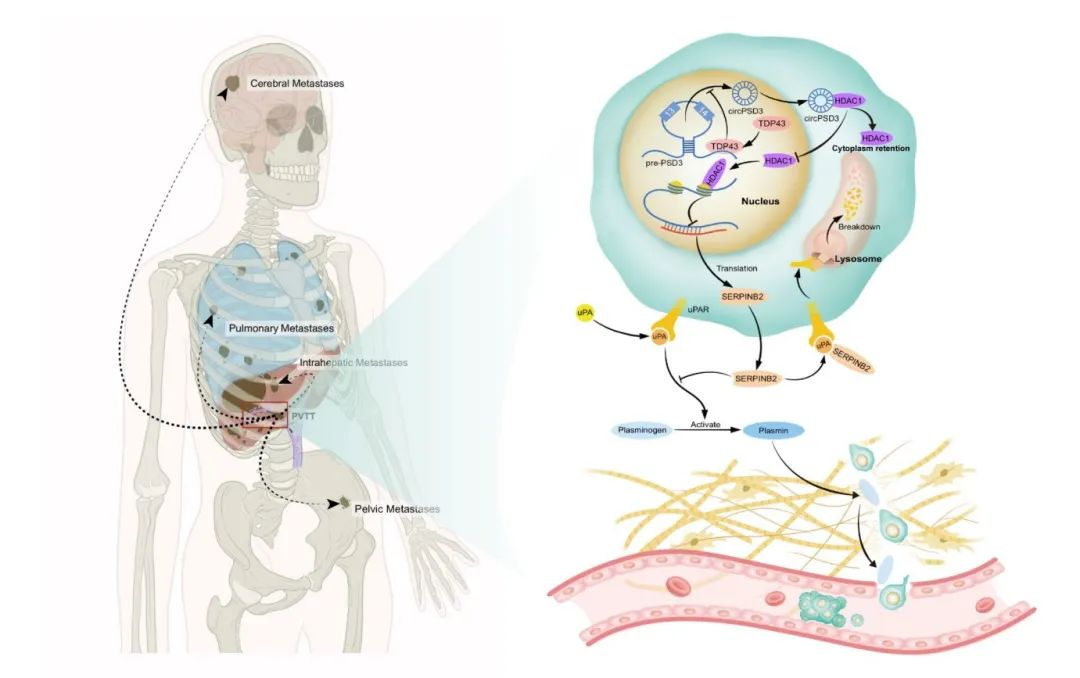
circPSD3 是一種參與侵襲和轉(zhuǎn)移的 circRNA轉(zhuǎn)移。腫瘤組織中 circPSD3 的減少預示著部分肝切除術(shù)后的HCC患者預后不佳。TDP43有助于circPSD3的生物生成。從機制上講,circPSD3與HDAC1 相互作用,將 HDAC1 封閉在細胞質(zhì)中,從而釋放 HDAC1 的轉(zhuǎn)錄抑制作用。HDAC1 對 SERPINB2 的轉(zhuǎn)錄抑制作用。升高的 SERPINB2 會抑制uPA系統(tǒng),并介導的抑制作用(圖 8)。
本研究中,使用了吉凱生產(chǎn)的過表達慢病毒過表達circPSD3和uPAR

參考文獻:
Liangliang Xu1, et al., circPSD3 is a promising inhibitor of uPA system to inhibit vascular invasion and metastasis in hepatocellular carcinoma. Molecular Cancer, 2023.Oct 26;22(1):174.
