?
乳腺癌是女性中最常見的癌癥之一,是導(dǎo)致女性癌癥致死的主要原因。這其中又以后期骨轉(zhuǎn)移導(dǎo)致的骨組織癌癥居多,因此研究乳腺癌相關(guān)的癌細(xì)胞轉(zhuǎn)移機(jī)制就顯得尤為重要。在癌細(xì)胞轉(zhuǎn)移性播散過程中,來自原發(fā)腫瘤的乳腺癌細(xì)胞必須首先進(jìn)行上皮-間充質(zhì)轉(zhuǎn)化侵染周圍組織,進(jìn)入血液循環(huán)系統(tǒng)的微血管,進(jìn)而轉(zhuǎn)移到骨組織內(nèi)。RUNX2 (Runt-related transcription factor 2, RUNX2)是一種與成骨相關(guān)的轉(zhuǎn)錄因子,已經(jīng)成為一個(gè)重點(diǎn)研究的致癌過程中的轉(zhuǎn)錄抑制因子。然而,RUNX2在乳腺癌轉(zhuǎn)移中的作用尚不明確。
?
?
?
2022年5月9日,黃蔚課題組和王艷課題組在Cell Death & Differentiation上發(fā)表題為RUNX2 recruits the NuRD(MTA1)/CRL4B complex to promote breast cancer progression and bone metastasis的研究成果。
?
該研究證實(shí)了RUNX2促進(jìn)并結(jié)合 metastasis-associated 1 (MTA1)/NuRD和Cullin 4B (CUL4B)-Ring E3 ligase (CRL4B)復(fù)合物形成轉(zhuǎn)錄抑制復(fù)合物,催化組蛋白去乙酰化和泛素化。對(duì)RUNX2/NuRD(MTA1)/CRL4B復(fù)合靶點(diǎn)的全基因組分析確定了包括過氧化物酶體在內(nèi)的一組基因增殖因子:激活受體α (PPARα)和超氧化物歧化酶2 (SOD2)在細(xì)胞生長(zhǎng),上皮-間充質(zhì)轉(zhuǎn)化(EMT)和細(xì)胞侵襲中起重要作用。
?
?
該研究證明了RUNX2/NuRD(MTA1)/CRL4B復(fù)合物促進(jìn)體外和體內(nèi)乳腺癌的增殖、侵襲、腫瘤發(fā)生、骨轉(zhuǎn)移、癌干性,表明RUNX2在將來乳腺癌治療發(fā)展中可以作為潛在靶點(diǎn)。
?
?
?

?
該研究首先通過數(shù)據(jù)庫(kù)分析得出RUNX2上調(diào)與乳腺癌發(fā)生相關(guān),并且進(jìn)一步的實(shí)驗(yàn)結(jié)果表明RUNX2調(diào)節(jié)腫瘤抑制基因的表達(dá)和參與骨轉(zhuǎn)移相關(guān)信號(hào)通路。
?
實(shí)驗(yàn)結(jié)果顯示了幾個(gè)最常見的腫瘤抑制因子在RUNX2被敲減后,基因表達(dá)上調(diào),包括BAX, EIF3F, FADD, PPARα,F(xiàn)BXW7, HSP90B1, CASP 7, SIAH2, TNFAIP3,TSC22D1和SOD2。此外,還有幾個(gè)癌相關(guān)基因在RUNX2被敲減后的細(xì)胞中出現(xiàn)下調(diào)。這些結(jié)果顯示RUNX2可能與乳腺癌的發(fā)生有關(guān)。
?
?
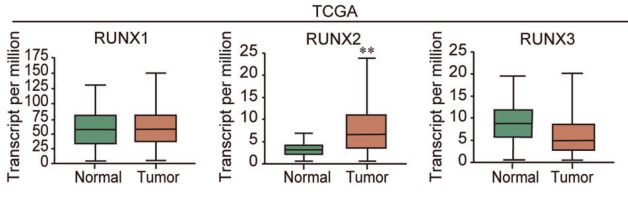
?
圖1. RUNX家族在正常及乳腺癌組織中基于GEO和TCGA數(shù)據(jù)庫(kù)的表達(dá)分析,結(jié)果表明RUNX2在癌細(xì)胞的轉(zhuǎn)錄頻率差異相較于正常細(xì)胞最高。
?
?
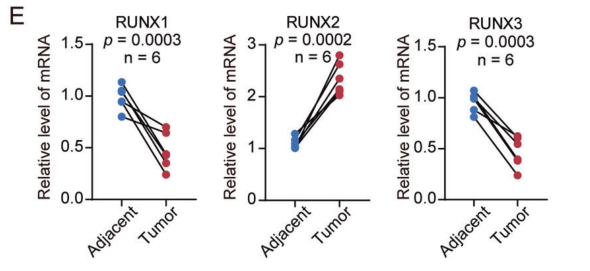
圖2. RUNX2在乳腺癌組織中的表達(dá)量顯著高于癌旁組織中的表達(dá)。
?
?
免疫親和純化和質(zhì)譜分析結(jié)果表明RUNX2與NuRD(MTA1)和CRL4B復(fù)合物相關(guān)聯(lián),進(jìn)一步的純化結(jié)果表明NuRD (MTA1)和CRL4B復(fù)合體與RUNX2可以直接結(jié)合互作。
?
?
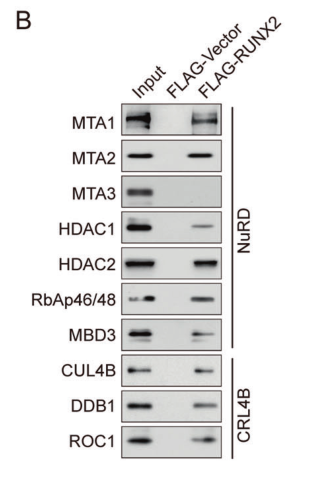
?
圖3. 使用MDA-MB-231細(xì)胞FLAG抗體對(duì)純化的部分進(jìn)行Western blotting分析,結(jié)果表明NuRD(MTA1)和CRL4B的組分含量較高。
?
?
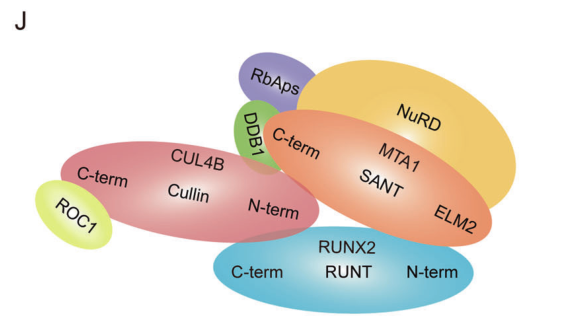
?
圖4. RUNX2/NuRD(MTA1)/CRL4B復(fù)合體分子相互作用示意圖
?
?
細(xì)胞實(shí)驗(yàn)結(jié)果表明 RUNX2、MTA1或CUL4B的敲減導(dǎo)致上皮間質(zhì)轉(zhuǎn)化相關(guān)標(biāo)記因子 fibronectin、N-cadherin和vimentin的表達(dá)減少,并誘導(dǎo)間充質(zhì)標(biāo)記因子E-cadherin、α-catenin和γ-catenin的表達(dá),而RUNX2、MTA1或CUL4B的過表達(dá)得到的結(jié)果剛好相反。
?
?
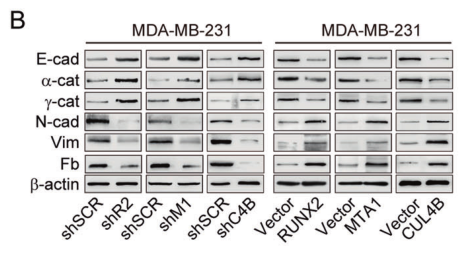
圖5. MDA-MB-231細(xì)胞中RUNX2、MTA1或CUL4B敲減或過表達(dá)后相應(yīng)上皮和間充質(zhì)標(biāo)記因子的表達(dá)量變化。
?
?
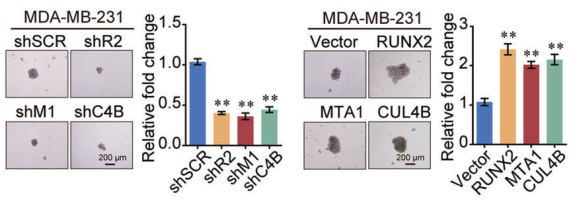
另外干細(xì)胞標(biāo)志物在RUNX2、MTA1或CUL4B敲減后下調(diào),在RUNX2、MTA1或CUL4B正常表達(dá)時(shí)上調(diào),以及 細(xì)胞成球?qū)嶒?yàn)和腫瘤生長(zhǎng)實(shí)驗(yàn)的結(jié)果都說明RUNX2/NuRD(MTA1)/CRL4B可以促進(jìn)癌細(xì)胞增殖。
?
?
?
?
圖6. 細(xì)胞成球?qū)嶒?yàn)結(jié)果表明RUNX2、NuRD(MTA1)和CRL4B都可以促進(jìn)癌細(xì)胞增殖。
?
?
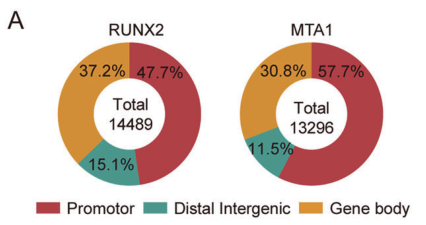
RNA-seq 和KEGG分析結(jié)果表明,RUNX2和MTA1共同參與PI3K-AKT, HIF-1和 IL-17信號(hào)通路。qChIP分析顯示RUNX2/NuRD(MTA1)/CRL4B復(fù)合物大量富集腫瘤抑制基因啟動(dòng)子(SOD2、CASP7、PPARα、BAX、SIAH2、ANXAN7、FBAW7、EIF3F、EI24、TSC22D1、EGR1和NEURL1)。
?
?
?
圖7. 使用CUT&Tag技術(shù)分析確定RUNX2和MTA1的基因組分布。
?
?
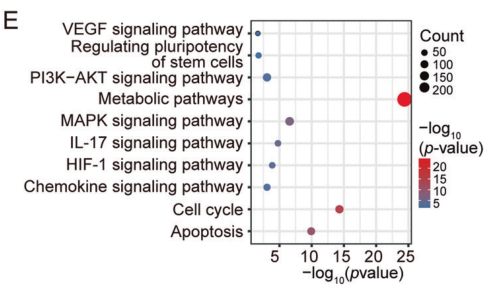
圖 8. 3857個(gè)與RUNX2/MTA1/CUL4B復(fù)合物結(jié)合的啟動(dòng)子(重疊區(qū)域)基因的KEGG通路分析
?
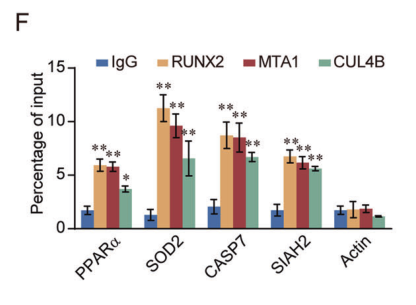
圖9. qChIP結(jié)果表明SOD2、CASP7、PPARα 、SIAH2的基因啟動(dòng)子和RUNX2、NuRD(MTA1)和CRL4B的富集度均較高。
?
進(jìn)一步的qChIP實(shí)驗(yàn)表明,RUNX2、MTA1或CUL4B的敲減導(dǎo)致目標(biāo)基因啟動(dòng)子上相應(yīng)蛋白的募集顯著減少。另外,在WB實(shí)驗(yàn)中也得到了類似結(jié)果。綜上所述,這些結(jié)果證實(shí)了RUNX2、NuRD(MTA1)和CRL4B通過功能性結(jié)合來對(duì)多組抑癌靶基因(如PPARα、SOD2、CASP7和SIAH2)的轉(zhuǎn)錄進(jìn)行抑制。
?
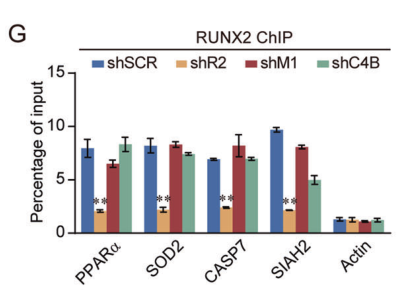
圖10. qChIP結(jié)果表明SOD2、CASP7、PPARα 、SIAH2的基因啟動(dòng)子豐度在RUNX2敲減后均有顯著降低。
?
?
該部分實(shí)驗(yàn)中應(yīng)用了近岸蛋白的NovoNGS? CUT&Tag 3.0 High-Sensitivity Kit (for Illumina?)(Cat.No.:N259-YH01),首先使用CUT&Tag試劑盒對(duì)細(xì)胞樣本依次進(jìn)行ConA磁珠結(jié)合、一抗和二抗結(jié)合、 pAG-Tn5結(jié)合、 加入Tagmentation buffer片段化DNA,DN**段純化后用于文庫(kù)構(gòu)建和高通量測(cè)序。接著,通過qChIP實(shí)驗(yàn)分析了RUNX2、MTA1或CUL4的結(jié)合位點(diǎn),并成功確定了腫瘤抑制基因的富集啟動(dòng)子。后續(xù)用qChIP實(shí)驗(yàn)驗(yàn)證了RUNX2、MTA1或CUL4敲減對(duì)啟動(dòng)子富集的影響。
?
?
該研究發(fā)現(xiàn)RUNX2的敲減促進(jìn)了上皮標(biāo)記因子的表達(dá),降低了EMT標(biāo)記因子的表達(dá),而共同敲除PPARα或 SOD2可以部分恢復(fù)該表型,這表明RUNX2可以通過抑制PPARα或 SOD2的表達(dá)促進(jìn)乳腺癌細(xì)胞的侵襲,同時(shí),骨轉(zhuǎn)移相關(guān)標(biāo)記因子表達(dá)的降低可以通過PPARα的共同敲減而得到恢復(fù)。這些結(jié)果表明RUNX2通過抑制PPARα和SOD2的表達(dá)促進(jìn)乳腺癌細(xì)胞EMT和骨轉(zhuǎn)移。
?
?
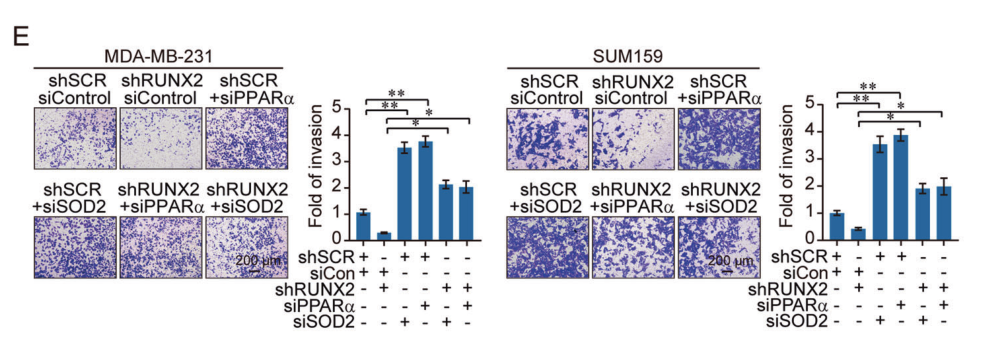
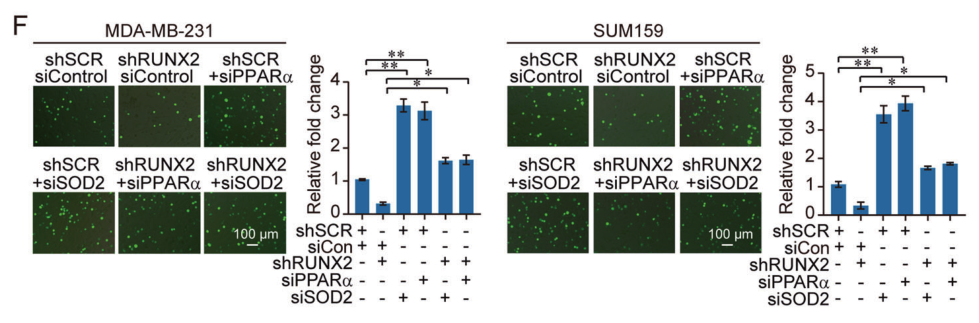
?
圖11和12. MDA-MB-231和SUM159細(xì)胞的趨化遷移試驗(yàn)和癌細(xì)胞-骨基質(zhì)粘附試驗(yàn)都表明RUNX2通過抑制PPARα和SOD2的表達(dá)促進(jìn)乳腺癌EMT和骨轉(zhuǎn)移。
?
?
綜上所述,RUNX2在包括乳腺癌在內(nèi)的多種癌癥中表達(dá)上調(diào),而PPARα作為RUNX2的下游調(diào)節(jié)因子在乳腺癌中表達(dá)下調(diào),提示RUNX2可能作為乳腺癌的生物標(biāo)記因子。RUNX2可以與NuRD(MTA1)/CRL4B復(fù)合體合作,并且誘發(fā)癌細(xì)胞增殖、侵襲、骨轉(zhuǎn)移和癌干細(xì)胞特性。此外,RUNX2/NuRD(MTA1)/CRL4B復(fù)合體有助于腫瘤抑制因子的表觀遺傳沉默。PPARα和SOD2被證實(shí)是RUNX2/NuRD(MTA1)/CRL4B復(fù)合體的靶基因。本研究為RUNX2在腫瘤發(fā)生和轉(zhuǎn)移中的作用提供了新的轉(zhuǎn)錄調(diào)控模型和新的分子基礎(chǔ),表明RUNX2是一種潛在的治療手段癌癥治療的目標(biāo)。
?
在該項(xiàng)研究中使用的試劑盒NovoNGS? CUT&Tag 3.0 High-Sensitivity Kit (for Illumina?)(Cat.No.:N259-YH01)來自近岸蛋白。產(chǎn)品引用文獻(xiàn)已有10余篇,為研究蛋白與DNA互作提供了幫助,為整個(gè)研究奠定了基礎(chǔ)。
蘇州近岸蛋白質(zhì)科技股份有限公司,是一家專注于重組蛋白應(yīng)用解決方案的高新技術(shù)企業(yè),主營(yíng)業(yè)務(wù)為靶點(diǎn)及細(xì)胞因子類蛋白、重組抗體、酶及試劑的研發(fā)、生產(chǎn)和銷售,并提供相關(guān)技術(shù)服務(wù)。公司定位為醫(yī)療健康與生命科學(xué)領(lǐng)域原料與技術(shù)解決方案的上游供應(yīng)商,致力于為下游客戶提供及時(shí)、穩(wěn)定、優(yōu)質(zhì)的產(chǎn)品及服務(wù),助力全球生物醫(yī)藥企業(yè)和研究機(jī)構(gòu)的技術(shù)與產(chǎn)品創(chuàng)新升級(jí)。
詳詢www.novoprotein.com.cn或致電400-600-0940。
