類器官是干細(xì)胞衍生的體外3D自組織培養(yǎng)物,與來(lái)源組織擁有分子機(jī)制與結(jié)構(gòu)功能的相似性,因此已經(jīng)在發(fā)育生物學(xué)、藥物發(fā)現(xiàn)和再生醫(yī)學(xué)領(lǐng)域展現(xiàn)出巨大潛力。然而,當(dāng)前類器官(尤其是神經(jīng)類器官)血管化技術(shù)仍不成熟,球體直徑生長(zhǎng)到約150μm時(shí),由于缺乏血管網(wǎng)絡(luò)的支持,氧氣、營(yíng)養(yǎng)物質(zhì)、代謝物、信號(hào)分子擴(kuò)散不足,類器官中會(huì)出現(xiàn)缺氧和代謝物堆積,從而導(dǎo)致細(xì)胞增殖停滯和核心區(qū)域的壞死。在培養(yǎng)第60天的球狀中腦類器官中便有超過(guò)50%的類器官細(xì)胞缺氧或壞死,腦類器官的功能和表型尤其受限,與人腦體內(nèi)的生理機(jī)能仍有較大差距,無(wú)法精準(zhǔn)進(jìn)行疾病和藥效表征。
目前,血管化技術(shù)正在不斷突破。可行的路線包括加入促進(jìn)血管生成的細(xì)胞因子(如VEGF)、與血管內(nèi)皮細(xì)胞共培養(yǎng)、氣液界面切片培養(yǎng)以及工程化技術(shù)等。不過(guò),這些過(guò)往的技術(shù)方法仍欠缺簡(jiǎn)便性與高效性。
2025年3月17日,美國(guó)印第安納大學(xué)及其合作團(tuán)隊(duì)在期刊Cell Stem Cell發(fā)表論文“Vascular network-inspired diffusible scaffolds for engineering functional midbrain organoids”,創(chuàng)新性地開(kāi)發(fā)了一種受血管網(wǎng)絡(luò)啟發(fā)的可擴(kuò)散支架(VID支架)。該支架具有生物相容性,成本低廉、堅(jiān)固耐用,可批量制造,并可模擬生理擴(kuò)散,從而生成幾乎不出現(xiàn)壞死和缺氧現(xiàn)象的工程化的神經(jīng)類器官(ENOs),顯著增強(qiáng)了類器官的生理功能和藥物篩選的準(zhǔn)確性。

01 VID支架的設(shè)計(jì)
研究團(tuán)隊(duì)使用生物相容性塑料,通過(guò)3D打印在孔板上高通量生成了網(wǎng)狀管腔網(wǎng)絡(luò)。接下來(lái),研究人員模擬原代人腦組織中的信息和物質(zhì)擴(kuò)散,在獲得的VID支架上培養(yǎng)類胚體(embryonic body,使用已充分表征的中腦類器官方案,培養(yǎng)過(guò)程中添加了FGF-8b、BDNF、GDNF等細(xì)胞因子)以獲得ENOs。
與最初的設(shè)計(jì)一致,類器官內(nèi)所有細(xì)胞到最近的可擴(kuò)散表面的距離均不超過(guò)150μm,可保證充足的營(yíng)養(yǎng)和氧氣供應(yīng),細(xì)胞基本處于健康狀態(tài),無(wú)缺氧壞死現(xiàn)象,與常規(guī)神經(jīng)類器官(CNOs)存在顯著差異。
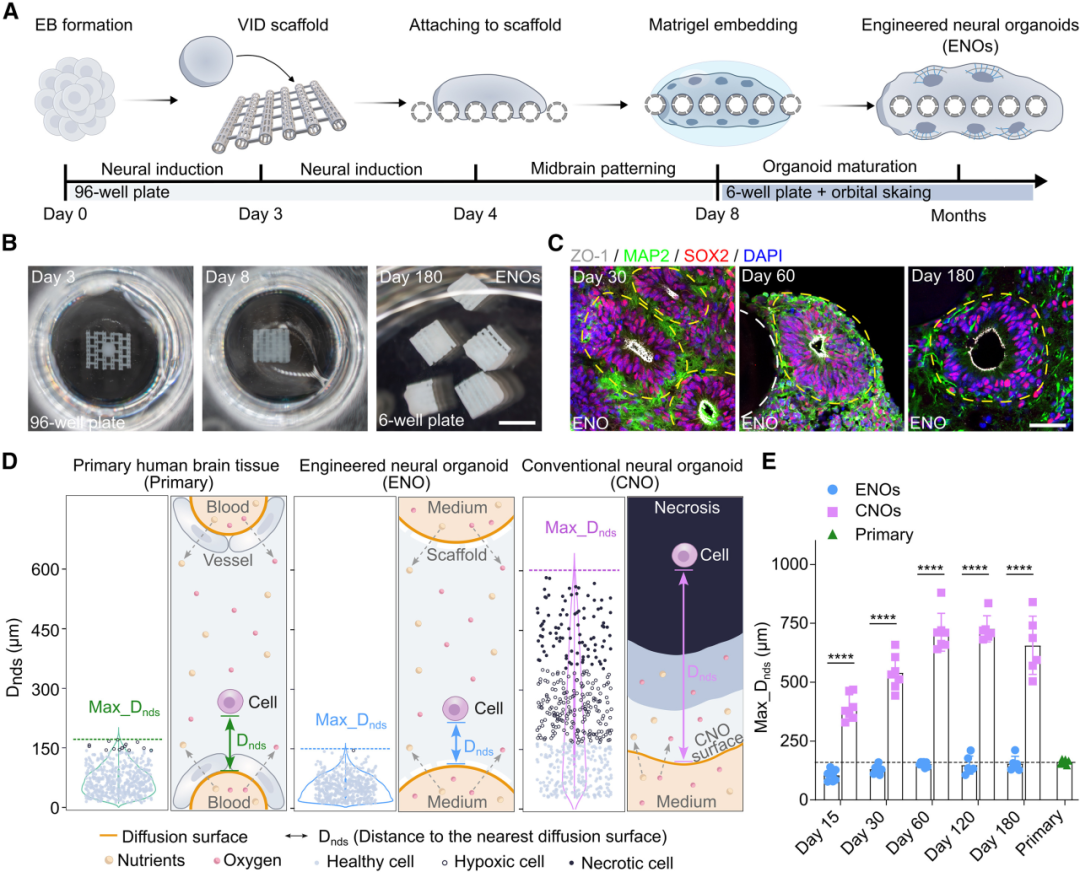
圖1:在VID指甲上聲張的腦類器官成功發(fā)育以形成多個(gè)腦室區(qū)(VZ)結(jié)構(gòu)為特征
02 VID支架有效改善類器官內(nèi)部氧氣供應(yīng)
為了進(jìn)一步證明VID支架切實(shí)地利用擴(kuò)散管網(wǎng)絡(luò)直接向類器官細(xì)胞提供了營(yíng)養(yǎng)物質(zhì)、氧氣和信號(hào)分子,研究人員隨后對(duì)其進(jìn)行了全面表征。定量染色結(jié)果再次強(qiáng)調(diào),ENOs直至培養(yǎng)第180也未出現(xiàn)缺氧現(xiàn)象,且三種不同分子量的生長(zhǎng)因子在灌注后均勻且高效分布于ENOs。總的來(lái)說(shuō),培養(yǎng)過(guò)程中ENOs內(nèi)部細(xì)胞的氧氣供應(yīng)充足,缺氧區(qū)域顯著減少,細(xì)胞活力顯著提高。
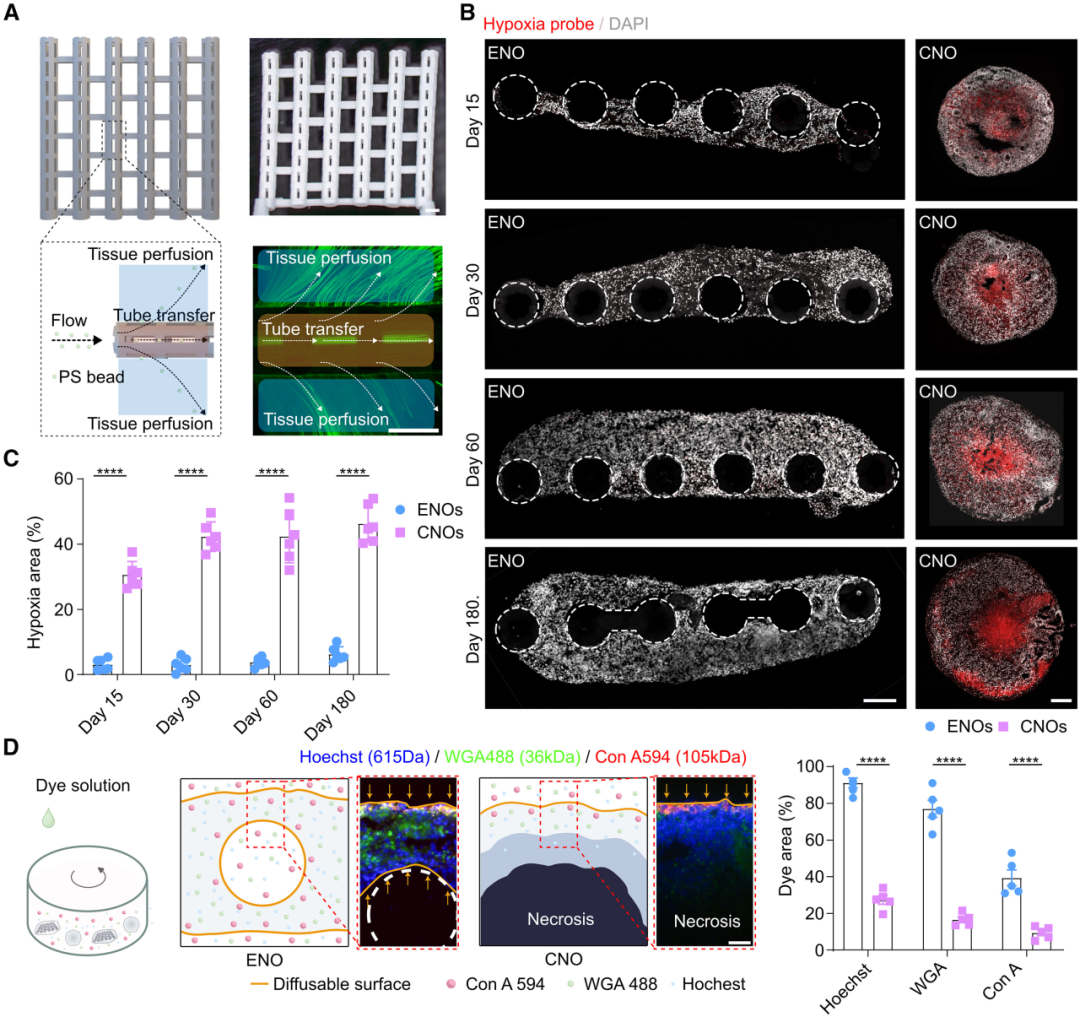
圖2:ENOs中介質(zhì)、氧和信號(hào)分子的擴(kuò)散增強(qiáng)
03 VID支架促進(jìn)中腦特異性分化
在培養(yǎng)第15到第180天是神經(jīng)祖細(xì)胞(NPC)擴(kuò)展和神經(jīng)成熟的關(guān)鍵階段,在ENOs和CNOs中均觀察到了成熟神經(jīng)元和VZ標(biāo)志物的發(fā)生。但CNOs在第15天開(kāi)始出現(xiàn)明顯的壞死核心,從第15天到180天繼續(xù)擴(kuò)大。而ENOs缺乏壞死核心,在同一時(shí)間內(nèi)非壞死增殖區(qū)也顯示較少的細(xì)胞死亡。此外,但ENOs在60-180天的增殖細(xì)胞比例(ki67)高于CNOs,表現(xiàn)出更強(qiáng)勁的發(fā)育態(tài)勢(shì)。
scRNA-seq測(cè)序分析顯示,與傳統(tǒng)類器官相比,ENOs中的神經(jīng)前體細(xì)胞具有更低的內(nèi)質(zhì)網(wǎng)應(yīng)激、缺氧和凋亡相關(guān)基因的表達(dá),而與細(xì)胞周期、DNA復(fù)制和神經(jīng)元發(fā)育相關(guān)的基因表達(dá)更高,表明ENOs的神經(jīng)新生更為頻繁與持續(xù)。
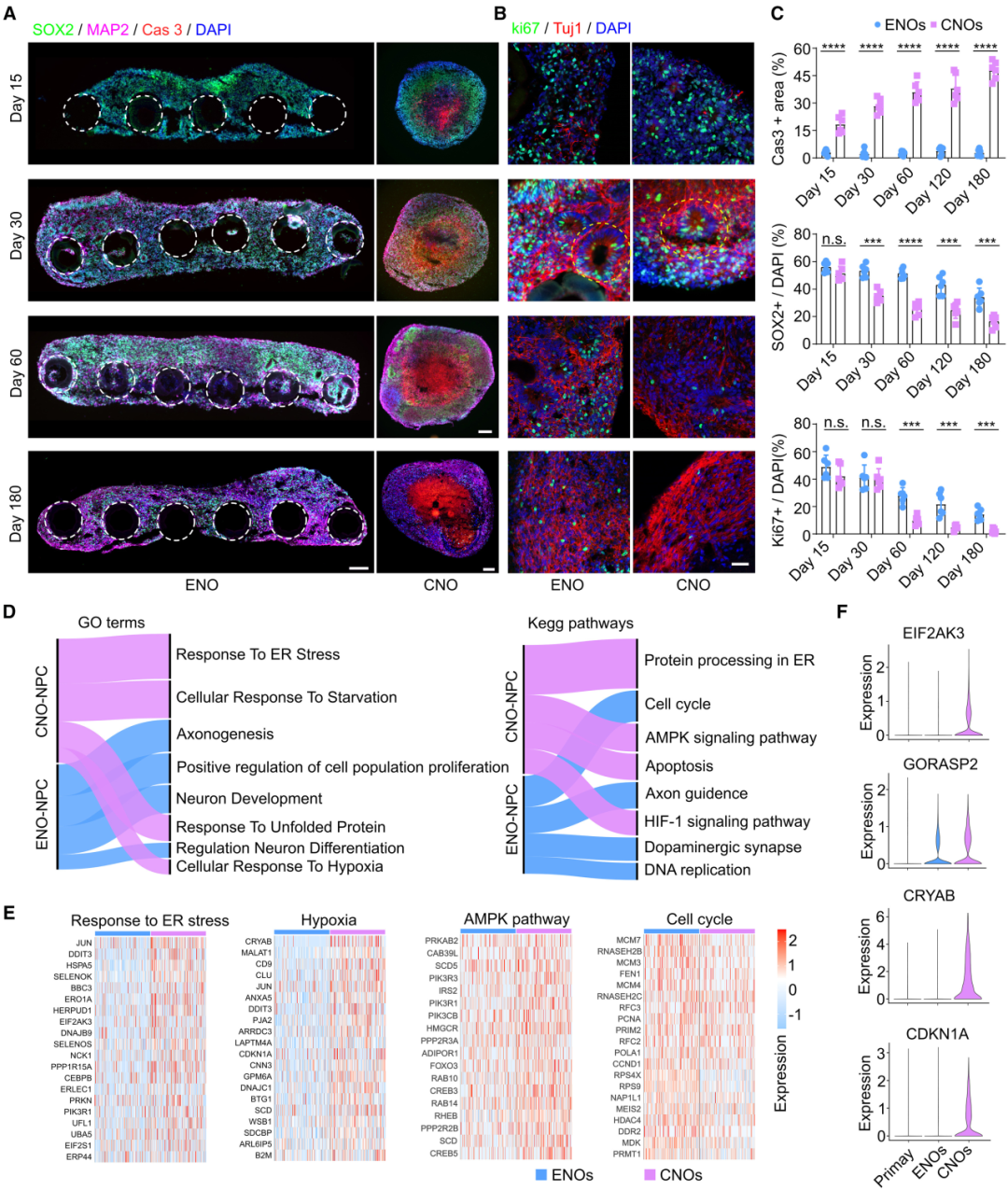
圖3:VID支架維持了ENOs中的神經(jīng)新生
需要注意的是,隨著CNOs中的細(xì)胞死亡與應(yīng)激的發(fā)生,細(xì)胞類型的分化也受到了嚴(yán)重限制。相較而言,ENOs VZ中存在更高比例的LMX1A多巴胺能祖細(xì)胞(46%對(duì)比23%)。在整體非壞死區(qū)域內(nèi),ENOs也擁有更高比例的多巴胺能神經(jīng)元(37%對(duì)比25%),且這些神經(jīng)元在類器官中的分布更加均勻,形成了更復(fù)雜的神經(jīng)網(wǎng)絡(luò)結(jié)構(gòu)。進(jìn)一步的分析顯示,ENOs與原代人胚胎中腦具有更高的相似性。與CNOs相比,ENOs中未識(shí)別細(xì)胞(5%對(duì)比14%)和非多巴胺能神經(jīng)元(8%對(duì)比19%)減少,多巴胺能神經(jīng)元(22%對(duì)比15%)和祖細(xì)胞(35%對(duì)比28%)增加,中腦特異性標(biāo)記的基因表達(dá)也有顯著上調(diào),表明ENOs中腦特異性神經(jīng)發(fā)生增強(qiáng)。
總之,與傳統(tǒng)類器官相比,ENOs在中腦特異性身份、氧氣代謝、神經(jīng)元成熟和網(wǎng)絡(luò)活動(dòng)等方面表現(xiàn)出更符合生理特征的功能。
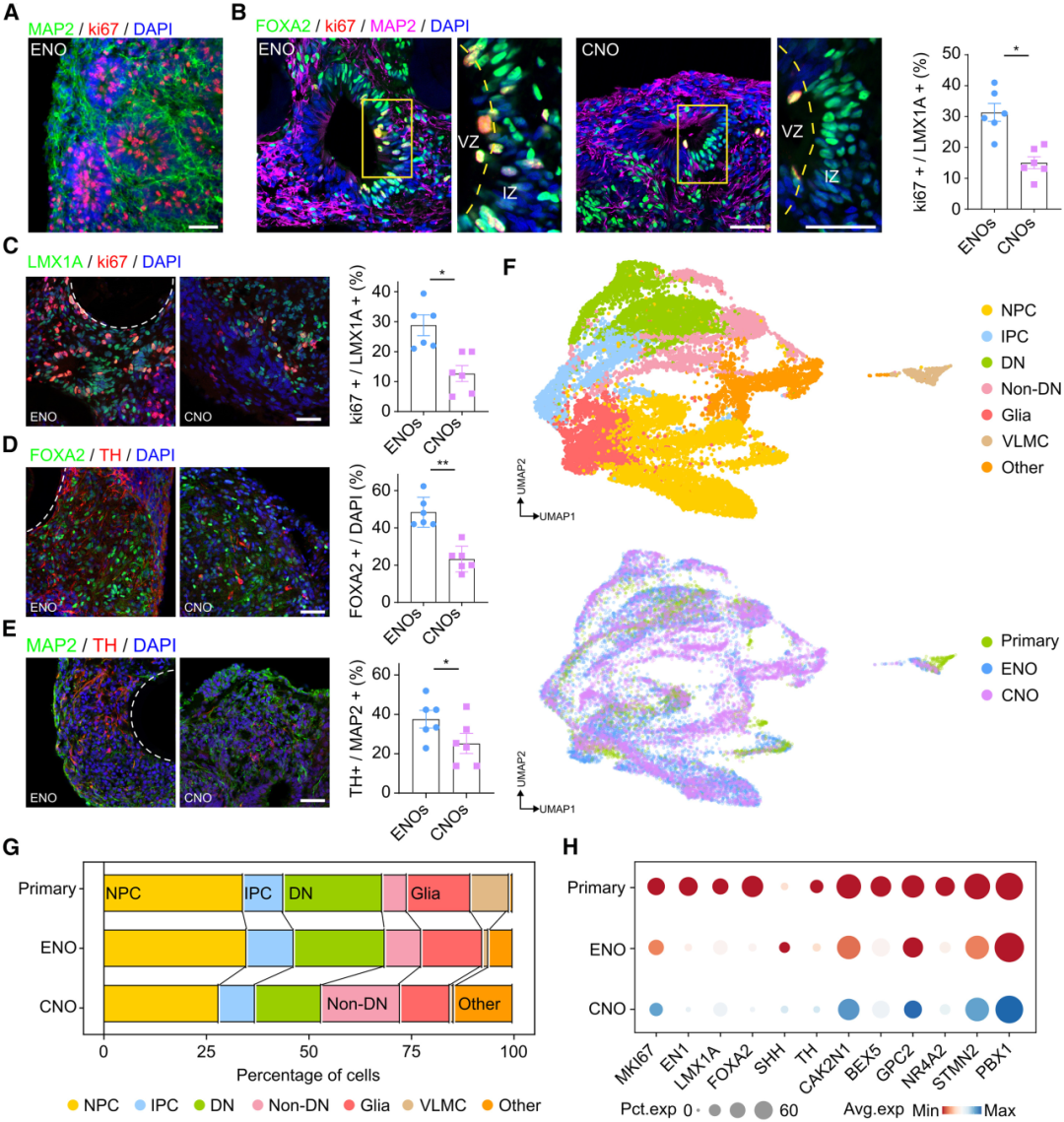
圖4:VID支架增強(qiáng)了中腦區(qū)域特異性分化
04 VID支架增強(qiáng)神經(jīng)功能
使用多電極陣列(MEA)系統(tǒng)記錄ENOs和傳統(tǒng)類器官的神經(jīng)活動(dòng),研究人員發(fā)現(xiàn)ENOs在培養(yǎng)90天后表現(xiàn)出更均勻的神經(jīng)活動(dòng)和更復(fù)雜的神經(jīng)網(wǎng)絡(luò)連接。且ENOs的神經(jīng)元放電頻率、爆發(fā)頻率和活躍電極數(shù)量均顯著高于傳統(tǒng)類器官,功能連接性也更強(qiáng),具有定義良好的神經(jīng)元網(wǎng)絡(luò),整體神經(jīng)活動(dòng)顯著優(yōu)于CNOs。
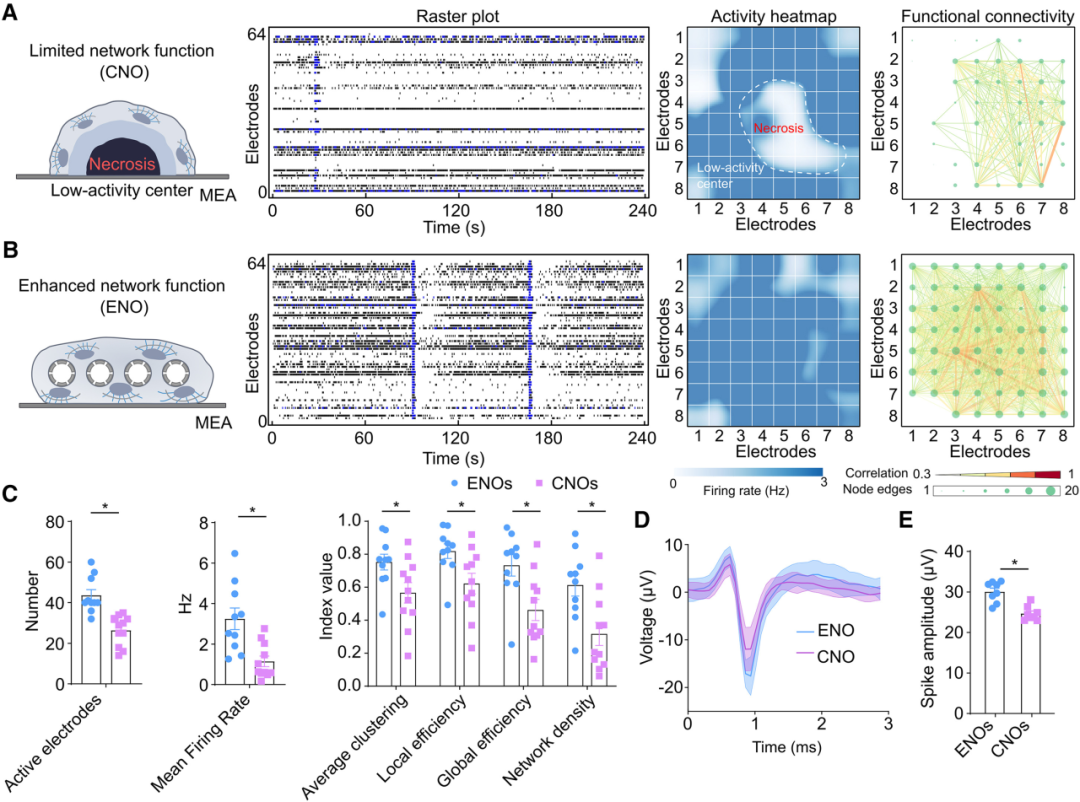
圖5:VID支架改善了ENOs的神經(jīng)活動(dòng)和功能神經(jīng)網(wǎng)絡(luò)
05 ENOs是更良好的藥物測(cè)試平臺(tái)
接下來(lái)研究人員,研究了ENOs和CNOs對(duì)藥物的反應(yīng),發(fā)現(xiàn)VID支架還解決了靠近MEA電極的神經(jīng)元可能失去電活動(dòng),及藥物難以到達(dá)MEA電極附近神經(jīng)元造成的療效不準(zhǔn)的問(wèn)題。
MEA結(jié)果顯示,ENOs在處理后表現(xiàn)出明顯的藥理效應(yīng),包括放電事件和爆發(fā)次數(shù)減少,網(wǎng)絡(luò)活動(dòng)同步性喪失,且相關(guān)基因表達(dá)變化與藥物作用機(jī)制相符。而CNOs在相同處理?xiàng)l件下未表現(xiàn)出顯著的電活動(dòng)變化。scRNA-seq進(jìn)一步證實(shí)了處理對(duì)ENOs中神經(jīng)元和星形膠質(zhì)細(xì)胞基因表達(dá)的影響,表明ENOs在藥物反應(yīng)方面更符合生理實(shí)際情況。
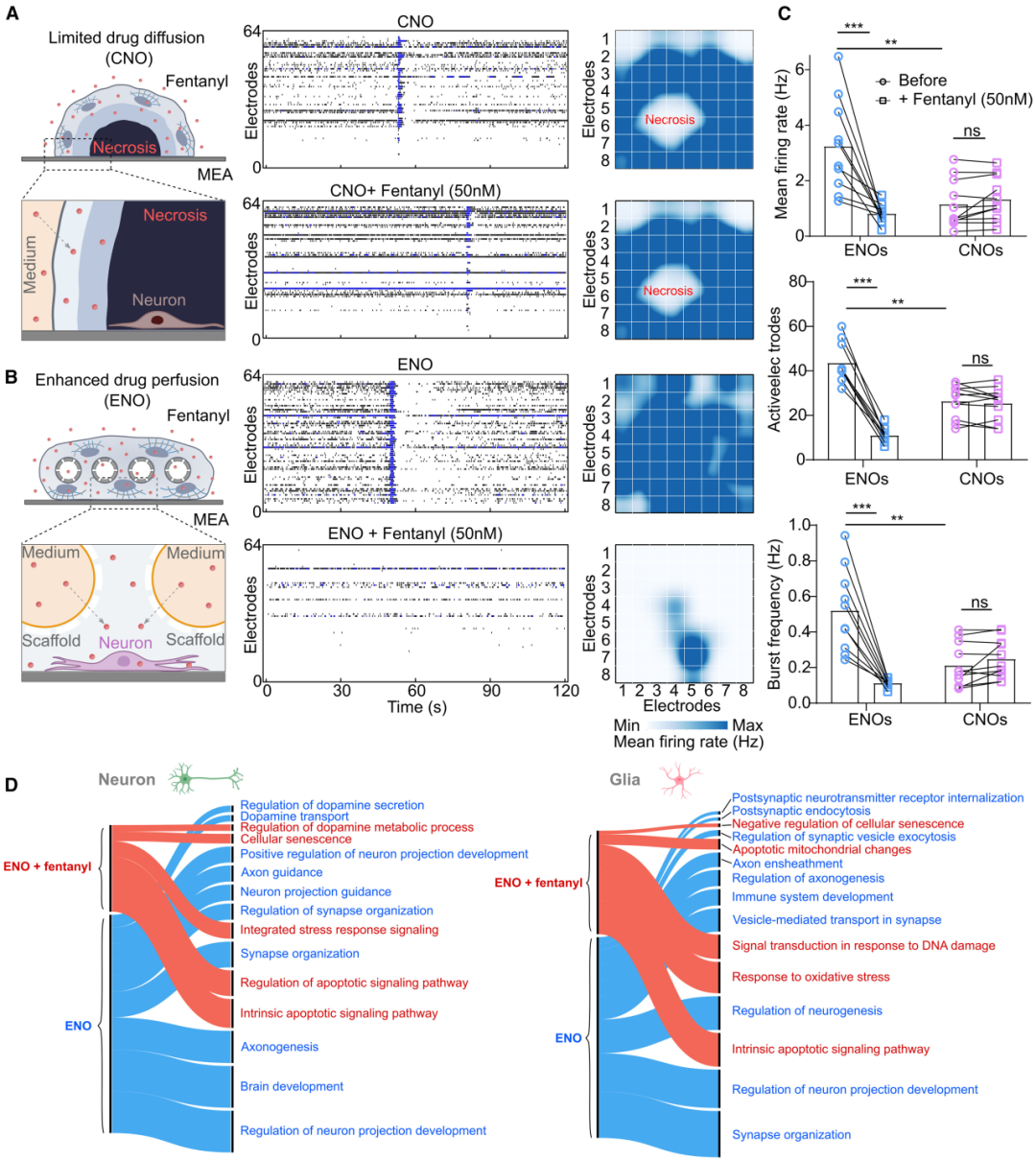
圖6:VID支架增強(qiáng)了藥理學(xué)反應(yīng)
06 總結(jié)
本研究開(kāi)發(fā)的VID支架解決了傳統(tǒng)類器官培養(yǎng)中的擴(kuò)散限制問(wèn)題,還能支持類器官在生理灌注樣條件下的長(zhǎng)期培養(yǎng)和功能維持,可顯著改善類器官的生理功能和藥物反應(yīng)表型,為藥物篩選和疾病模型研究提供了更準(zhǔn)確的平臺(tái)。
作者在最后提到,未來(lái)的研究可以集中在開(kāi)發(fā)更先進(jìn)的生物墨水和高精度3D打印技術(shù),以克服當(dāng)前支架設(shè)計(jì)的局限性。此外,將人類臍靜脈內(nèi)皮細(xì)胞或其他來(lái)源的內(nèi)皮細(xì)胞整合到支架中,形成更完整的可灌注血管網(wǎng)絡(luò),也是未來(lái)研究的一個(gè)重要方向。
近岸蛋白相關(guān)產(chǎn)品
近岸蛋白提供多種類器官體外培養(yǎng)全方案,包括基質(zhì)膠、培養(yǎng)基、相關(guān)細(xì)胞因子等:
經(jīng)類器官培養(yǎng)驗(yàn)證的完全培養(yǎng)基
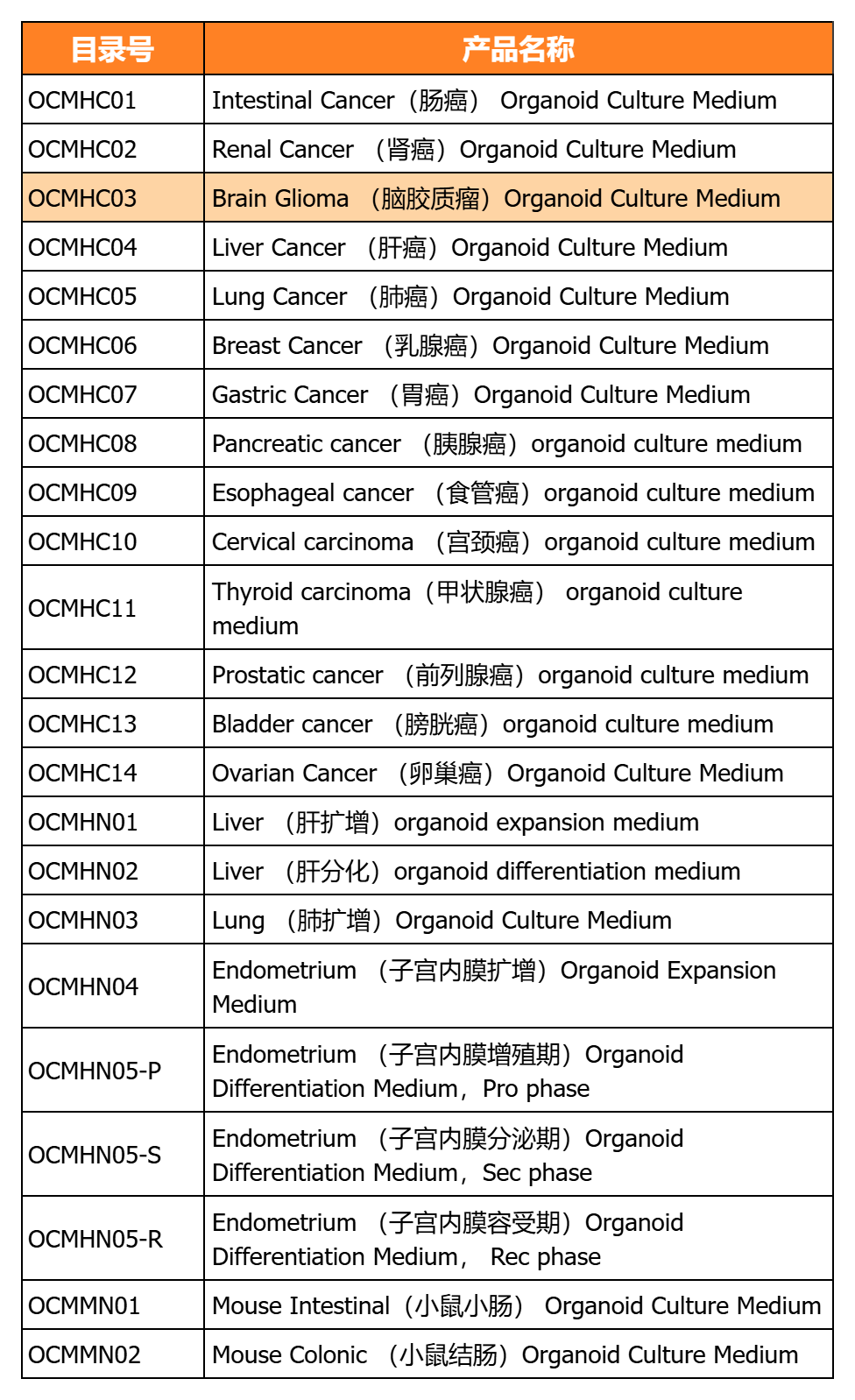
經(jīng)類器官培養(yǎng)驗(yàn)證的細(xì)胞因子
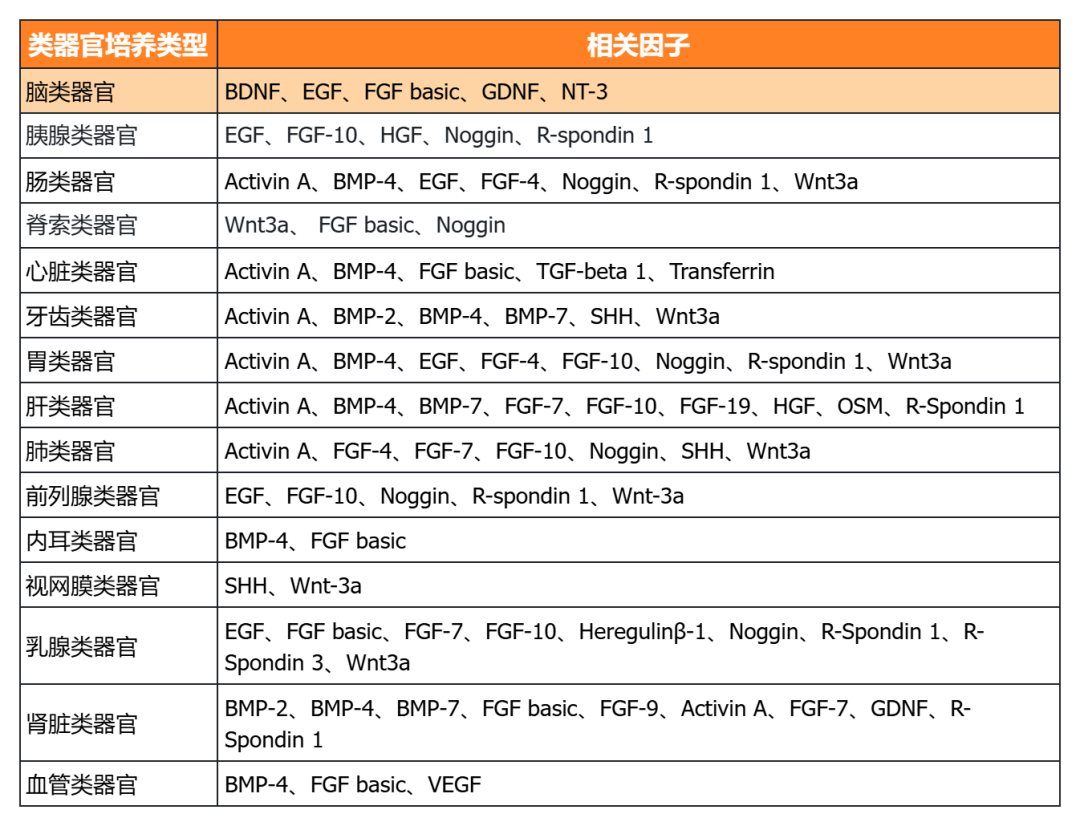
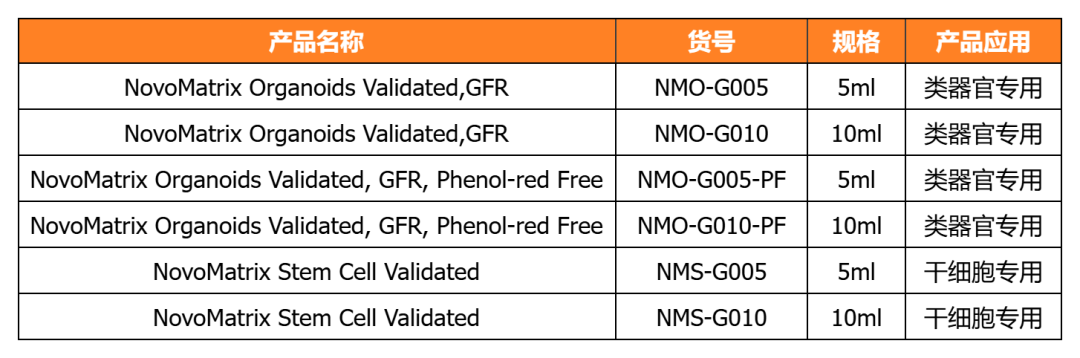
NovoMatrix 基質(zhì)膠
掃碼添加小編,加入類器官培養(yǎng)交流群
技術(shù)支持答疑解惑,前沿進(jìn)展定期分享

??掃碼添加小編微信
參考資料
1. Cai, Hongwei et al. “Vascular network-inspired diffusible scaffolds for engineering functional midbrain organoids.” Cell stem cell, S1934-5909(25)00049-9. 8 Mar. 2025, doi:10.1016/j.stem.2025.02.010
