【答疑解惑】類器官培養(yǎng)100問-上篇50問
類器官是能夠在體外三維培養(yǎng),并表現(xiàn)出相應(yīng)器官生物學(xué)特征的“最小系統(tǒng)”。雖然對(duì)于類器官的研究日趨成熟,但大家總會(huì)有這樣那樣的小困惑:為什么要用上皮細(xì)胞培養(yǎng)?為什么培養(yǎng)基的成分這么復(fù)雜?
近岸蛋白憑借構(gòu)建類器官平臺(tái)的實(shí)踐經(jīng)驗(yàn)和深厚的文獻(xiàn)積累,圍繞類器官培養(yǎng)基本操作(基礎(chǔ)篇),腫瘤類器官培養(yǎng)(PDO篇),以及類器官應(yīng)用等多個(gè)主題方向,精心整理了類器官培養(yǎng)常見問題100問,今天為大家?guī)砩掀?/span>
基礎(chǔ)篇
Q1: 類器官培養(yǎng)對(duì)于起始細(xì)胞的來源有要求嗎?
A1: 目前培養(yǎng)的類器官主要來源于上皮細(xì)胞,對(duì)于非上皮細(xì)胞來源的類器官培養(yǎng)方式還需要進(jìn)一步研究。
Q2: 類器官按照起始細(xì)胞的類型,分為幾種呢?
A2: 常見的類器官根據(jù)起始細(xì)胞的類型,可以分為兩種:
(1)腫瘤組織來源的腫瘤類器官;
(2)干細(xì)胞來源的類器官,包括:多能性干細(xì)胞 (PSC) /成體干細(xì)胞 (ASC)以及誘導(dǎo)多能干細(xì)胞(iPSC)。
Q3: 類器官是由單一種類細(xì)胞組成的嗎?
A3: 類器官并不是單一細(xì)胞組成的結(jié)構(gòu),而是由具有干細(xì)胞性質(zhì)的起始細(xì)胞進(jìn)行分裂和分化,并將多種類型的細(xì)胞自組裝的結(jié)構(gòu),自組裝后的形態(tài)和功能與體內(nèi)相應(yīng)器官相似。
Q4:在沒有新鮮組織的情況下,可以用凍存組織提取的原代細(xì)胞進(jìn)行3D培養(yǎng)嗎?
A4:可以的。已有學(xué)者驗(yàn)證過,將人結(jié)腸癌、甲狀腺癌、肺癌、腎癌和肝癌的手術(shù)組織切碎后,以梯度降溫的方式進(jìn)行冷凍,最終在液氮中保存15-18個(gè)月后進(jìn)行復(fù)蘇和原代細(xì)胞提取,分別對(duì)細(xì)胞進(jìn)行2D和3D培養(yǎng),證實(shí)了凍存對(duì)于細(xì)胞活力和生長速度均無顯著影響【1】。
當(dāng)然,由于組織來源不同、凍存條件不同,還需要大家根據(jù)實(shí)際情況進(jìn)行驗(yàn)證,新鮮組織提取的細(xì)胞依然是3D培養(yǎng)的最佳選擇。
Q5:類器官可以像細(xì)胞一樣進(jìn)行凍存和復(fù)蘇嗎?
A5:類器官可以凍存,通常會(huì)在傳代2-3次之后選擇凍存。為了達(dá)到最佳的效果,可以選擇類器官成熟(傳代7-10次)后再進(jìn)行凍存。
Q6:類器官的尺寸需要進(jìn)行控制嗎?
A6:是的,主要的原因是類器官內(nèi)部缺乏循環(huán)系統(tǒng)。
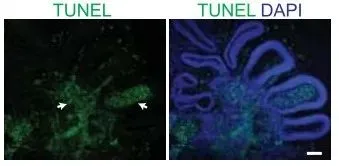
當(dāng)類器官的尺寸較大時(shí),靠近中心的細(xì)胞難以和外界進(jìn)行氧氣和營養(yǎng)成分的交換。因此這個(gè)結(jié)構(gòu)尺寸越大,死亡的細(xì)胞就越多(見下圖)【2】。我們?cè)谂囵B(yǎng)的過程中,需要控制類器官的大小在4-5mm以內(nèi)。未來的類器官技術(shù)可以與血管類器官結(jié)合在一起,建立一個(gè)功能性的封閉循環(huán)系統(tǒng),用以培養(yǎng)出更大尺寸的類器官。
TUNEL染色表明較大尺寸的類器官中心有大量細(xì)胞死亡(綠色),比例尺為100μm【2】
Q7:類器官傳代的標(biāo)準(zhǔn)是什么?
A7:類器官的傳代通常是根據(jù)培養(yǎng)的時(shí)間判斷。一般在7-14天時(shí)進(jìn)行第一次傳代,后續(xù)則每7-10天傳代一次【3】。
Q8:類器官可以進(jìn)行多少次傳代?
A8:大部分類器官可以在體外連續(xù)傳代10次(>6個(gè)月),甚至有些類器官可以連續(xù)傳代20次(>12個(gè)月)并且維持原有的生長速度【4】。
Q9: 鑒定類器官的方法有哪些?
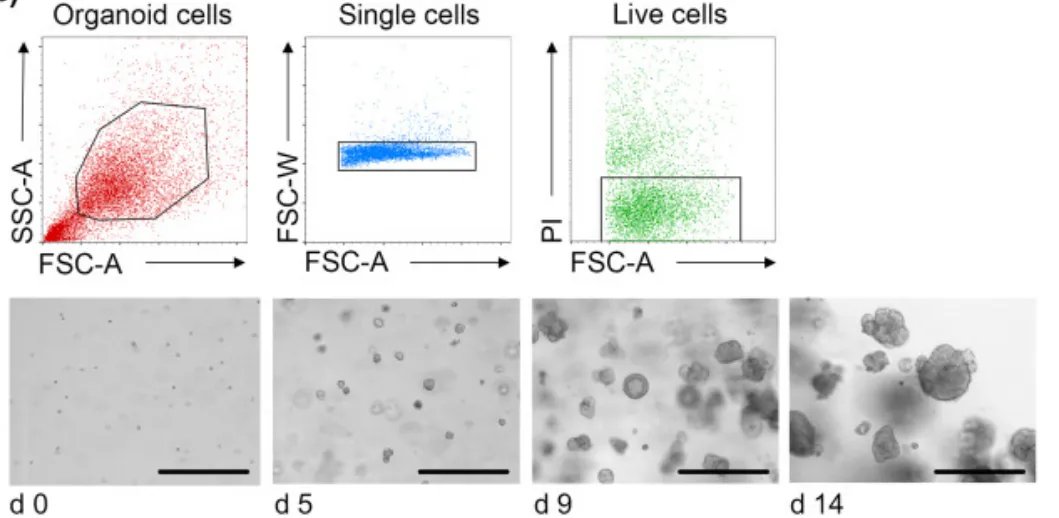
A9: 初步可以通過顯微鏡和H&E染色觀察形態(tài);然后可以用Western Blot、qRT-PCR、免疫熒光、流式細(xì)胞術(shù)檢測該類器官是否表達(dá)相應(yīng)的biomarker;基因測序可以鑒定所培養(yǎng)的類器官是否有某些特征丟失;對(duì)于部分類器官,還可以檢測其是否具有功能,例如:已有研究檢測出胃類器官可以分泌胃酸,心臟類器官可以自主跳動(dòng)。
Q10: 類器官是如何按照我們的意愿進(jìn)行定向分化的?
A10: 在進(jìn)行類器官培養(yǎng)前,我們需要了解該器官在體內(nèi)的發(fā)育過程,及早期發(fā)育相關(guān)的信號(hào)通路。
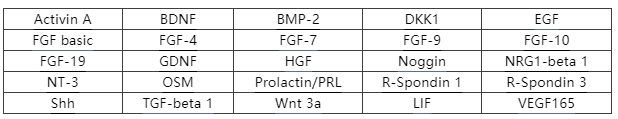
以胃類器官培養(yǎng)為例:胃由前后腸發(fā)育而來,早期發(fā)育需要由多種信號(hào)通路共同調(diào)控。那么在體外我們需要通過添加細(xì)胞因子的方式,指導(dǎo)激活/抑制相應(yīng)的信號(hào)通路,來達(dá)到相同的效果,如:PSCs在Activin A的作用下分化為內(nèi)胚層,Wnt3a、FGF-4和Noggin指導(dǎo)細(xì)胞向向前腸分化【5】。
PDO篇
患者來源類器官(Patient Derived Organoid, PDO)是體外評(píng)估藥物的有效模型,目前較常用于患者的個(gè)性化用藥和抗癌藥物的測試領(lǐng)域。今天小編整理了部分PDO培養(yǎng)中常遇到的問題,希望能夠?qū)Ω魑恍』锇橛兴鶐椭?/span>
Q11:對(duì)于病人的腫瘤組織,需要怎樣處理盡量避免污染?
A11:1、將腫瘤組織置于70%-75%乙醇中30秒,清洗表面血塊等雜物,并用剪刀對(duì)組織稍加修整。
2、放入含有青/鏈霉素、兩性霉素B、慶大霉素(單獨(dú)使用某一種或幾種組合)的PBS緩沖液進(jìn)行進(jìn)一步清洗。
3、原代細(xì)胞提取前,建議先進(jìn)行支原體檢測,防止支原體污染。
Q12: PDO對(duì)于藥敏反應(yīng)的準(zhǔn)確度是怎樣的呢?
A12:有數(shù)據(jù)表明,PDO對(duì)藥敏反應(yīng)的陽性預(yù)測值(預(yù)測某一特定藥物有效)為88%,陰性預(yù)測值(預(yù)測某一特定藥物無效)為100%,敏感性達(dá)100%,特異性為93%【6】。
Q13:病灶和癌旁培養(yǎng)出的類器官有差別嗎?腫瘤組織的取材部位有什么要求?
A13:原發(fā)病灶和癌旁來源的腫瘤類器官是有差別的。
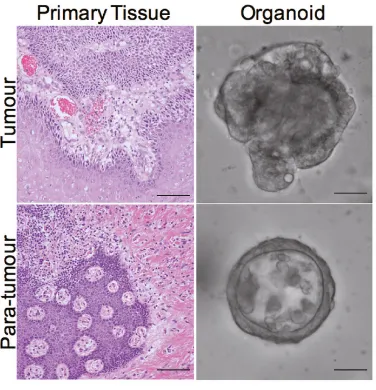
如:從形態(tài)上看,原發(fā)病灶來源的類器官比癌旁來源的類器官更具有侵襲性的結(jié)構(gòu)【7】。
由于腫瘤具有異質(zhì)性,因此類器官存在差異也是很常見的。如果想要盡量減小建模或藥物篩選的誤差,可以考慮多點(diǎn)位取材。
原發(fā)病灶來源的類器官比癌旁來源的類器官更具有侵襲性的結(jié)構(gòu)【7】
Q14:PDO培養(yǎng)的成功率是多少?成功率和是否進(jìn)行治療有關(guān)系嗎?
A14:不同類型來源的PDO成功率略有不同,大部分的PDO培養(yǎng)成功率在63%-70%左右【6】,并且臨床治療對(duì)于這個(gè)統(tǒng)計(jì)結(jié)果影響不大【8】。通過縮短樣本離體時(shí)間和操作步驟,可以適當(dāng)提高成功率。
Q15:凍存多長時(shí)間內(nèi)的組織可以用于類器官培養(yǎng)?
A15:對(duì)于凍存在-80℃的組織,6周之內(nèi)復(fù)蘇并進(jìn)行類器官培養(yǎng)是最佳選擇【9】。當(dāng)然如果是保存在液氮中,保存的時(shí)間可以更久一些。
Q16:原代細(xì)胞提取時(shí),通常會(huì)混有增殖非常迅速的成纖維細(xì)胞,應(yīng)該怎樣快速去除呢?
A16:成纖維細(xì)胞主要有兩種去除方式:
1、鑒于成纖維細(xì)胞貼壁不牢的性質(zhì),可以采用反復(fù)貼壁的方式去除大部分成纖維細(xì)胞。
2、目前已有商用的成纖維細(xì)胞去除試劑,但是否會(huì)影響類器官的培養(yǎng)還需要實(shí)驗(yàn)驗(yàn)證。
Q17:培養(yǎng)腫瘤類器官需要原始腫瘤組織的大小是多少?活檢樣本量足夠嗎?
A17:手術(shù)組織大概需要3顆黃豆大小以上,穿刺活檢樣本需要至少3針,內(nèi)鏡活檢至少鉗取6顆以上。
Q18:從腫瘤組織中提取原代細(xì)胞后,發(fā)現(xiàn)細(xì)胞呈紅色,這是為什么?
A18:紅色主要是由于腫瘤組織中的大量紅細(xì)胞所導(dǎo)致的。
首先,可以在拿到組織后盡量多清洗幾次,能夠去除大部分的紅細(xì)胞;
其次,可以使用商品化的紅細(xì)胞裂解液。紅細(xì)胞裂解液的原理是去除無核細(xì)胞,因此不會(huì)影響其他有核細(xì)胞的正常培養(yǎng)。
Q19:怎樣構(gòu)建含有PDO的腫瘤微環(huán)境?
A19:目前構(gòu)建含有PDO的腫瘤微環(huán)境主要有三種方式:
(I)將腫瘤組織經(jīng)過物理或酶解分離后,在細(xì)胞外基質(zhì)(Matrigel或BME)中進(jìn)行類器官培養(yǎng);同時(shí)分離外源性免疫細(xì)胞(通常來源于自體外周血或腫瘤組織),隨后與生長的類器官進(jìn)行共培養(yǎng)。
(II)將腫瘤消化后形成的球狀組織與膠原蛋白混合,并接種到微流體培養(yǎng)裝置中,即腫瘤細(xì)胞與樣本中的固有免疫微環(huán)境共同培養(yǎng),形成天然TME模型。
(III)將含有免疫細(xì)胞的腫瘤組織物理切割成組織碎片,在包被膠原蛋白凝膠的transwell小室中進(jìn)行培養(yǎng)。凝膠的頂部暴露在空氣中,同時(shí)外皿中的培養(yǎng)基通過可滲透的transwell擴(kuò)散到內(nèi)皿中,形成氣-液交互界面(air–liquid interface, ALI)。腫瘤免疫微環(huán)境的類器官培養(yǎng)系統(tǒng)建立可參考“腫瘤微環(huán)境的類器官模型,助力耐藥腫瘤的治療”。
Q20:由于取到的腫瘤組織太小了,培養(yǎng)的類器官數(shù)目不足以進(jìn)行后續(xù)的檢測。我可以將類器官傳代擴(kuò)增嗎?
A20:對(duì)于腫瘤來源的類器官一般是不建議傳代的,因?yàn)閭鞔蟮谋硇蜁?huì)和體內(nèi)情況略有差異。文獻(xiàn)中的PDO一般會(huì)控制在2-3代【9】,最多不超過5代【10】。
如果細(xì)胞數(shù)目太少,傳代5次依然不能滿足測試需求,可以考慮將檢測的方式改變一下,比如從96孔板換成384孔板,甚至更小體系的微流控芯片。
Q21:腫瘤組織中會(huì)存在正常細(xì)胞嗎?怎么去除這些正常細(xì)胞?
A21:即使是肉眼判斷為腫瘤的組織中,也會(huì)混有一部分正常細(xì)胞。因此在進(jìn)行類器官培養(yǎng)前,可以先將原代細(xì)胞進(jìn)行流式分選或磁珠分選,得到腫瘤細(xì)胞再進(jìn)行類器官培養(yǎng)。
Q22: 正常細(xì)胞是否也會(huì)生長為類器官?腫瘤類器官培養(yǎng)時(shí)怎么去除正常類器官?
A22:由于腫瘤組織中通常混有一些健康細(xì)胞,因此培養(yǎng)出的腫瘤類器官很有可能混雜了來源于正常上皮的類器官。為了得到更純的PDO,除了Q1中提到的對(duì)原代細(xì)胞進(jìn)行處理外,也可以對(duì)類器官群進(jìn)行“純化”,主要有以下三種途徑【6】。
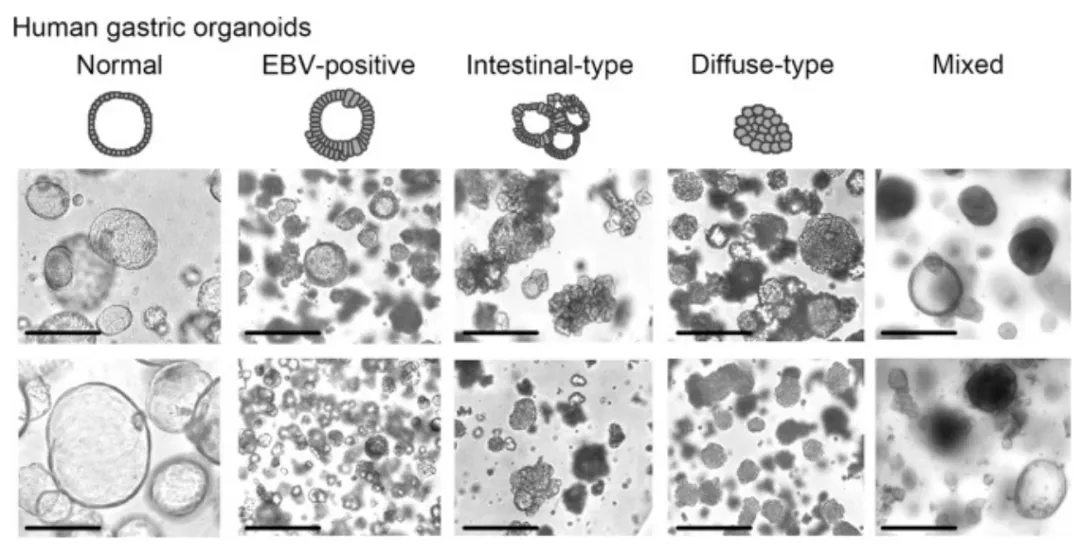
1、利用正常類器官和PDO的形態(tài)不同,在鏡下進(jìn)行手動(dòng)篩選。圖1展示了胃類器官和腫瘤類器官的形態(tài)差異:正常的胃類器官呈球形,由單層上皮細(xì)胞組成,具有較大的管腔;而腫瘤類器官通常是囊狀,且有多層細(xì)胞形態(tài)。
正常胃類器官和腫瘤類器官的鏡下形態(tài)不同,比例尺300μm【6】
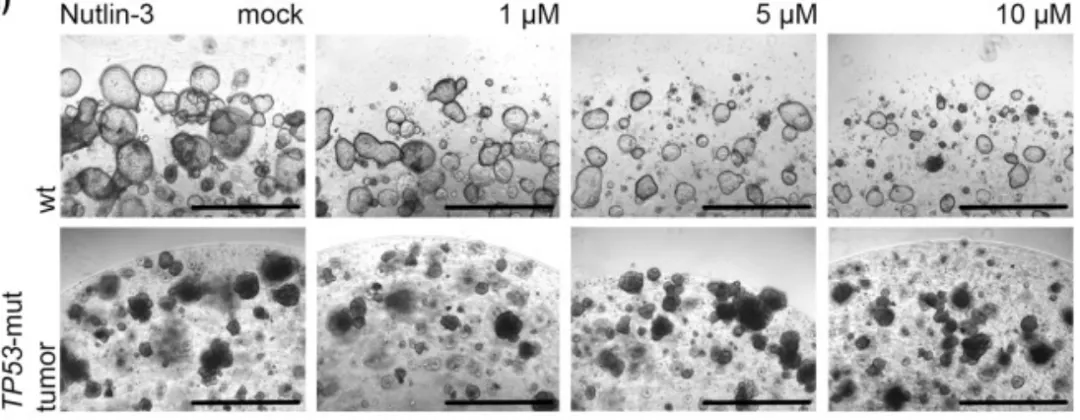
2、通過調(diào)節(jié)培養(yǎng)基中的組分進(jìn)行篩選。如:大多數(shù)胃癌表現(xiàn)出TP53突變,這一突變使PDO表現(xiàn)出對(duì)Nutlin-3更耐受,而正常類器官則會(huì)死亡。
3、將類器官消化為單個(gè)細(xì)胞后,流式分選出腫瘤細(xì)胞。
腫瘤類器官的單細(xì)胞流式分選,比例尺400 μm【6】
Q23:進(jìn)行藥敏實(shí)驗(yàn)時(shí),需要將PDO從基質(zhì)膠中消化下來嗎?
A23:可能有很多小伙伴擔(dān)心基質(zhì)膠會(huì)阻礙藥物進(jìn)入到PDO中,但無數(shù)實(shí)驗(yàn)已經(jīng)證明,基質(zhì)膠內(nèi)的PDO是可以對(duì)藥物進(jìn)行響應(yīng)的;而且PDO需要三維結(jié)構(gòu)才能模擬體內(nèi)狀況,如果沒有了基質(zhì)膠的支撐,藥敏實(shí)驗(yàn)的準(zhǔn)確性會(huì)打折扣。
Q24:PDO實(shí)驗(yàn)可以代替動(dòng)物模型(PDX)嗎?
A24:PDO相較于動(dòng)物模型有很多優(yōu)點(diǎn),例如成本低、耗時(shí)短、可以進(jìn)行大規(guī)模培養(yǎng)和實(shí)驗(yàn)等。不過在藥物代謝、癌癥的浸潤、轉(zhuǎn)移等方向的研究則需要?jiǎng)游飳?shí)驗(yàn)來進(jìn)行。
Q25:在培養(yǎng)過程中,PDO生長情況與之前相比異常,主要表現(xiàn)為生長周期變短,增殖迅速,這是什么原因?
A25:如果PDO在培養(yǎng)過程中突然增殖迅速,可能是某些雜質(zhì)細(xì)胞(如成纖維細(xì)胞)的大量生長導(dǎo)致的,此時(shí)最好進(jìn)行切片染色,觀察一下是否存在這些細(xì)胞的污染。如果不是這個(gè)原因,則考慮是突變引起的,最好進(jìn)行測序驗(yàn)證并與初代PDO進(jìn)行比對(duì)。
Q26:怎樣檢測PDO對(duì)藥物的敏感性?
A26:主要有兩種途徑進(jìn)行檢測。
1、進(jìn)行細(xì)胞活力檢測,即線粒體呼吸(耗氧率)、糖酵解 (H+濃度)等;
2、可以通過高內(nèi)涵成像技術(shù)進(jìn)行分析。
Q27:PDO和腫瘤原代細(xì)胞的藥敏實(shí)驗(yàn)濃度范圍相同嗎?
A27:小編查閱了大量的相關(guān)文獻(xiàn),發(fā)現(xiàn)PDO的藥物測試有效濃度會(huì)整體高于2D細(xì)胞,不同種類的PDO之間也存在很大的倍數(shù)差異。
Q28:PDO模型可以進(jìn)行抗體類藥物篩選嗎?
A28:由于抗體類藥物需要免疫細(xì)胞的參與,因此單純的PDO模型并不適合。可以考慮在PDO的基礎(chǔ)上建立腫瘤微環(huán)境(TME),從而進(jìn)行抗體類藥物的測試。
Q29:腫瘤細(xì)胞系(如Hela細(xì)胞系)可以培養(yǎng)成為PDO嗎?
A29:不可以。PDO需要依賴多種細(xì)胞在體外的自組裝形成,而腫瘤細(xì)胞系沒有自組裝的能力,可能會(huì)形成細(xì)胞團(tuán),但這并不是PDO。
Q30:PDO可以進(jìn)行建庫嗎?
A30:不論是原發(fā)型還是轉(zhuǎn)移型腫瘤,都可以建立PDO樣本庫。但考慮到PDO的培養(yǎng)并不是百分之百成功的(比如CRC-PDO的培養(yǎng)成功率大約是73%【12】),因此建庫所需的樣本量會(huì)比較大。
應(yīng)用篇
類器官是能夠在體外三維培養(yǎng),并表現(xiàn)出相應(yīng)器官生物學(xué)特征的“最小系統(tǒng)”。隨著類器官培養(yǎng)技術(shù)的不斷進(jìn)步,應(yīng)用也越來越廣泛。今天小編整理了一些關(guān)于類器官應(yīng)用方面的問題,希望能夠?qū)Ω魑恍』锇橛兴鶐椭?/span>
Q31:用于疾病研究的類器官需要最大限度減小差異。但在實(shí)際培養(yǎng)過程中,同批次類器官個(gè)體之間、以及不同批次類器官樣本之間均存在顯著差異,這個(gè)問題怎樣克服呢?
A31: 類器官是由不同類型的細(xì)胞組成的結(jié)構(gòu),并且在體外是自組裝的,因此很容易存在同一樣本在相同培養(yǎng)條件下的孔間差異。
如果是用于患者個(gè)性化醫(yī)療的腫瘤類器官,需要更精準(zhǔn)地模擬患者體內(nèi)的特征,這種情況建議采用多個(gè)平行來減小差異;
如果是用于機(jī)制研究或用作疾病模型的類器官,可以考慮利用“微流控液滴技術(shù)”進(jìn)行工程化培養(yǎng),相關(guān)成果已發(fā)表在Cell Reports Medicine【13】。
Q32: 目前培養(yǎng)出的類器官可以進(jìn)行體內(nèi)移植,用于器官重建嗎?
A32:已有動(dòng)物實(shí)驗(yàn)證實(shí)過可行性,比如:腸類器官移植小鼠治療潰瘍性結(jié)腸炎【14】;胰島類器官移植小鼠治療糖尿病【15】。
雖然目前類器官移植尚未進(jìn)入臨床,但在2021年2月,Science【16】首次報(bào)道了利用膽道類器官修復(fù)離體條件下的人類肝臟,實(shí)現(xiàn)了膽道再生,并改善了膽汁性質(zhì)。
Q33:類器官一般長到什么程度可以用來進(jìn)行藥物測試?
A33:這個(gè)問題可以在Nature Protocols【17】找到答案。
對(duì)于新鮮培養(yǎng)的類器官:建議對(duì)低代次類器官(2-3代)進(jìn)行藥物篩選,以最大限度地減少使用過的培養(yǎng)基或體外突變累積對(duì)藥物測試的影響。
對(duì)于經(jīng)過凍存的類器官:由于冷凍/解凍可能導(dǎo)致復(fù)蘇時(shí)器官樣形態(tài)的變化,因此建議類器官至少傳代一次再進(jìn)行藥物篩選。如果出現(xiàn)復(fù)蘇后細(xì)胞活力不佳,則需要延長培養(yǎng)時(shí)間以恢復(fù)細(xì)胞狀態(tài)。
Q34:類器官建立是否成功有怎樣的標(biāo)準(zhǔn)嗎?
A34:1、判斷形態(tài)。顯微鏡下類器官形態(tài)可能為空泡狀、出芽狀、緊密型、松散型等,但整體形態(tài)一致。
2、可以鑒定相應(yīng)的biomarker是否有表達(dá),及分布是否與組織切片相似。
3、是否能夠傳代3次以上,并可以凍存復(fù)蘇。
4、如果有條件的話,可以進(jìn)行測序分析。
Q35:類器官可以進(jìn)行基因編輯嗎?
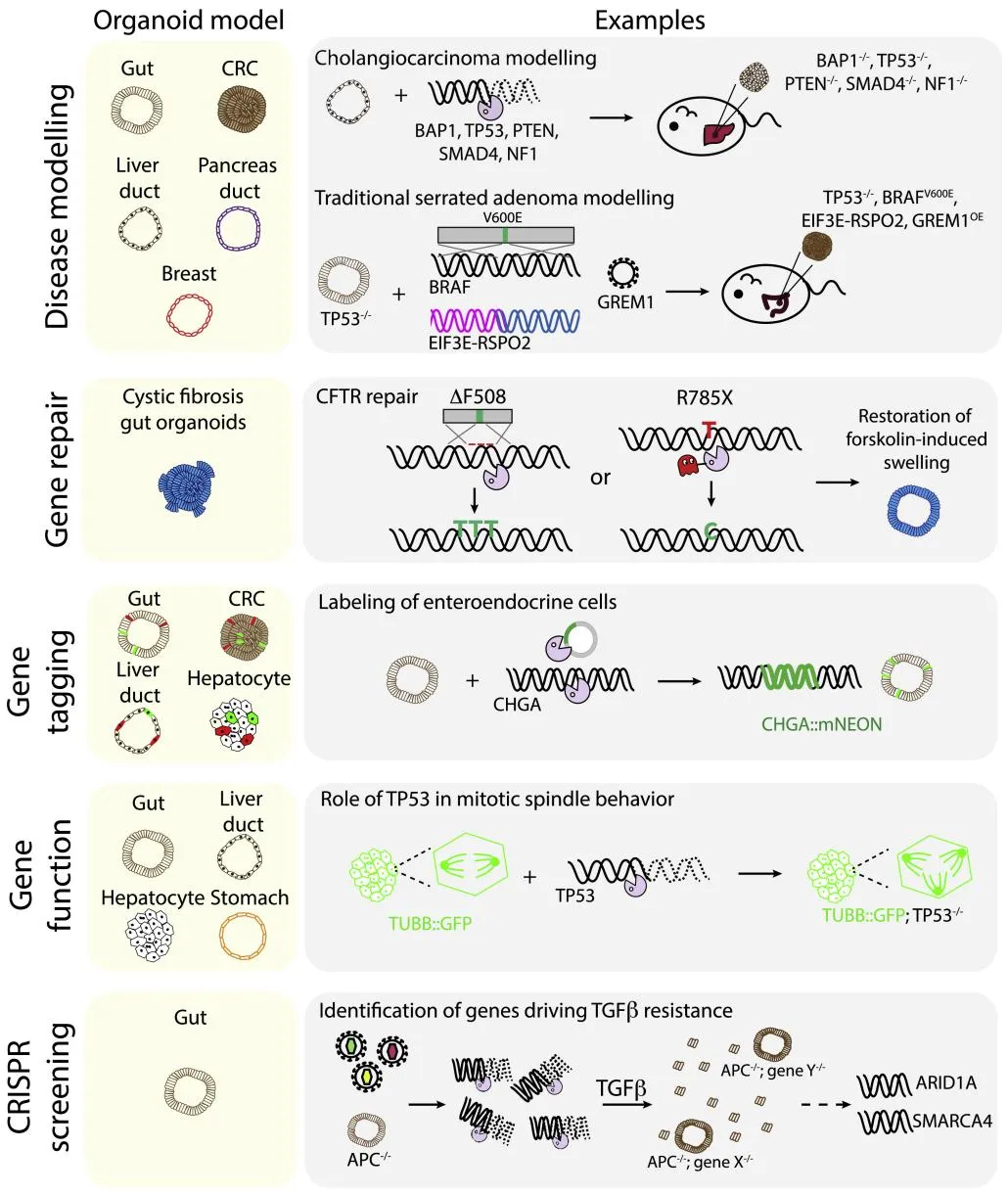
A35:可以,干細(xì)胞來源類器官的基因編輯多用于疾病建模,而腫瘤來源的類器官則多用于尋找疾病相關(guān)突變點(diǎn)或治療靶點(diǎn),下圖列舉了類器官基因編輯的部分研究和應(yīng)用。
類器官基因編輯的部分研究和應(yīng)用【18】
Q36:類器官培養(yǎng)和普通細(xì)胞培養(yǎng)有何不同之處?
A36:1、細(xì)胞來源有區(qū)別:類器官的細(xì)胞來源是具有多能性的上皮細(xì)胞,而普通細(xì)胞培養(yǎng)適用于培養(yǎng)多種類型細(xì)胞;
2、 細(xì)胞培養(yǎng)方式不同:1)類器官需要基質(zhì)膠等材料支撐其三維結(jié)構(gòu),普通細(xì)胞培養(yǎng)則不需要;2) 類器官需要實(shí)現(xiàn)體外分化和自組裝,因此需要多種細(xì)胞因子的組合進(jìn)行誘導(dǎo),培養(yǎng)基成分復(fù)雜。而普通細(xì)胞培養(yǎng)通常為單一種類細(xì)胞,因此培養(yǎng)基成分較簡單;
Q37:用哪種培養(yǎng)基培養(yǎng)來自轉(zhuǎn)移部位腫瘤的類器官,比如原發(fā)灶為A類型腫瘤,轉(zhuǎn)移灶為B類型腫瘤?
A37:通常來講,如果腫瘤發(fā)生了轉(zhuǎn)移,我們依然選用相對(duì)應(yīng)的原發(fā)灶(A類型)PDO培養(yǎng)基。
Q38:怎樣證明培養(yǎng)出的結(jié)構(gòu)是類器官,而不是簡單聚集在一起的細(xì)胞團(tuán)?
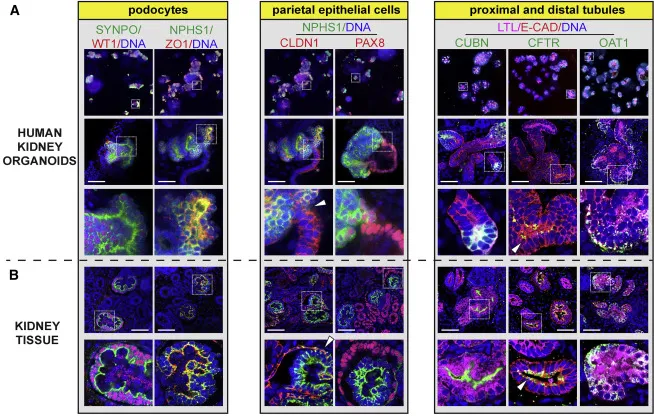
A38:類器官的分化方式本質(zhì)上是在模擬體內(nèi)的器官發(fā)育,因此表達(dá)形態(tài)及各細(xì)胞分布情況與實(shí)際器官具有相似性,而細(xì)胞團(tuán)則沒有這種規(guī)律。我們可以通過免疫熒光的方式檢測biomarkers的分布情況來區(qū)分。例如下圖中的結(jié)果表明,腎類器官與腎組織的biomarkers分布高度一致【19】。
腎類器官與腎組織的biomarkers分布高度一致【19】
Q39:類器官的的來源細(xì)胞必須要具有多能性嗎?正常組織成熟體細(xì)胞可以進(jìn)行類器官培養(yǎng)嗎?
A39:由于類器官涉及到體外分化和自組裝,因此來源細(xì)胞必須具有多能性。正常組織的成熟體細(xì)胞中往往會(huì)有一部分成體干細(xì)胞(標(biāo)志物為Lgr5,CD133等),這部分細(xì)胞也可以進(jìn)行類器官培養(yǎng)。
Q40:可以通過構(gòu)建條件性培養(yǎng)基代替商品化的細(xì)胞因子嗎?
A40:依據(jù)Hans Clevers實(shí)驗(yàn)室早期發(fā)表的文章,可以采用條件性培養(yǎng)基代替純化的細(xì)胞因子進(jìn)行類器官培養(yǎng),但同時(shí)也需要考慮條件性培養(yǎng)基的不足之處。小編總結(jié)了條件性培養(yǎng)基和近岸細(xì)胞因子的參數(shù)差異。
表1. 條件性培養(yǎng)基和近岸蛋白細(xì)胞因子的參數(shù)差異
總的來說,條件性培養(yǎng)基對(duì)于部分預(yù)實(shí)驗(yàn)或少量類器官培養(yǎng)是可行的,但鑒于質(zhì)粒構(gòu)建和驗(yàn)證消耗的時(shí)間,以及檢測過程涉及的抗體、qPCR等成本也是需要考慮在內(nèi)的。同時(shí),細(xì)胞代謝產(chǎn)物、內(nèi)毒素和宿主殘留物等也有可能影響實(shí)驗(yàn)結(jié)果。因此,選用高品質(zhì)的商品化細(xì)胞因子能夠幫您節(jié)約時(shí)間和金錢成本,快速推動(dòng)類器官培養(yǎng)進(jìn)程。
實(shí)際操作篇
類器官是能夠在體外三維培養(yǎng),并表現(xiàn)出相應(yīng)器官生物學(xué)特征的“最小系統(tǒng)”。雖然許多類器官的培養(yǎng)方案日漸成熟,但在實(shí)際操作中總會(huì)碰到這樣那樣的問題,今天小編整理了一些類器官培養(yǎng)操作中常遇到的問題,希望能夠?qū)Ω魑恍』锇橛兴鶐椭?/span>
Q41: 按照文獻(xiàn)方法進(jìn)行類器官培養(yǎng),為什么觀察到的形態(tài)卻和文獻(xiàn)不一致?
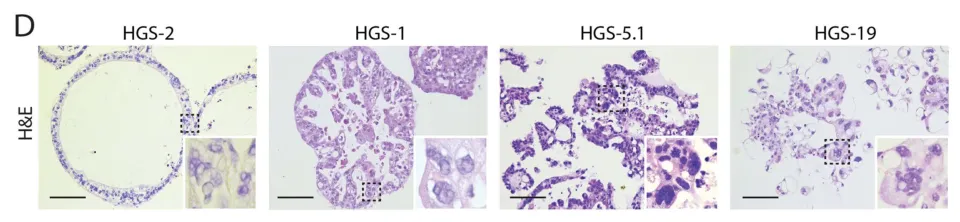
A41:決定類器官形態(tài)的因素有很多,樣本來源是否相同、選用的細(xì)胞因子品質(zhì)是否有差異都有可能改變最終的類器官形態(tài)。這里舉一個(gè)文獻(xiàn)中的例子,分別取四個(gè)高級(jí)別漿液性(HGS)卵巢癌患者的腫瘤組織,用同樣的條件進(jìn)行類器官培養(yǎng),H&E染色結(jié)果顯示它們的形態(tài)千差萬別【20】。因此對(duì)于類器官的鑒定,我們不能局限于形態(tài)觀察,需要使用多種方法相結(jié)合。
由4例HGS卵巢癌患者的腫瘤組織所制備的類器官形態(tài)不同【20】
Q42:類器官的藥敏實(shí)驗(yàn)中需要使用DMSO作為藥物的溶劑,需要控制DMSO的用量嗎?
A42:考慮到DMSO這類有機(jī)物的細(xì)胞毒性,建議終濃度不超過0.1%(v/v)。
Q43:培養(yǎng)過程中發(fā)現(xiàn)類器官培養(yǎng)物中有黑色小顆粒,這個(gè)是雜質(zhì)嗎?應(yīng)該怎樣去除?
A43:黑色小顆粒大概率是雜質(zhì)或細(xì)胞碎片,去除它們有以下兩種方式可以參考:
1、將類器官消化下來,用培養(yǎng)基進(jìn)行反復(fù)清洗,達(dá)到稀釋雜質(zhì)的作用;
2、用無菌手術(shù)刀將類器官切成兩半,取1ml注射器吸滿培養(yǎng)基并輕輕推出,沖洗類器官中的雜質(zhì)【21】。
Q44:對(duì)于腫瘤患者的個(gè)性化醫(yī)療測試,PDO、PDX、PDXO的模型可以相互結(jié)合使用嗎?
A44:PDO、PDX、PDXO模型有各自的優(yōu)勢,通常有以下兩種結(jié)合方式:PDO-PDX和PDX-PDXO。
1、PDO-PDX是性價(jià)比更高的方式,即:先利用PDO進(jìn)行高通量的藥物篩選,篩選出有效的藥物再進(jìn)行PDX測試。
2、PDX-PDXO是更精準(zhǔn)的藥物測試方式,即:先利用PDX產(chǎn)生大量的體內(nèi)腫瘤,然后將這些腫瘤分離進(jìn)行PDXO培養(yǎng),此時(shí)可以通過PDX模型,將PDXO的藥敏實(shí)驗(yàn)結(jié)果與體內(nèi)用藥結(jié)果一一對(duì)應(yīng),進(jìn)而預(yù)測人體用藥的結(jié)果,實(shí)現(xiàn)對(duì)患者更精準(zhǔn)的用藥指導(dǎo);并且可以用PDX模型將轉(zhuǎn)移后的腫瘤分離,同樣進(jìn)行PDXO培養(yǎng)和用藥,能夠更精確地對(duì)轉(zhuǎn)移灶進(jìn)行藥物篩選。
Q45:類器官怎么從基質(zhì)膠中回收?
A45:1、將類器官放置在冰上,待基質(zhì)膠融化后離心進(jìn)行回收,這種方式適用于不需要將類器官結(jié)構(gòu)完全打散的情況;
2、市售的細(xì)胞回收液,可以溫和有效地獲得細(xì)胞懸液,不會(huì)損傷細(xì)胞或細(xì)胞表面蛋白。
Q46:為什么用基質(zhì)膠來培養(yǎng)類器官?可以用其它類型的凝膠替代嗎?
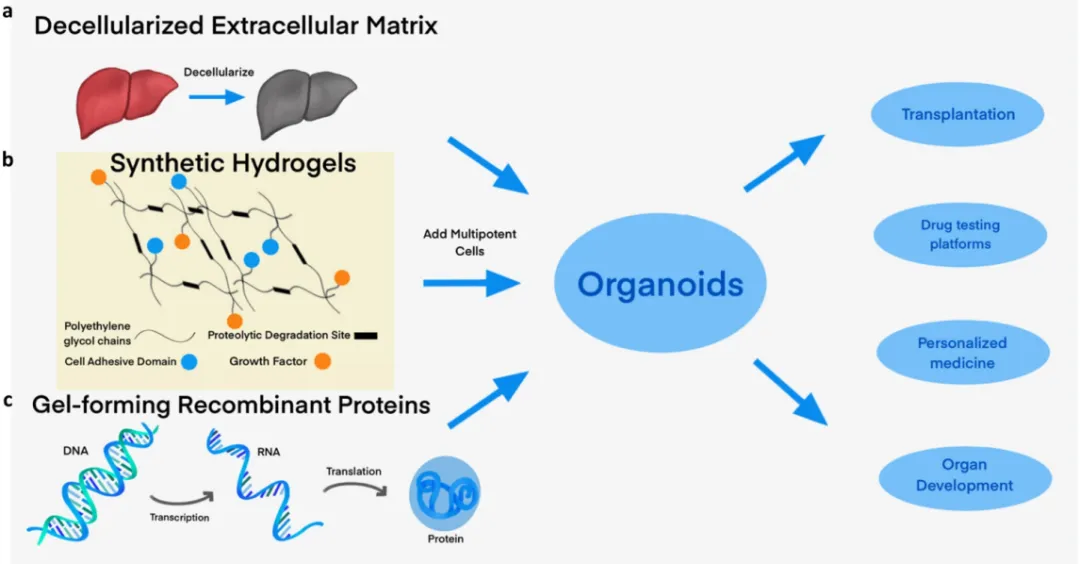
A46:基質(zhì)膠能夠?yàn)轭惼鞴偬峁┲巫饔茫壳邦惼鞴倥囵B(yǎng)用的基質(zhì)膠來源于小鼠肉瘤的基底膜基質(zhì),其中含有約60%層粘連蛋白、30% IV 膠原和8%的巢蛋白,還含有基底膜聚糖、TGF-ß、表皮生長因子、類胰島素生長因子、組織纖溶酶原等1800多種獨(dú)特的蛋白質(zhì)。由于基質(zhì)膠中各因子的不確定性,并且存在批次間差異,因此目前也有一些聚焦于基質(zhì)膠替代方案的研究,見下圖【22】。
基質(zhì)膠的三種替代方案【22】。(a)去細(xì)胞外基質(zhì)和其他衍生蛋白質(zhì),(b)合成水凝膠,以及(c)工程重組蛋白凝膠
Q47:怎樣確定某一種類器官的培養(yǎng)方式更適用于基質(zhì)膠包埋法還是氣-液交互法呢?
A47:1、根據(jù)所模擬的器官自身生長情況選擇,例如:皮膚的正常生長是有一面需要接觸空氣,那么對(duì)于皮膚類器官的培養(yǎng)傾向于利用氣-液交互法來培養(yǎng)【23】;
2、考慮所培養(yǎng)的類器官模型的應(yīng)用方向,例如:氣-液交互法培養(yǎng)易于進(jìn)行病毒感染實(shí)驗(yàn),因此用于病毒感染實(shí)驗(yàn)的氣道類器官會(huì)優(yōu)先選擇氣-液交互法培養(yǎng)【24】。
Q48:在進(jìn)行藥敏實(shí)驗(yàn)前,類器官的接種方式是怎樣的呢?
A48:藥物篩選前,通常將類器官吹散后,用含2%-5%基質(zhì)膠的培養(yǎng)基懸浮,并最終鋪在基質(zhì)膠包被的孔板中【25-26】。
Q49:在離心回收時(shí),會(huì)有很多類器官粘附在離心管壁,有沒有更好的辦法提高回收率?
A49:建議采用水平轉(zhuǎn)子代替角轉(zhuǎn)子,可以有效減少類器官掛在離心管壁的情況。
Q50:利用腫瘤類器官模型進(jìn)行篩選的藥物有什么局限性嗎?
A50:1、抗體藥物因?yàn)樾枰庖呒?xì)胞的參與,因此腫瘤類器官不能篩選抗體類藥物,此類藥物篩選需要構(gòu)建腫瘤類器官-腫瘤微環(huán)境的模型來實(shí)現(xiàn);
2、由于腫瘤類器官中沒有對(duì)血管進(jìn)行培養(yǎng),因此抗血管類的藥物也同樣不能進(jìn)行篩選。
近岸蛋白依靠專業(yè)的研發(fā)團(tuán)隊(duì),精心打造類器官驗(yàn)證平臺(tái),可提供一系列經(jīng)驗(yàn)證、高活性、可信任的類器官培養(yǎng)產(chǎn)品,包括經(jīng)類器官培養(yǎng)驗(yàn)證的細(xì)胞因子及類器官培養(yǎng)基,助您類器官實(shí)驗(yàn)省心高效!
推薦產(chǎn)品
類器官培養(yǎng)基
參考文獻(xiàn):
【1】He, A. et al. (2020). Cryopreservation of viable human tissues: Renewable resource for viable tissue, cell lines, and organoid development. Biopreservation and Biobanking, 18(3), 222-227.
【2】Lancaster, M. A. et al. (2013). Cerebral organoids model human brain development and microcephaly. Nature, 501(7467), 373-379.
【3】Sheridan, M. A. et al. (2020). Establishment and differentiation of long-term trophoblast organoid cultures from the human placenta. Nature Protocols, 15(10), 3441-3463.
【4】Beshiri, M. L. et al.(2018). A PDX/organoid biobank of advanced prostate cancers captures genomic and phenotypic heterogeneity for disease modeling and therapeutic screening. Clinical Cancer Research, 24(17), 4332-4345.
【5】McCracken, K. W. et al. (2014). Modelling human development and disease in pluripotent stem-cell-derived gastric organoids. Nature, 516(7531), 400-404
【6】Vlachogiannis, G. et al.(2018). Patient-derived organoids model treatment response of metastatic gastrointestinal cancers. Science, 359(6378), 920-926.
【7】Chen, X. et al.(2021). Phenotype transition of fibroblasts incorporated into patient‐derived oral carcinoma organoids. Oral Diseases.
【8】Ooft, S. N. et al.(2019). Patient-derived organoids can predict response to chemotherapy in metastatic colorectal cancer patients. Science translational medicine, 11(513), eaay2574.
【9】Mullins, C. S. et al. (2013). Establishment and characterization of primary glioblastoma cell lines from fresh and frozen material: a detailed comparison. PloS one, 8(8), e71070.
【10】Vogel, T. W. et al.(2005). Proteins and protein pattern differences between glioma cell lines and glioblastoma multiforme. Clinical cancer research, 11(10), 3624-3632.
【11】Wallaschek N. et al. Establishing pure cancer organoid cultures: identification, selection and verification of cancer phenotypes and genotypes[J]. Journal of molecular biology, 2019, 431(15): 2884-2893.
【12】HERPERS, Bram, et al. Functional patient-derived organoid screenings identify MCLA-158 as a therapeutic EGFR× LGR5 bispecific antibody with efficacy in epithelial tumors. Nature Cancer, 2022, 1-19.
【13】Jiang, Shengwei, et al.. (2020). An automated organoid platform with inter-organoid homogeneity and inter-patient heterogeneity. Cell Reports Medicine, 1(9), 100161.
【14】WATANABE, Satoshi, et al. Transplantation of intestinal organoids into a mouse model of colitis. Nature Protocols, 2022, 1-25.
【15】Wang, D. et al. (2020). Long-term expansion of pancreatic islet organoids from resident Procr+ progenitors. Cell, 180(6), 1198-1211.
【16】Sampaziotis, F. et al. (2021). Cholangiocyte organoids can repair bile ducts after transplantation in the human liver. Science, 371(6531), 839-846.
【17】Driehuis, E., Kretzschmar, K., & Clevers, H. (2020). Establishment of patient-derived cancer organoids for drug-screening applications. Nature protocols, 15(10), 3380-3409.
【18】Hendriks, D., Clevers, H., & Artegiani, B. (2020). CRISPR-Cas tools and their application in genetic engineering of human stem cells and organoids. Cell Stem Cell, 27(5), 705-731.
【19】Czerniecki, S. M. et al. (2018). High-throughput screening enhances kidney organoid differentiation from human pluripotent stem cells and enables automated multidimensional phenotyping. Cell stem cell, 22(6), 929-940.
【20】Kopper, O. et al. (2019). An organoid platform for ovarian cancer captures intra-and interpatient heterogeneity. Nature medicine, 25(5), 838-849.
【21】MILLER, Alyssa J., et al. Generation of lung organoids from human pluripotent stem cells in vitro. Nature protocols, 2019, 14.2: 518-540.
【22】Kozlowski, M. T. et al. (2021). Towards organoid culture without Matrigel. Communications biology, 4(1), 1-15.
【23】Gangatirkar, P. et al. (2007). Establishment of 3D organotypic cultures using human neonatal epidermal cells. Nature protocols, 2(1), 178-186.
【24】Mulay, A. et al. (2021). SARS-CoV-2 infection of primary human lung epithelium for COVID-19 modeling and drug discovery. Cell reports, 35(5), 109055.
【25】Van de Wetering, M. et al. (2015). Prospective derivation of a living organoid biobank of colorectal cancer patients. Cell, 161(4), 933-945.
【26】Hirt, C. K. et al. (2022). Drug screening and genome editing in human pancreatic cancer organoids identifies drug-gene interactions and candidates for off-label therapy. Cell genomics, 2(2), 100095.