隨著臨床醫(yī)學(xué)和檢驗醫(yī)學(xué)的不斷發(fā)展,實驗室自建檢測方法(包括自制試劑等)流程與管理規(guī)范化成為醫(yī)療機構(gòu)的迫切需求。北京醫(yī)學(xué)會檢驗醫(yī)學(xué)分會、上海市醫(yī)學(xué)會檢驗醫(yī)學(xué)專科分會組織京滬兩地檢驗醫(yī)學(xué)專家形成共識小組,就LDT全流程管理的10個方面形成30條共識。該共識基于自建檢測的質(zhì)量、風(fēng)險、性能三方面核心關(guān)鍵要素,圍繞術(shù)語、研發(fā)與產(chǎn)品準(zhǔn)備、檢驗流程、登記備案、督查、檢驗前中后環(huán)節(jié)、轉(zhuǎn)化應(yīng)用與推廣等內(nèi)容給出了共識性建議,以期為醫(yī)療機構(gòu)開展相應(yīng)工作提供參考。

LDT試劑為國內(nèi)尚無同品種產(chǎn)品上市的體外診斷試劑。與已取得醫(yī)療器械注冊證的體外診斷試劑相比,其技術(shù)原理、預(yù)期用途方面存在實質(zhì)性差異,或臨床性能獲得根本性改進,可明顯提高臨床診斷能力,或具有新的臨床診斷應(yīng)用價值。開展LDT的機構(gòu),可重點關(guān)注國家相關(guān)文件中提及的試點項目,如腫瘤精準(zhǔn)診療、治療藥物監(jiān)測、代謝物質(zhì)譜分析、病原微生物檢測、遺傳代謝病診療等。
該專家共識對于醫(yī)療機構(gòu)臨床實驗室自建檢測方法流程中的質(zhì)量控制也尤為重視。其中:
第三章——檢驗要素(試劑、耗材)制備
共識7:醫(yī)療機構(gòu)可自行制備檢驗試劑或耗材,也可在研發(fā)定型后委托具有醫(yī)療器械生產(chǎn)許可證且生產(chǎn)范圍包括第二類或第三類體外診斷試劑的企業(yè)完成制備。受委托企業(yè)獲批的產(chǎn)品類目需與LDT一致。
共識8:應(yīng)根據(jù)原材料對產(chǎn)品性能、安全等的影響程度,明確關(guān)鍵物質(zhì)原料及其質(zhì)量標(biāo)準(zhǔn),并進行檢驗或驗證,以確保滿足試劑制備要求。
共識9:醫(yī)療機構(gòu)應(yīng)對試劑和耗材制備進行管理,自行制備時需負全責(zé),委托制備時需按合同規(guī)定,確保產(chǎn)品質(zhì)量合格;制備過程需有記錄、可回溯;制備環(huán)節(jié)具備相應(yīng)的質(zhì)控參數(shù),形成記錄并隨產(chǎn)品交接;制備的產(chǎn)品標(biāo)識清晰、內(nèi)容完整,并有必要的應(yīng)用、安全等提示;制備后的交接過程有記錄和反饋機制。委托制備時,應(yīng)在合同中規(guī)定雙方人員職責(zé),并按不低于同類產(chǎn)品的質(zhì)量要求明確規(guī)定質(zhì)量標(biāo)準(zhǔn)。
共識10:關(guān)注標(biāo)準(zhǔn)品、校準(zhǔn)品、質(zhì)控品、參考品等的制備。制定不同級別相應(yīng)產(chǎn)品的量值溯源程序,建立制備和交接記錄。
標(biāo)準(zhǔn)品、校準(zhǔn)品、質(zhì)控品、參考品是確定LDT質(zhì)量(精密度、準(zhǔn)確度)的關(guān)鍵,無成熟可用產(chǎn)品時,LDT必須進行針對以上物質(zhì)的研制和配備[15]。記錄其來源、批號、效期、溯源途徑、主要技術(shù)指標(biāo)、保存狀態(tài)等信息,按照規(guī)定對其進行復(fù)驗并保存記錄,并評估其準(zhǔn)確度和穩(wěn)定性。
第四章——檢驗流程
共識15:檢驗流程建立后,應(yīng)對LDT性能、配套產(chǎn)品性能等進行研究和評價,至少包括分析性能、穩(wěn)定性、陰性和陽性判斷值、質(zhì)量控制程序、參考區(qū)間等。評價頻率:分別評價前3個批號配套產(chǎn)品的性能,如均符合預(yù)期,可改為年度評價;如不符合預(yù)期,則不能啟動LDT應(yīng)用。
第八章——臨床檢測:檢驗中
共識25:行政管理機構(gòu)審核同意LDT的通知或證書,需放置于實驗室,隨時備查。實驗室應(yīng)對LDT使用說明書中規(guī)定的程序落實為文件,并在開展LDT臨床應(yīng)用前進行性能確認,評估LDT項目被測量值的測量不確定度、規(guī)定生物參考區(qū)間或臨床決定限、并建立質(zhì)量保證程序(至少包括室內(nèi)質(zhì)量控制、正確性驗證、比對等),以保證檢驗結(jié)果的有效性。
第十章——醫(yī)療機構(gòu)內(nèi)部管理要求
共識29:開展LDT的醫(yī)療機構(gòu)應(yīng)設(shè)置內(nèi)部管理機構(gòu),建立與LDT相適應(yīng)的質(zhì)量管理體系,建立風(fēng)險管理制度和不良事件監(jiān)測處理機制,配備相應(yīng)信息管理系統(tǒng)。LDT應(yīng)用中,及時發(fā)現(xiàn)設(shè)計環(huán)節(jié)生產(chǎn)環(huán)節(jié)和檢驗全流程可能存在的問題,并及時反饋和優(yōu)化。對嚴重問題導(dǎo)致的結(jié)果精密度、準(zhǔn)確度出現(xiàn)偏差,暫停LDT的應(yīng)用。
相關(guān)原文附件請點擊: 醫(yī)療機構(gòu)臨床實驗室自建檢測方法流程與管理專家共識.pdf
醫(yī)療機構(gòu)臨床實驗室自建檢測方法流程與管理專家共識.pdf
菁良技術(shù)優(yōu)勢
![]() 產(chǎn)品形式豐富
產(chǎn)品形式豐富
菁良可提供gDNA、ctDNA、FFPE (DNA/RNA)、假病毒 (溶液/凍干珠)、細胞溶液、RNA干粉等不同形式的產(chǎn)品。
![]() 自有細胞庫
自有細胞庫
累積近千細胞系資源: 涵蓋腫瘤、生殖、遺傳等多個方向。
![]() 多項創(chuàng)新產(chǎn)品
多項創(chuàng)新產(chǎn)品
自主創(chuàng)新研發(fā)的NIPT、HRD、TMB、COVID-19凍干珠質(zhì)控品等;以及包含數(shù)百種突變位點,監(jiān)控范圍超廣的泛腫瘤 800 gDNA標(biāo)準(zhǔn)品等。
![]() 定制化產(chǎn)品和服務(wù)
定制化產(chǎn)品和服務(wù)
根據(jù)用戶需求進行個性化定制:可定制多種產(chǎn)品形式;可定制突變位點組合及突變頻率。
![]() 全面的質(zhì)控體系
全面的質(zhì)控體系
400+實驗生產(chǎn)SOP,ISO13485質(zhì)量體系保障;數(shù)字PCR質(zhì)檢及NGS多平臺協(xié)同檢測定標(biāo)。
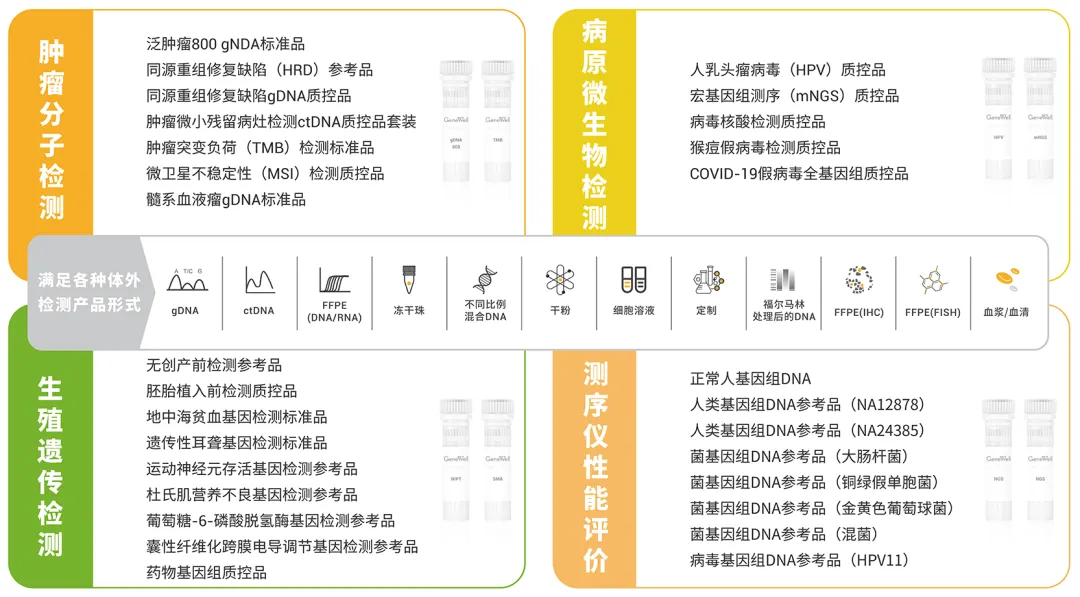
分子質(zhì)控品——覆蓋多種疾病類型
關(guān)于菁良
菁良科技(深圳)有限公司是全球領(lǐng)先的提供體外檢測標(biāo)準(zhǔn)品的研發(fā)創(chuàng)新型高科技企業(yè)。
體外檢測需要標(biāo)準(zhǔn)品!隨著經(jīng)濟的快速發(fā)展,科技細分領(lǐng)域的不斷拓展,國民生活水平的不斷提高,檢驗檢測市場需求也隨之快速上升,體外檢測進入高速發(fā)展階段。然而配套的質(zhì)量控制和規(guī)范化意識卻相對滯后,很大一部分體外檢測方法仍然存在效率低下且檢測準(zhǔn)確率有限的情況。菁良通過自主研發(fā)的高科技平臺,向體外檢測行業(yè)用戶及合作伙伴提供全球領(lǐng)先的標(biāo)準(zhǔn)物質(zhì)、第三方質(zhì)控產(chǎn)品和研發(fā)參考品服務(wù),助力提高行業(yè)檢測準(zhǔn)確率!
菁良自2018年成立以來,始終以推動行業(yè)規(guī)范化、標(biāo)準(zhǔn)化為己任,參與多項由檢測領(lǐng)域行業(yè)龍頭發(fā)起的標(biāo)準(zhǔn)制定工作,多次支持由臨檢中心發(fā)起的室間質(zhì)量評價 (EQA)/能力驗證項目。菁良擁有全球領(lǐng)先的標(biāo)準(zhǔn)品研發(fā)技術(shù)和資深的國際拓展經(jīng)驗,已推出眾多行業(yè)首創(chuàng)的參考品和第三方質(zhì)控品,被廣泛用于檢測試劑和儀器的工藝開發(fā)、以及檢測過程之中。菁良秉承著“菁準(zhǔn)制標(biāo),匠心良造”的理念,懷抱著“提高體外檢測準(zhǔn)確率,助力精準(zhǔn)醫(yī)學(xué)快速發(fā)展”的愿景,致力于建立規(guī)范化的中國體外檢測金標(biāo)準(zhǔn)平臺。
