?
?
精神分裂癥(Schizophrenia)是一種復(fù)雜而嚴(yán)重的精神疾患,其特征是感知現(xiàn)實(shí)的方式受到嚴(yán)重?fù)p害,出現(xiàn)持續(xù)性妄想、幻想、思維混亂及行為異常等,影響到全球約2400萬人。精神分裂癥患者病理變化包括少突膠質(zhì)細(xì)胞分化受損、髓鞘和白質(zhì)丟失等。
精神分裂癥斷裂基因1(Disrupted-in-schizophrenia-1, DISC1)被認(rèn)為是精神分裂癥發(fā)病的主要易感基因之一,研究發(fā)現(xiàn),DISC1功能障礙參與影響少突膠質(zhì)細(xì)胞前體細(xì)胞(oligodendrocyte precursor cells, OPCs)的成熟和髓鞘的形成。此外,DISC1的部分致病單核苷酸突變將導(dǎo)致DISC1的可變剪切增加,其中DISC1-Δ3(缺少外顯子3的剪切體)在精神分裂癥患者中顯著升高,但其致病機(jī)制仍不清楚。
?
2022年9月21日,陸軍軍醫(yī)大學(xué)牛建欽教授團(tuán)隊(duì)聯(lián)合肖嵐教授團(tuán)隊(duì)、曼切斯特大學(xué)Alexei Verkhratsky教授團(tuán)隊(duì)合作在Molecular Psychiatry上發(fā)表了題為“Pathological oligodendrocyte precursor cells revealed in human schizophrenic brains and trigger schizophrenia-like behaviors and synaptic defects in genetic animal model”的研究論文,揭示了OPCs中DISC1-Δ3表達(dá)通過調(diào)控Wnt/β-catenin信號(hào)通路異常激活與其下游Wif1高表達(dá),參與精神分裂癥發(fā)病機(jī)制。該研究找到一個(gè)臨床干預(yù)精神分裂癥的分子靶點(diǎn)—Wif1,并提供了強(qiáng)有力的實(shí)驗(yàn)依據(jù)。
?

?
結(jié)果
?
精神分裂癥患者OPCs形態(tài)異常
首先,研究人員基于臨床樣本率先發(fā)現(xiàn),精神分裂癥(Schizophrenia)患者海馬、前額葉皮層和杏仁核中被NG2標(biāo)記的少突膠質(zhì)細(xì)胞前體細(xì)胞(oligodendrocyte precursor cells, OPCs)的數(shù)量無明顯變化,而形態(tài)發(fā)生改變,表現(xiàn)為更為復(fù)雜的肥大形態(tài)(圖1)。
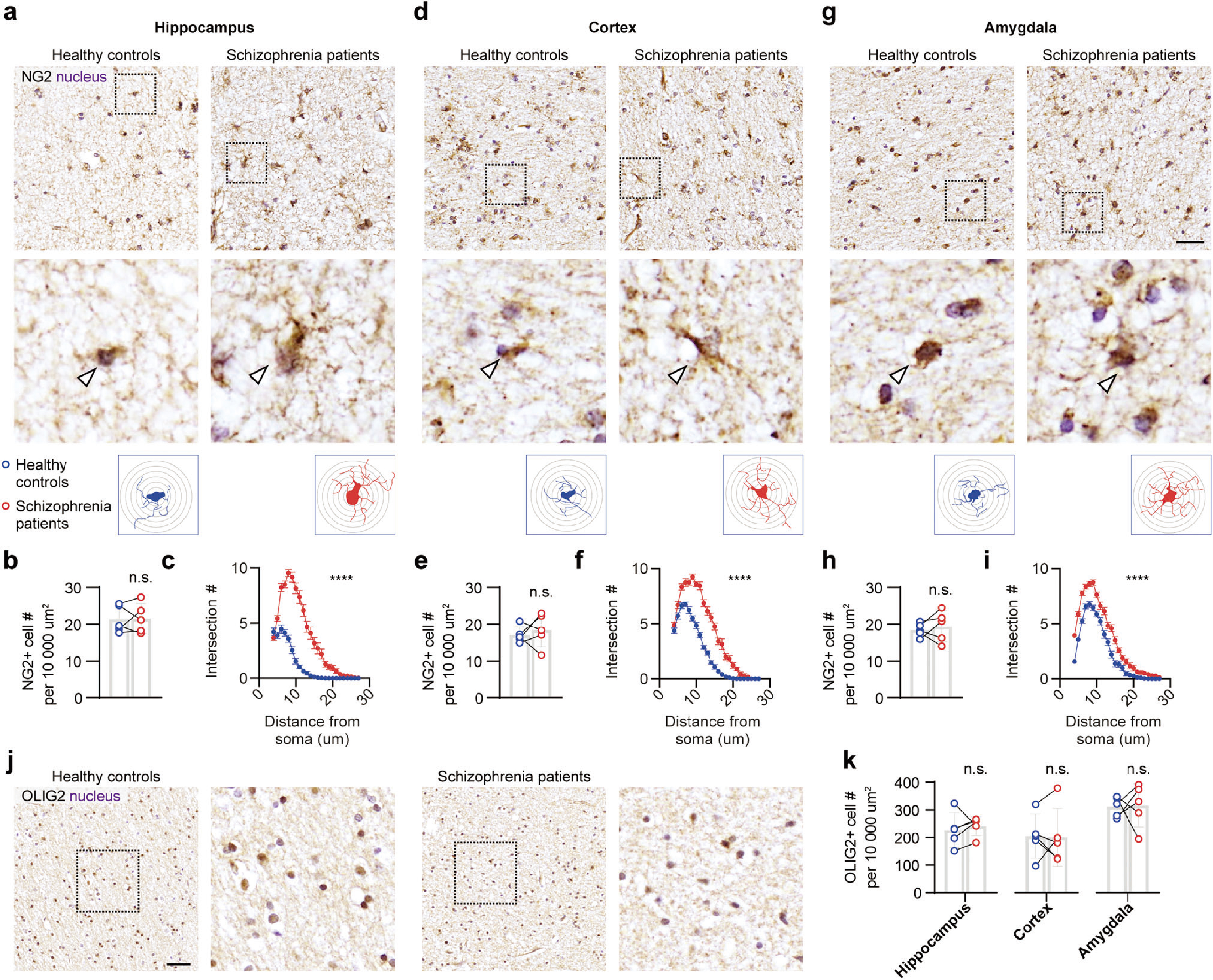
圖1精神分裂癥患者OPCs形態(tài)異常
?
DISC1-Δ3鼠模擬精神分裂癥樣表型
DISC1作為精神分裂癥發(fā)病的主要易感基因之一,參與調(diào)節(jié)少突膠質(zhì)細(xì)胞的發(fā)育,RNA測(cè)序結(jié)果顯示,DISC1在人和小鼠OPCs的表達(dá)遠(yuǎn)高于少突膠質(zhì)細(xì)胞和神經(jīng)元。此外,對(duì)DISC1剪切體分析發(fā)現(xiàn),DISC1-Δ3(缺少外顯子3的剪切體)在精神分裂癥患者腦中表達(dá)顯著升高。 基于此,研究者構(gòu)建NG2CreERT:DISC1exon3 fl/+小鼠(簡(jiǎn)稱DISC1-Δ3鼠,由DISC1exon3 flox鼠與NG2CreERT鼠雜交獲得,其特點(diǎn)為在不影響DISC1全基因表達(dá)情況下,經(jīng)他莫昔芬誘導(dǎo)可特異性在OPCs中上調(diào)DISC1-Δ3的表達(dá)),發(fā)現(xiàn)OPCs中特異性過表達(dá)DISC1-Δ3同樣導(dǎo)致OPCs過度肥大,并伴隨著髓鞘形成減少(圖2a-f),這與精神分裂癥患者腦內(nèi)OPCs形態(tài)類似(圖1)。此外,行為水平上 ,出生后25-36(P25-P36)DISC1-Δ3鼠表現(xiàn)出精神分裂癥樣的感覺運(yùn)動(dòng)門控障礙(圖2g-k)。同時(shí),研究者發(fā)現(xiàn)DISC1-Δ3鼠海馬CA1區(qū)興奮性突觸減少,且少突膠質(zhì)細(xì)胞中DISC1-Δ3表達(dá)上調(diào)降低了自發(fā)興奮性突觸后電流(sEPSC)頻率,增強(qiáng)了自發(fā)抑制性突觸后電流(sIPSC)頻率(圖2l-p)。
?
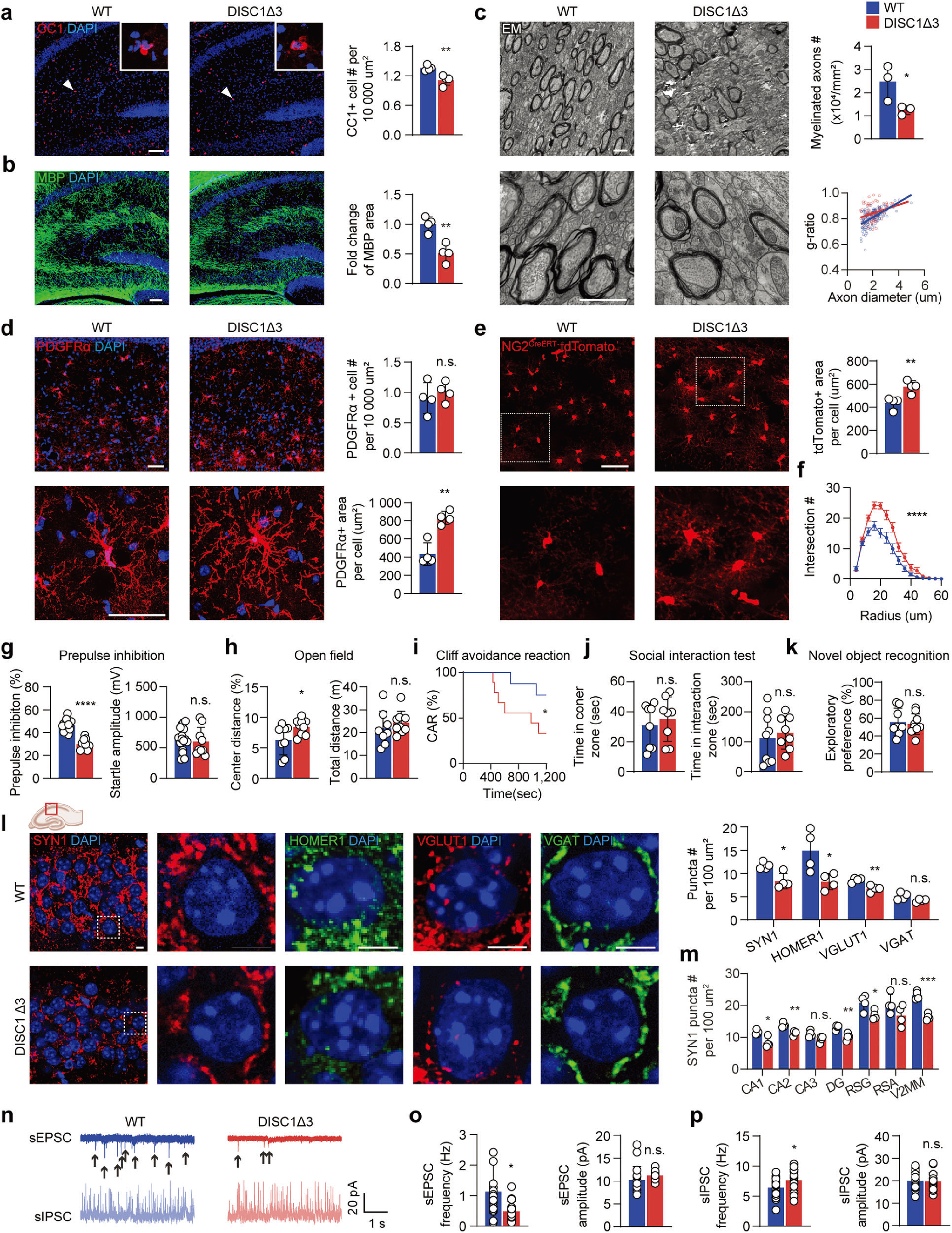
圖2 DISC1-Δ3模型鼠模擬精神分裂癥樣表型
?
?
DISC1-Δ3模型鼠中OPCs異常參與突觸形成缺陷及精神分裂癥
隨后,研究者分析了過度肥大的OPCs與精神分裂癥患者髓鞘丟失的關(guān)系,通過他莫昔芬誘導(dǎo)DISC1-Δ3鼠在不同周齡發(fā)生OPCs中DISC1外顯子3缺失,發(fā)現(xiàn)OPCs中DISC1外顯子3缺失足以誘導(dǎo)突觸功能障礙和精神分裂癥樣行為(圖3a-f)。 接下來,研究者構(gòu)建OL- DISC1-Δ3鼠(特異性在成熟少突膠質(zhì)細(xì)胞中增強(qiáng)DISC1-Δ3表達(dá))作進(jìn)一步驗(yàn)證,發(fā)現(xiàn)特異性在P21小鼠海馬OLs中增強(qiáng)DISC1-Δ3表達(dá)并未引起類似精神分裂癥的病理變化(圖3g-j)。同時(shí),體外實(shí)驗(yàn)也驗(yàn)證了DISC1-Δ3 OPCs對(duì)神經(jīng)元的直接影響(圖3k-m)。 這些結(jié)果提示了,證明DISC1-Δ3小鼠中的突觸形成缺陷與精神分裂癥樣表型是OPC本身的異常導(dǎo)致,而非髓鞘形成缺陷介導(dǎo)。
?
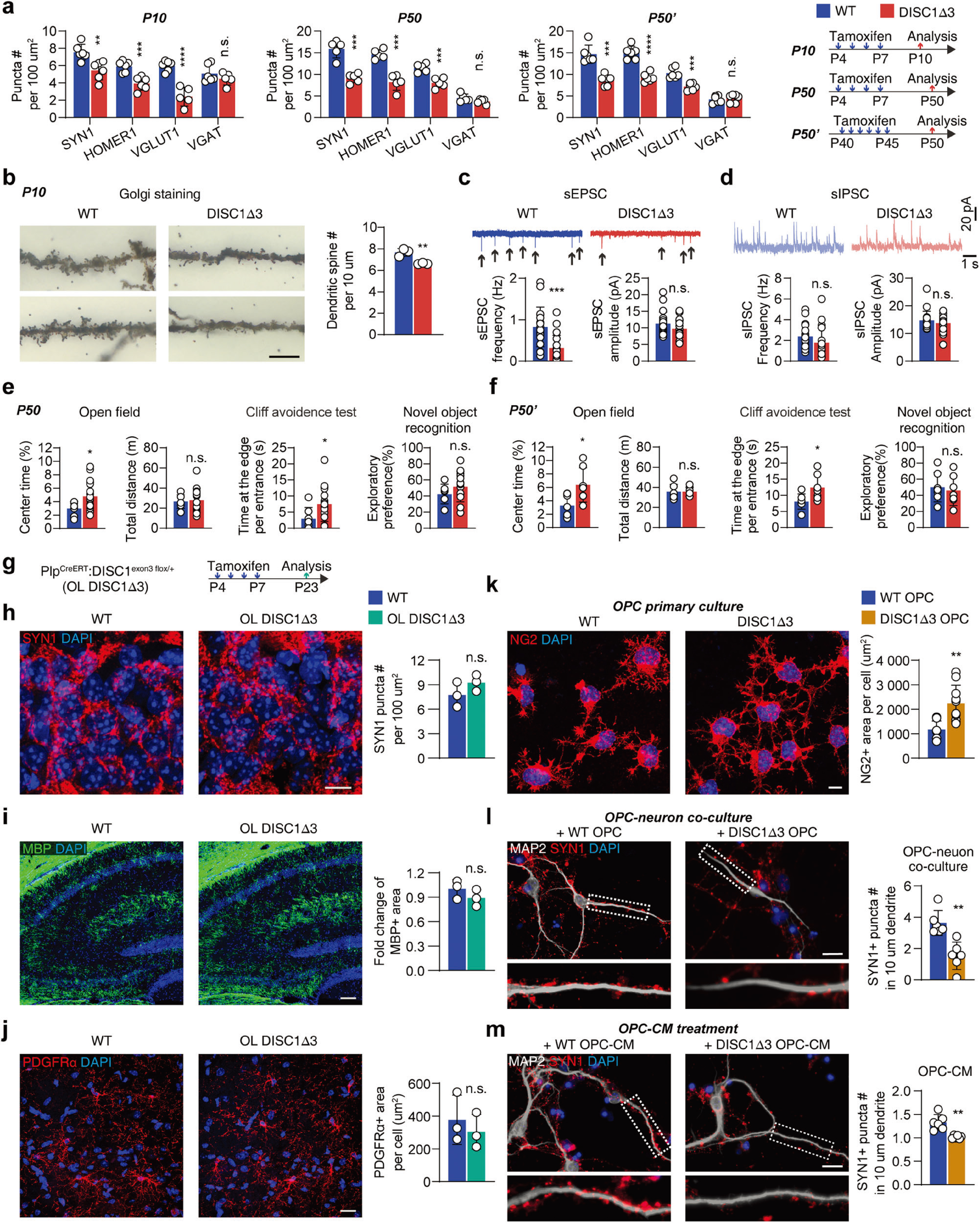
圖3 DISC1-Δ3小鼠中的突觸形成缺陷與精神分裂癥樣表型是OPC本身的異常導(dǎo)致,而非髓鞘形成缺陷介導(dǎo)
?
?
OPCs參與DISC1-Δ3模型鼠精神分裂癥發(fā)生的分子機(jī)制
為驗(yàn)證其分子機(jī)制,研究者對(duì)急性分離的OPC進(jìn)行RNA測(cè)序,發(fā)現(xiàn)在DISC1-Δ3 OPCs中Wnt/β-catenin信號(hào)通路過度激活(圖4a,b),這是由于DISC1-Δ3通過Girdin-Akt通路間接抑制GSK3β活性,進(jìn)而導(dǎo)致Wnt/β-catenin信號(hào)通路增加(圖4a-d)。此外,基于臨床樣本,研究者發(fā)現(xiàn)精神分裂癥患者海馬區(qū)OPCs Wnt下游基因RNF43表達(dá)顯著上調(diào),這也印證了精神分裂癥中少突膠質(zhì)細(xì)胞前體細(xì)胞Wnt/β-catenin信號(hào)通路異常激活(圖4e)。 接下來,研究者借助RNA-seq差異表達(dá)分析及分子生物學(xué)技術(shù),在精神分裂癥患者和DISC1-Δ3小鼠海馬組織中發(fā)現(xiàn)Wif1表達(dá)顯著增加(圖4f-j)。并借助體外實(shí)驗(yàn)發(fā)現(xiàn),Wnt/β-catenin過度激活的OPC通過Wif1抑制神經(jīng)元中非經(jīng)典Wnt通路,干擾突觸形成(圖4k,l)。
?
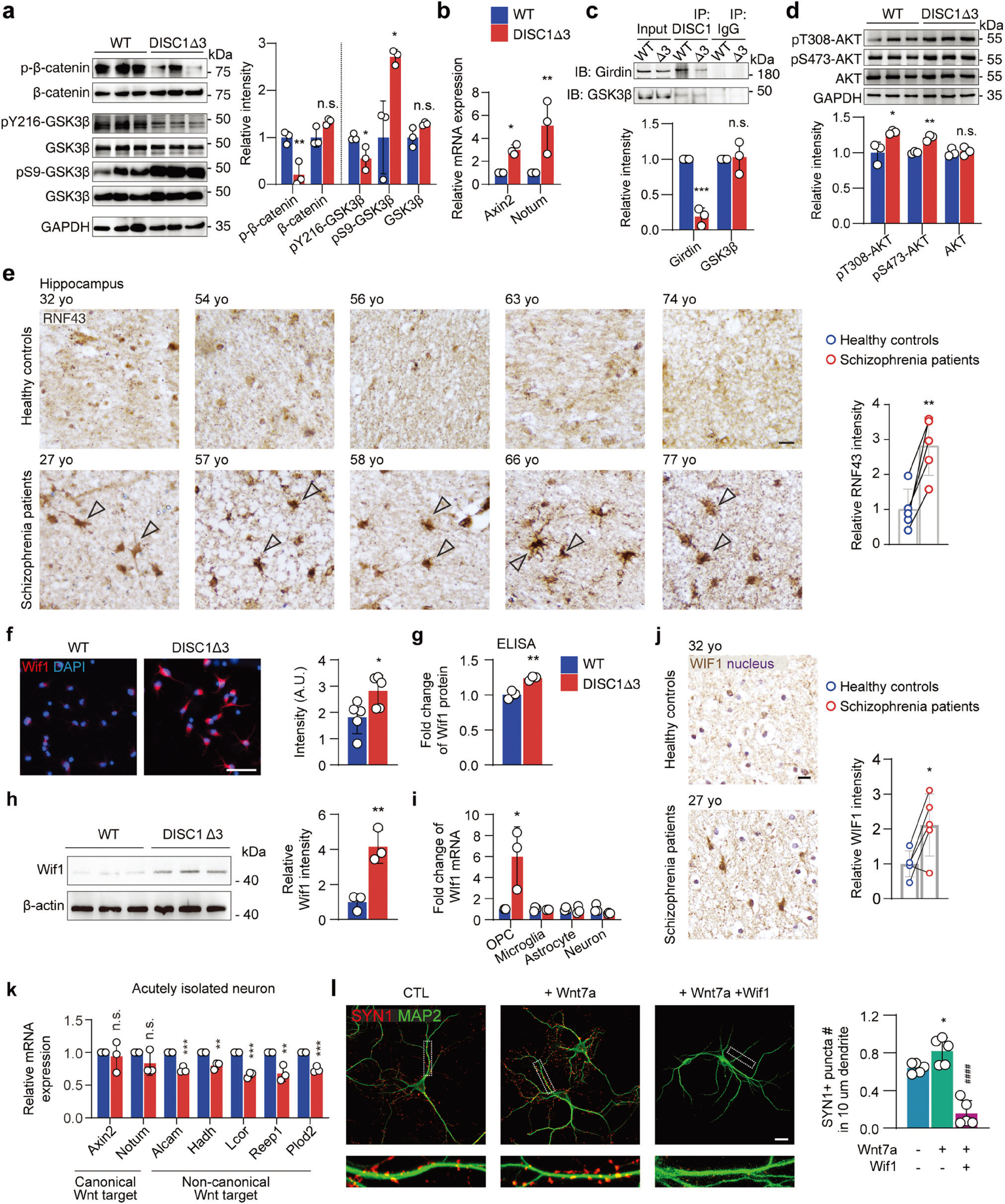
圖4 DISC1-Δ3 OPCs中異常的Wnt/β-catenin異常激活
?
最后,研究者向P10 DISC1-Δ3鼠海馬CA1注射逆轉(zhuǎn)錄病毒載體(特異性感染分裂期細(xì)胞)攜帶Wif1 shRNA(ROV-U6-shRNA(Wif1)-EF1A(S)-EGFP-3Flag)以特異性下調(diào)少突膠質(zhì)細(xì)胞前體細(xì)胞中Wif1表達(dá),發(fā)現(xiàn)增加了突觸發(fā)生(圖5a,b)。同樣地,特異性敲除DISC1-Δ3鼠OPCs中Wif1,亦增強(qiáng)了海馬興奮性突觸形成,并改善了精神分裂癥樣相關(guān)行為缺陷(圖6c-i)。這些結(jié)果提示了,DISC1-Δ3鼠OPCs中Wnt信號(hào)通路異常激活通過調(diào)控Wnt抑制劑—Wif1表達(dá)量異常增加從而破壞突觸形成,并啟動(dòng)精神分裂癥的發(fā)病機(jī)制,下調(diào)OPCs中Wif1的表達(dá)可恢復(fù)DISC1-Δ3鼠突觸形成,改善神經(jīng)功能。
?
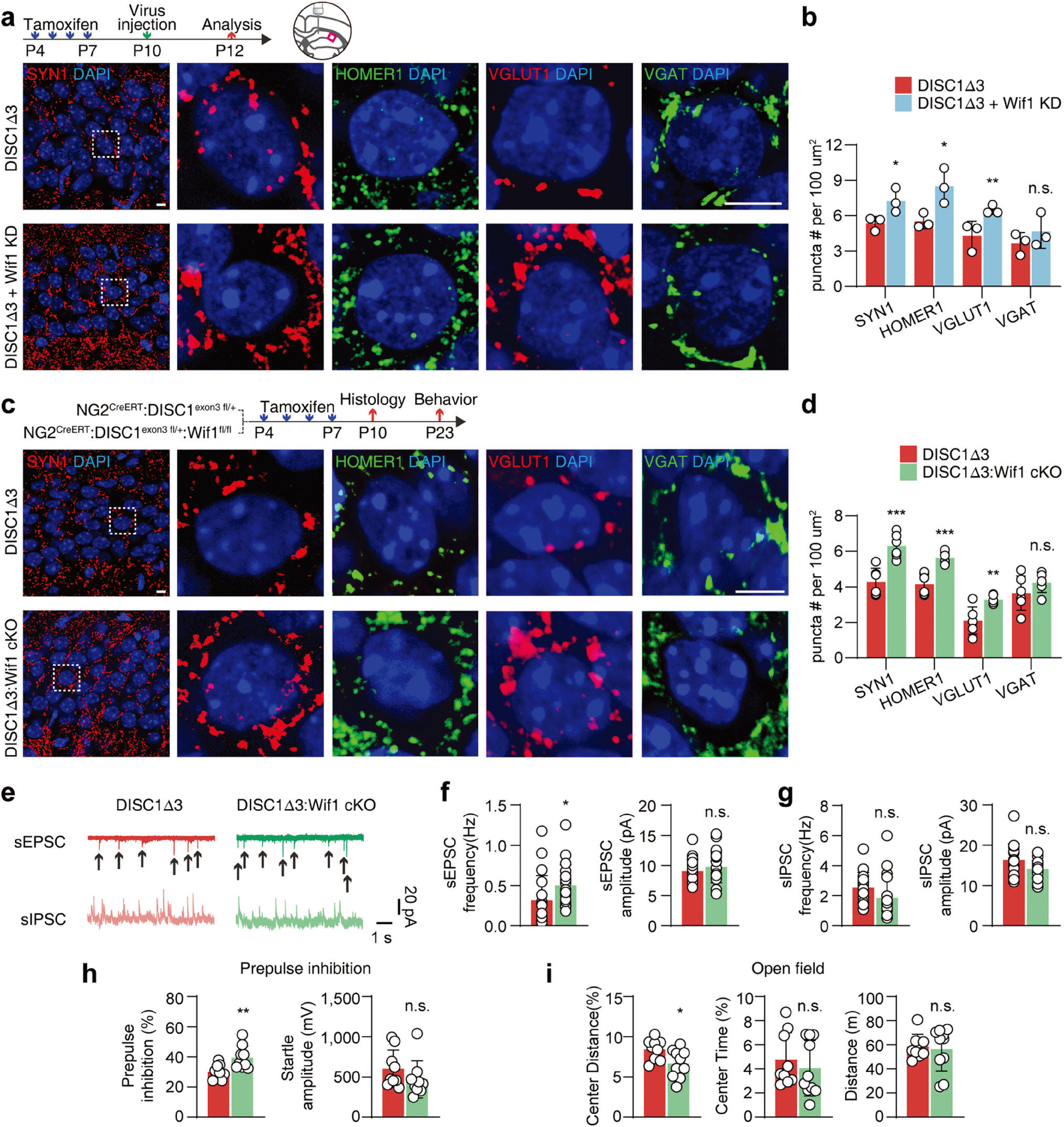
圖5 下調(diào)OPCs中Wif1的表達(dá)可改善DISC1-Δ3鼠突觸形成缺陷和行為障礙
?
?
結(jié)論
本文基于臨床樣本率先發(fā)現(xiàn)精神分裂癥患者少突膠質(zhì)細(xì)胞前體細(xì)胞(OPCs)形態(tài)異常,推測(cè)其可作為早期精神分裂癥發(fā)病的病理性特征。隨后,通過構(gòu)建DISC1-Δ3鼠模擬精神分裂癥表型,并借助RNA測(cè)序、行為學(xué)、病毒載體介導(dǎo)的基因功能丟失技術(shù)、分子生物學(xué)等多種技術(shù)手段發(fā)現(xiàn),DISC1-Δ3 OPCs中Wnt/β-catenin的過度激活與下游Wif1異常高表達(dá),并通過Wif1抑制神經(jīng)元中非經(jīng)典Wnt通路,干擾突觸形成,而調(diào)控Wif1表達(dá)量可改善突觸形成障礙和精神分裂癥相關(guān)行為缺陷。該研究找到一個(gè)臨床干預(yù)精神分裂癥的分子靶點(diǎn)—Wif1,為精神分裂癥的治療提供了新的理論基礎(chǔ)。 陸軍軍醫(yī)大學(xué)博士生庾光丹與中山大學(xué)附屬第七醫(yī)院助理研究員蘇一洵為本文共同第一作者。曼切斯特大學(xué)Alexei Verkhratsky教授、陸軍軍醫(yī)大學(xué)肖嵐教授與牛建欽教授(Lead Contact)為本文共同通訊作者。
