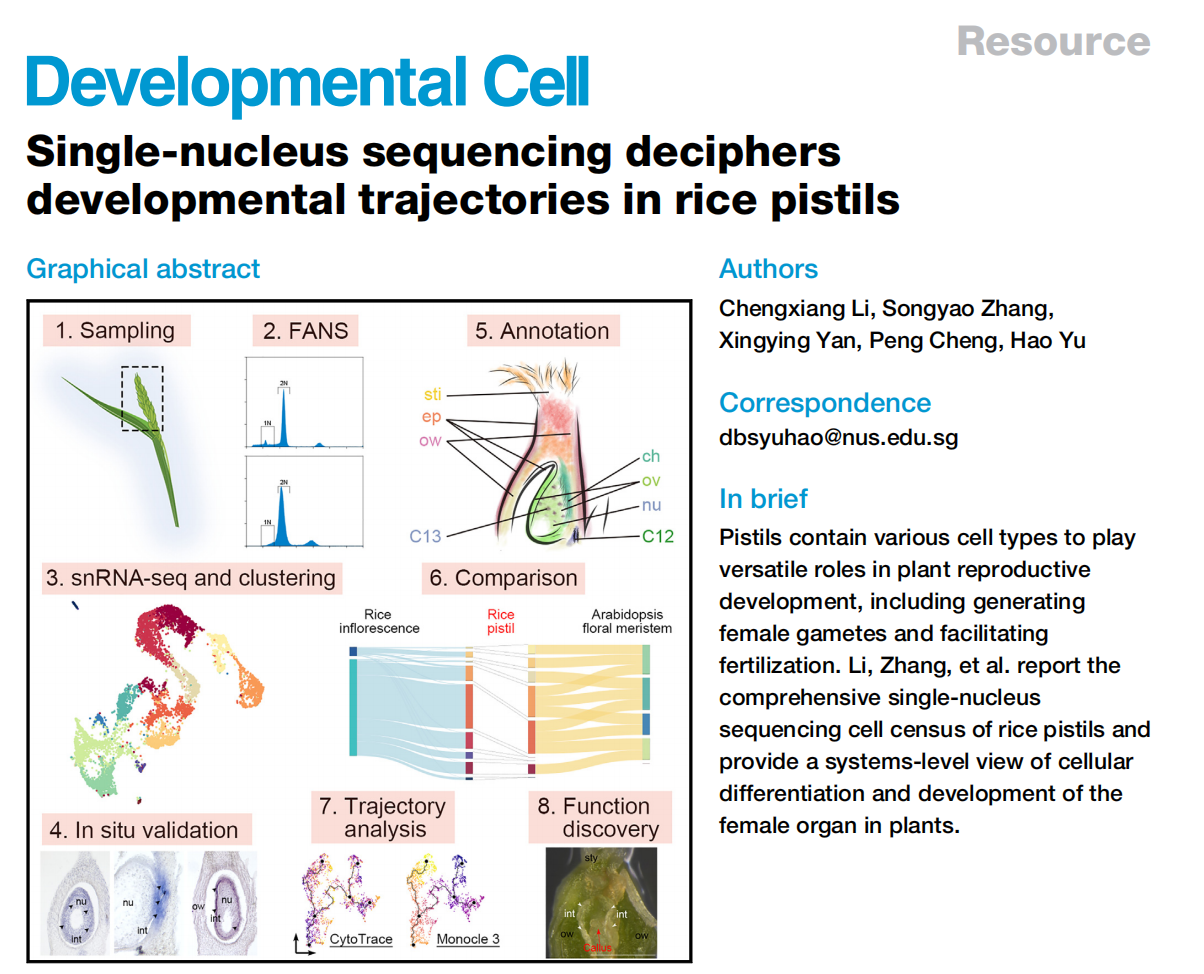
期刊:Developmental Cell
影響因子:10.7
主要技術:單細胞核RNA測序
導語
被子植物擁有孢子體和配子體世代交替的生命周期,這種交替發生在花柱這樣的植物器官中。水稻花柱包含胚珠并接受花粉以成功受精產生谷粒。水稻花柱中的細胞表達譜大部分是未知的。單細胞RNA測序(scRNA-seq)可能是一種選擇,但需要生成去壁原生質體。因此到目前為止,scRNA-seq的應用僅限于易于制備原生質體的某些營養器官,如根尖、莖頂分生組織、愈傷組織和幼葉。由于許多植物組織,包括子房,在原生質化方面難以處理,因此單細胞核RNA測序(snRNA-seq)是一種替代策略,它可以捕獲關于核內轉錄調控的確切信息,最大程度地避免了細胞質中正在發生的其他細胞過程的干擾。在這里,我們通過使用基于液滴的單細胞RNA測序展示了水稻花柱在受精前的細胞圖譜。通過原位雜交驗證的全新標記物識別有助于細胞類型注釋,揭示了胚珠來源和心皮來源細胞之間的細胞異質性。對1N(配子體)和2N(孢子體)核的比較確定了胚珠中生殖細胞在孢子體和配子體轉變之前的發育路徑,而對心皮來源細胞的軌跡分析顯示了先前被忽視的表皮特異性和柱頭功能特性。這些發現為在開花前水稻花柱的細胞分化和發育提供了系統級視角,并為理解植物雌性生殖發育奠定了基礎。
技術服務
單細胞核RNA測序、心皮來源細胞
雌性生殖發育、胚珠來源細胞
研究結果
1. 水稻子房的單細胞核RNA測序
為了研究水稻子房在單細胞水平上的細胞特性,我們首先對開花前1天收集的穗中未受粉子房進行了snRNA-seq(圖1A)。從未開放的小穗中解剖發育中的子房,并通過液氮快速冷凍來降低基因表達的變化,隨后立即進行原生質體的分離和通過熒光激活核排序(FANS)進一步純化核。在這個工作流程中解決了構建snRNA-seq文庫時遇到的兩個實驗挑戰,包括高質量核的要求、準確核計數和完整核RNA。首先,我們優化了工作流程中使用的RNase抑制劑的濃度,以達到最小化RNA降解。其次,我們還進行了初步測試,檢查核的質量并建立計數方法,簡化核計數步驟。因此,我們通過細胞分選儀分析了開放花中的核,記錄了由PI染色的細胞核發出的2N(二倍體;孢子體細胞)和1N(單倍體;主要由花粉貢獻)核的峰值位置。接著,我們在開花前1天收集的穗中未受粉子房進行snRNA-seq(圖1A和1B)。在FANS過程中,我們將子房2N核峰值與標準的2N峰值對齊,子房1N核的信號被2N峰的尾部掩蓋。
應用過濾后,我們得到了6004個細胞核(批次1),其中包含24656個可檢測基因(每個細胞759個)。我們還對另一個獨立的樣本進行了snRNA測序,得到了4360個細胞核(批次2),其中包含22738個可檢測基因(每個細胞455個),基于UMI分布選取了2169個從批次2中高質量的細胞核,并將其與批次1的數據結合進行進一步分析(總共8173個細胞核,每個細胞700個)。通過Seurat 4.0對結合數據集進行無監督分析,發現了14個不同的簇(0-13)(圖1C),批次1和批次2的數據表現出了類似的聚類趨勢。
2. 已知標記物對snRNA-seq的功能驗證
通過已知標記物驗證snRNA-seq的性能,簇11的標記基因包括SPW1,它是雄蕊(第3輪)的標識基因(圖1B和1C)。全胚位原位雜交實驗證實,簇11的另外兩個潛在標記物(OsFPPS3和OsCP1)確實在雄蕊殘余中表達,而簇5的兩個潛在標記物(OsWDA1和OsMTP11)在羽毛狀柱頭內表達(圖1D-1F)。這些結果支持我們snRNA-seq數據的聚類在生物學上具有意義,可用于進一步分析。
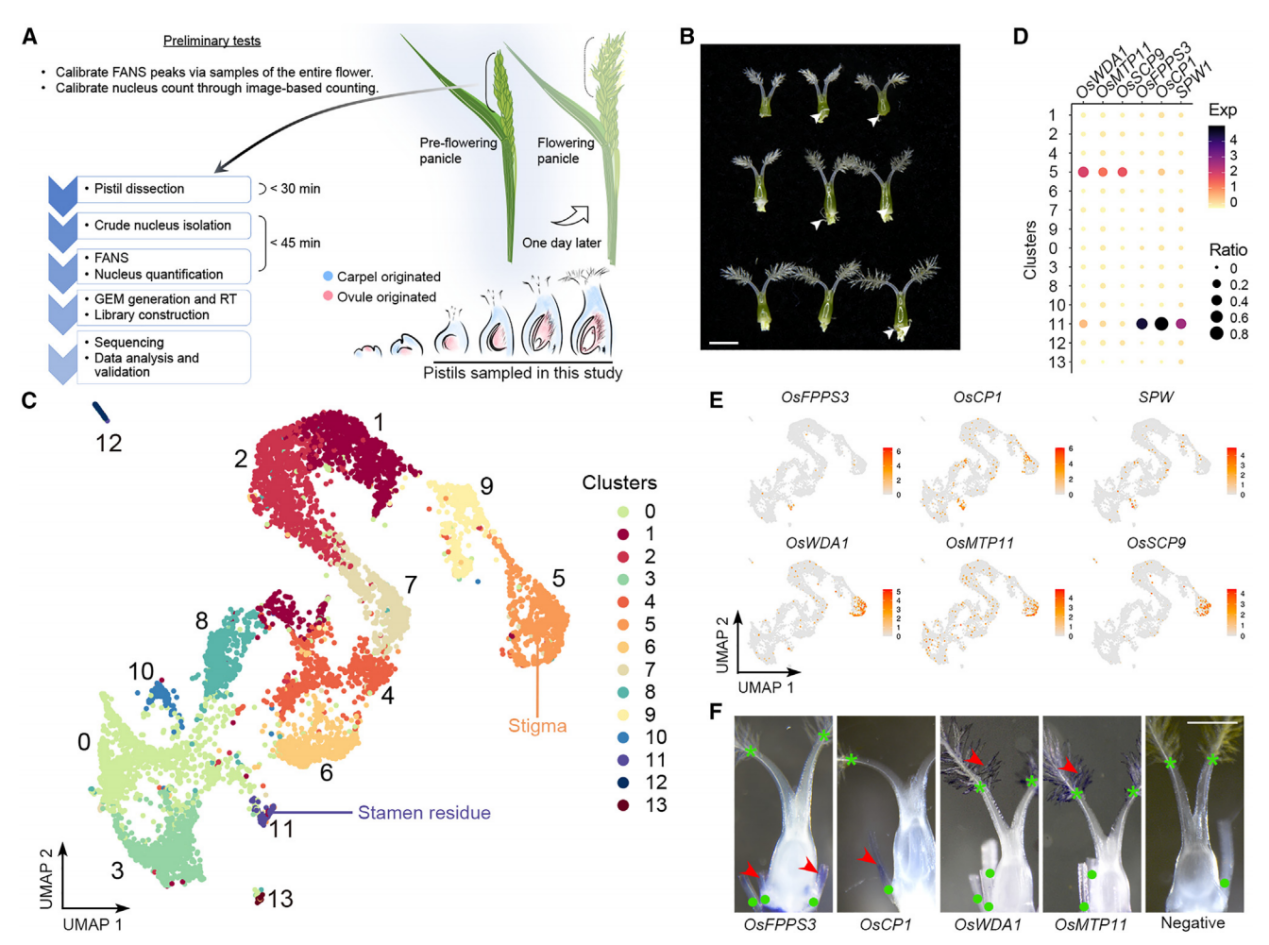
圖 1
3. 對簇標記物的原始細胞類型注釋
到目前為止,水稻柱頭中其他簇沒有經過驗證表達的特異標記物,我們試圖通過驗證一些相應候選標記物的空間定位來區分這些簇,原位雜交發現,一組不同簇中的標記物主要在子房和包圍胚珠的基部花柱中表達(圖2A,2B)。簇7的標記物(Os10g0562100/OsMYBS2和Os12g0566000/OsBOR1)在子房壁中表達,而簇1和2的標記物(Os11g0168500/OsERF118、Os03g0773300、Os02g0730000/OsALDH2a 和 Os06g0643500/OsHyPRP18)在子房壁的外側表面表達。我們還在花柱中檢測到簇4的標記物(Os08g0485400),并在基部花柱上方的兩側檢測到簇6的標記物(Os05g0380900/OsCML15和Os09g0517000)。簇9的標記物(Os01g0728100/OsGELP24),同樣在子房壁的內側表面和胚珠外皮中檢測到。另一組標記物的表達特異定位在胚珠的不同部分(圖2A,2B)。簇10標記物(Os12g0207000/OsMADS13和Os01g0220100/OsCEL9A)在整個胚珠中表達。簇8標記物(Os01g0849000/OsLTPd5 和 Os02g0686100)在胚珠及其連接的子房壁的柱頭端表達,而簇3標記物(Os03g0803066/ncRNA 和 Os02g0682200/MFO1)富集在胚珠的外種皮中。簇0標記物(Os05g0454500 和 Os05g0366900)特異地在胚珠核心內部表達。有趣的是,簇13標記物(Os04g0496300)僅以分散的小點形式存在于胚珠中,可能表明胚珠細胞的特定狀態。對簇12標記物(Os05g0130600)的檢查顯示其在胚珠下方的維管組織中表達(圖2B)。總體而言,除了簇5和11外,我們初步注釋了其它簇,其表達覆蓋了水稻雌蕊的各個部位(圖2C)。
4. 兩個主要分區表明是心皮細胞和胚珠細胞
值得注意的是,通過Monocle3進行的分區分析將簇分為五個不重疊的部分(圖2D)。最大的分區1包含簇1、2、4、5(柱頭)、6、7和9,而較小的分區2包含簇0、3、8和10(圖2E)。另外三個分區,包括簇11(雄蕊殘留)、12和13,分別與另外兩個主要分區相比,僅包含可忽略的核心數量(圖2D和2E)。那些已知的花器官鑒別基因在花發育的早期階段表達,其中大多數在本研究中未被識別為雌蕊給定簇的標記基因。然而,這些基因仍然可檢測到,并且在兩個主要分區(1和2)中優先表達。例如,C類基因OsMADS3/58,6,7,它們的上游調節基因OsMADS1,39,40,以及心皮鑒別基因DL7-9主要富集在分區1中,而D類基因OsMADS13存在于分區2,并被Seurat計算為簇10的標記物。另外,控制C和D類基因的SEP3類E類基因OsMADS8均勻地檢測到在分區1和2中。這些數據與原位雜交結果一起表明,分區1(簇1、2、4、5、6、7和9)和分區2(簇0、3、8和10)分別代表了起源于心皮和胚珠的細胞。此外,簇7和10中花器官鑒別基因的高表達表明這兩個簇都包含發育中雌蕊中較少分化狀態的細胞(圖2C)。
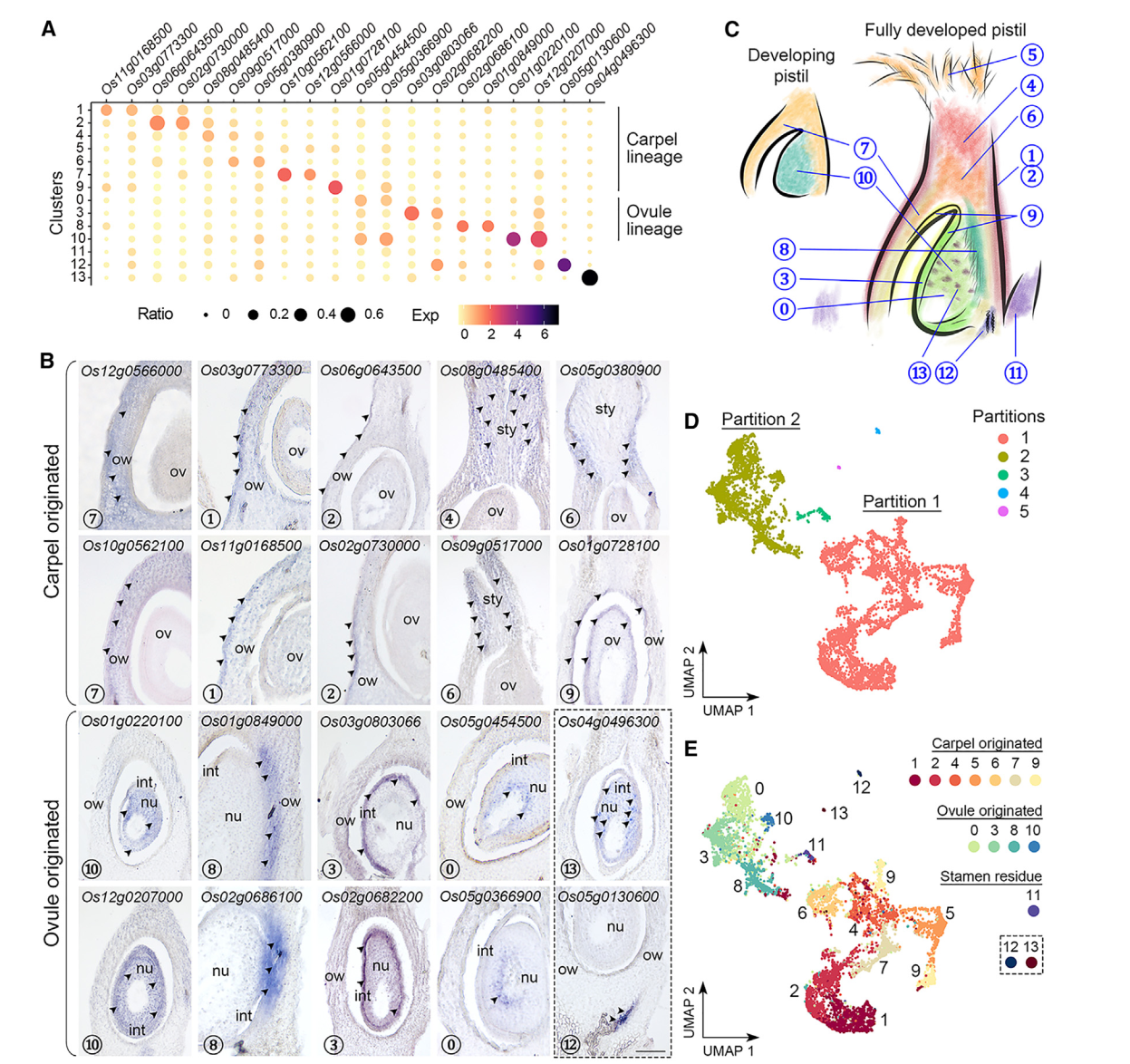
圖 2
5. 雌蕊、花序和花頂分裂細胞的比較
我們根據驗證的表達數據(圖2A和2B)將各個簇注釋為不同的細胞類型。三個單一簇,0、5和8,分別代表胚珠核、柱頭和柱頭區,而多個簇分別代表其他細胞類型,包括表皮(簇1、2和9)、子房壁(簇4、6和7)和胚珠(簇3和10)(圖3A)。雖然簇12和13不屬于分區1和2,并且無法確定地歸屬于任何細胞類型,但它們在兩個復制中具有相似的特征,并通過MetaNeighbor分析與柱頭和胚珠細胞密切相關(圖3B)。由于水稻雌蕊是從花序發出的穗子的一部分,我們將雌蕊細胞普查與報道的水稻發育中花序的單細胞數據集進行了比較。大多數雌蕊細胞被注釋為與穗子細胞具有高關聯概率的細胞類型,其次是軸節數、葉和分生組織細胞(圖3C)。雌蕊細胞只與穗子和軸節數細胞共享高相似性(圖3D)。在具有最高概率的細胞對比中(關聯概率>0.95),雌蕊中的大多數細胞類型與穗子細胞相似(圖3G)。因為雌蕊是從穗子而不是從花序的其它部分發育而來。柱頭細胞和簇12細胞與軸節數細胞相似(圖3G),這表明它們在維管組織中可能具有類似的功能,比如資源輸送和提供機械支持。
我們還將水稻雌蕊細胞與擬南芥多級蕊花分子單細胞數據集進行了比較。我們利用UMAP圖對擬南芥的細胞類型進行了標注(圖3E),并通過MetaNeighbor分析發現了幾種細胞類型之間的跨物種相似性。例如,水稻胚珠細胞和雌蕊細胞與擬南芥多級蕊花分子細胞相似,而水稻13號簇細胞與擬南芥的有絲分裂細胞高度相似(圖3F)。這五種細胞類型之間相互之間比其他細胞類型更接近,表現為高可能性關系(圖3F和3G)。此外,水稻邊孔細胞與擬南芥維管細胞相似,這些細胞與水稻12號簇細胞和擬南芥皮層細胞相對接近(圖3F和3G)。這些觀察結果表明了在不同植物物種的生殖器官發育中某些細胞類型的潛在保守性。
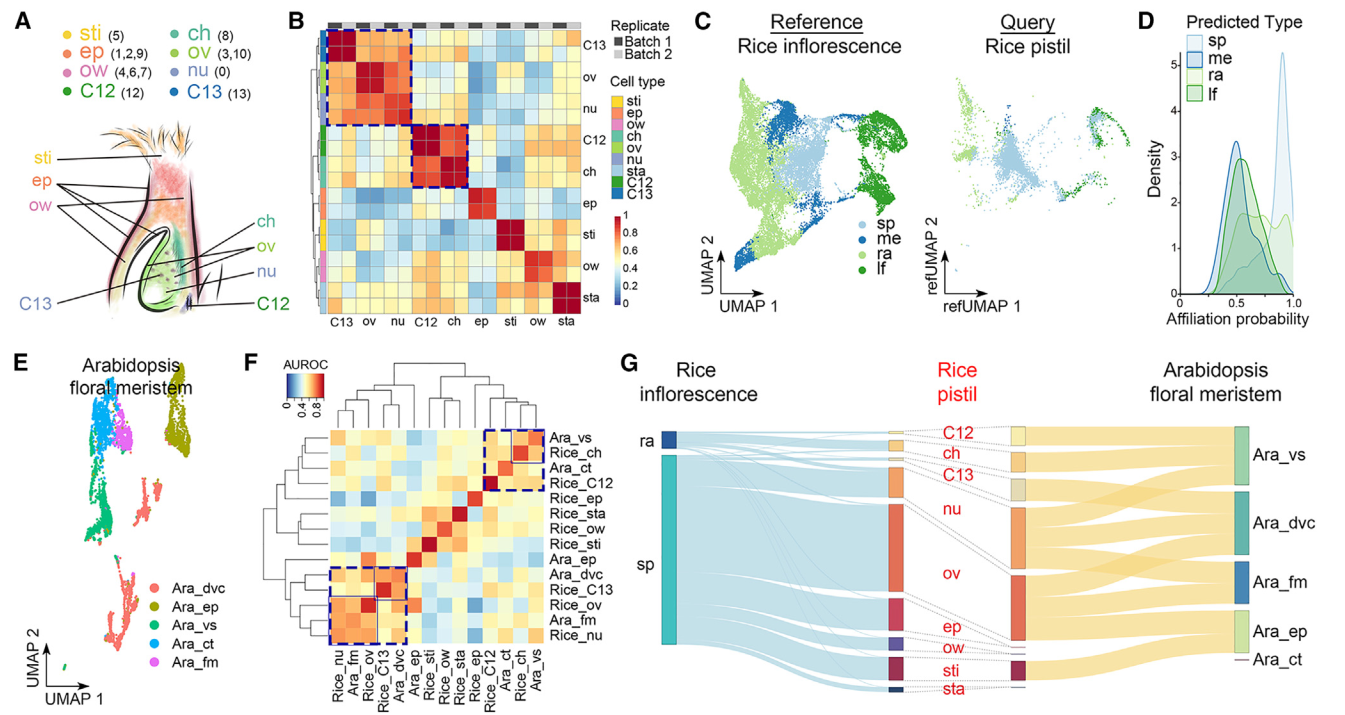
圖 3
6. 胚珠來源細胞的軌跡分析
為評估雌蕊細胞經歷的動態過程模式,我們隨后對來自0、3、8和10號簇的卵珠源細胞進行了軌跡分析,并通過原位雜交和分析證實(圖2)。我們選擇了表達OsMADS13最高的主節點Io作為Monocle3沿著軌跡進行擬時間分析的起始點(圖4A)。擬時間線的預測軌跡包括Io-IIo-IIIo-Vo的“莖路徑”和兩個“葉路徑”,IIo-VIo和IIIo-IVo(圖4A)。終點主節點VIo和IVo位于8號和3號簇(圖4A),分別被標注為邊孔細胞和珠被細胞(圖2A-2C)。因此,葉路徑表明了珠被和珠質分化的不同軌跡。分支點的偽時間表明,邊孔細胞較早確定(通過IIo),而珠被細胞則較晚確定(通過IIIo)(圖4A)。這符合胚珠基尖軸的分化。我們進一步研究了莖路徑的細節。沿偽時間有動態表達的基因被整合成幾個基因模塊(圖4B),進一步聚類成三組,“a”、“b”和“c”(圖4B)。這三組表現出莖路徑中三波基因表達,與基因本體的特征相關(圖4D)。組“a”代表路徑的起始部分,富集基因與發育調控和對內源和外源信號的反應有關,表明它們參與調節不太分化的細胞對發育和環境信號的反應,而組“c”代表路徑的末端部分,富集基因與DNA復制和染色體組織相關,與細胞分化相關。
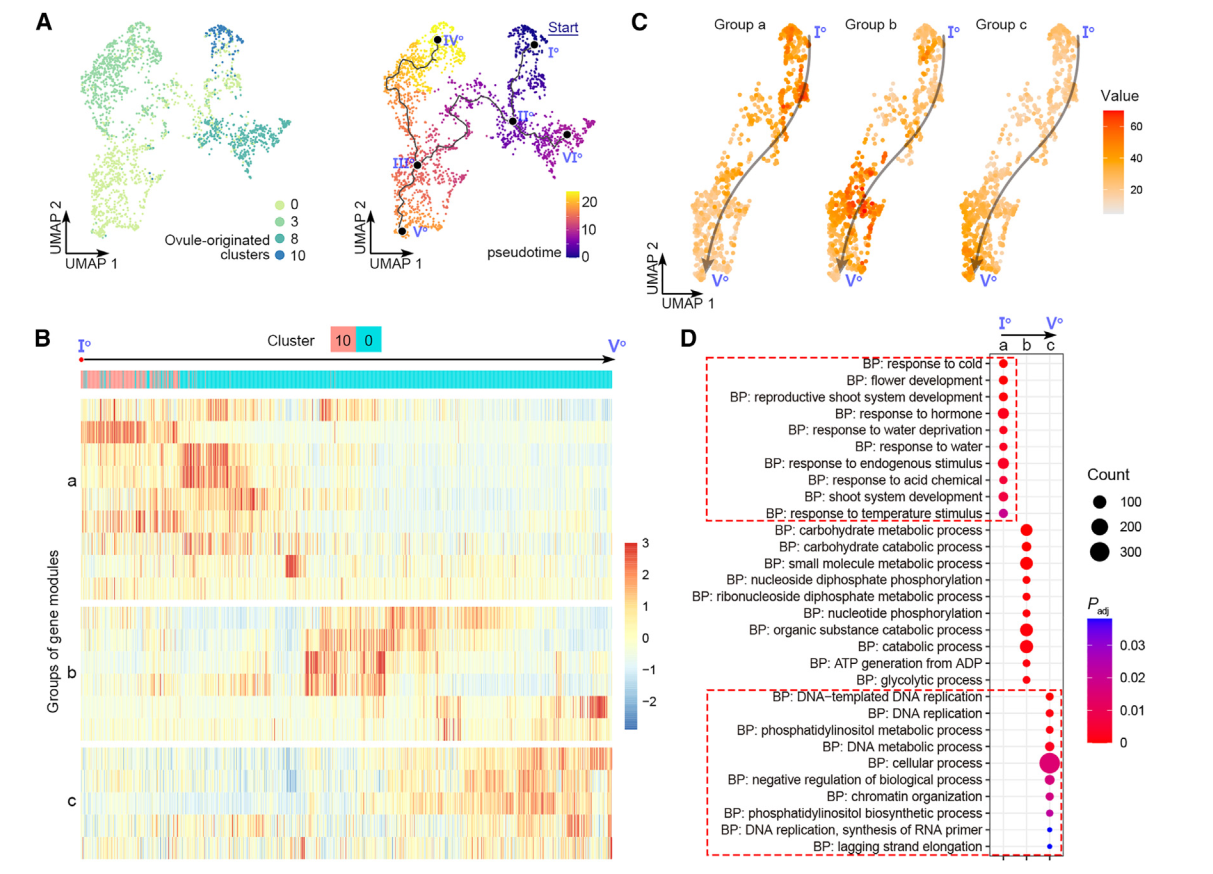
圖 4
7. 孢子體-配子體的轉變
我們還對由FANS分離出的推測1N細胞進行了snRNA-seq,獲得1625個核作為輸入1N細胞。當這些細胞被Seurat投射到2N細胞的UMAP結構上作為參考時,大多數這些細胞都與0簇(胚珠細胞)相關聯(圖5A),構成了卵珠源細胞的主要莖路徑(圖4A)。對于與0號簇關聯的推測1N細胞,大多數細胞的關聯概率在0.5和0.9之間,而關聯概率超過0.95的細胞只占很小一部分(圖5B)。對于注釋為其他簇的推測1N細胞(圖5A),大多數細胞的關聯概率超過0.95(圖5B),表明這些細胞是仍殘留在由FANS采集的推測1N核組織中2N細胞的尾部。因此,認為與0號簇相關的輸入1N細胞的部分是真實的1N細胞(1625個輸入1N細胞中的989個)。這些真實的1N細胞(989個細胞)和0號簇的2N細胞(共計兩批1237個核)通過Seurat 4.0分析相互區分(圖5C),并展現出不同的分子特征。
值得注意的是,0號簇的2N細胞與1N細胞之間的差異表達基因在生殖體-配子體轉變過程中顯示了轉錄組譜的變化。例如,OsMEL2和OsMADS29這兩個基因在2N細胞中更具有優勢表達,它們分別對于前減數G1/S階段轉變或核被細胞降解至關重要。相比之下,在1N細胞中特異表達的基因包括與減數分裂相關的基因,如水稻MutS同源(MSH)家族基因OsMSH4、46缺陷的偶合母紡線染色體1(OsDLC1)、以及OsPAIR2,以及一些已知的雌孢子發生調控者,如OsERECTA2(OsER2)和水稻不定形配子體1(OsIG1)(圖5D和5E)。這些數據表明,簇0細胞與擔孢子體-配子體轉變期間的減數分裂密切相關。此外,由于富集在胚珠來源細胞干路盡端的基因與DNA復制和染色體組織相關(圖4C和4D),主要由簇0細胞組成的干路主要代表雌性生殖細胞的特化。
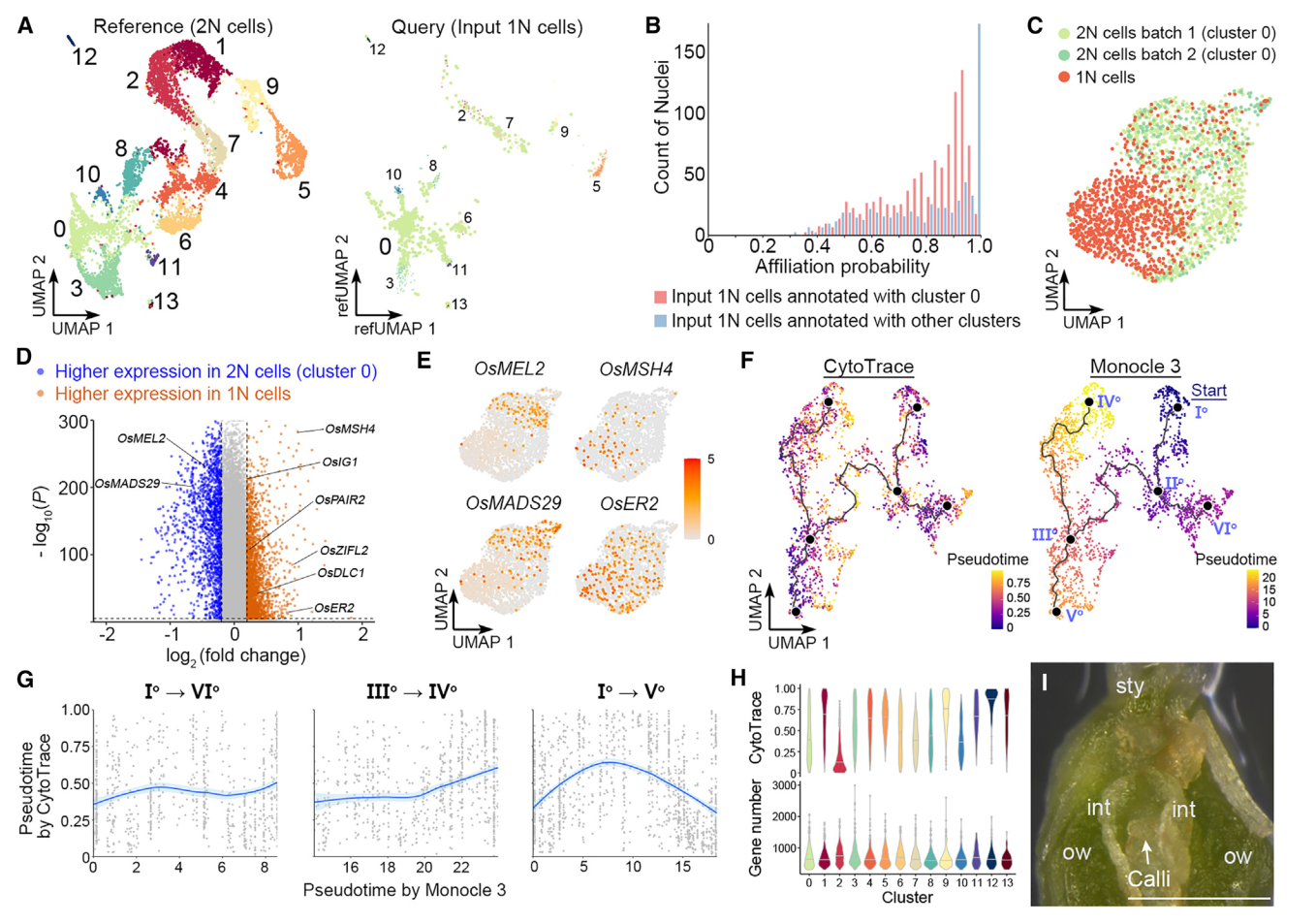
圖 5
8. 孢子-配子體轉變前多能性的重置
我們比較了由Monocle3和CytoTRACE推斷的胚珠來源細胞軌跡的擬時間,并發現這兩種方法預測的偽時間模式不總是在胚珠來源細胞軌跡中相關(圖5F)。在珠頭明確化路徑(Io–VIo)和珠被的后半部分(IIIo–IVo)中,它們呈正相關,在干路的后半部分(IIo–Vo)中則呈負相關(圖5G),其由胚珠細胞(群集0)(圖4A)構成。由于轉錄多樣性可能會受到不同群集中檢測到的基因數的技術性影響,我們計算了不同群集的平均可檢測基因數和CytoTRACE分數。在各群集中檢測到的平均基因數略有變化,而CytoTRACE分數差異較大,中值范圍為0.11至0.92(圖5H)。因此,干路后半段的CytoTRACE值的降低不太可能是由于可檢測基因數變化。由于從IIo–Vo到描繪通向雌性生殖細胞命運的子路,由CytoTRACE在干路后半段顯示的轉錄多樣性增加,意味著在孢子體-配子體過渡之前恢復多能性。在所有類型的細胞中,當將切開的雌蕊放在愈傷組織誘導培養基上時,只有珠心細胞容易產生愈傷組織(圖5I)。
9. 心皮來源細胞的軌跡分析
我們進一步對心皮來源細胞進行了軌跡分析,通過評估最大分區1,除了簇9(圖2E)。簇9細胞核被分成兩個不同的群體,其中一個鄰近簇4,另一個鄰近簇5(圖2D和2E)。此外,簇9的標記物位于子房壁的內表面和胚珠的外被(圖2B和2C)。由于這些觀察結果表明簇9細胞核的混合性質,在軌跡分析中排除了它們。我們選擇具有DL最高表達的主節點,這一節點是在心皮原基早期表達的,作為Monocle3沿著軌跡進行偽時間分析的起點(圖6A)。從起始節點(圖6A)分出了三個預測的子路徑,包括Ic–IIIc、Ic–IIc–IVc和Ic–IIc–Vc。由于Monocle3和CytoTRACE推斷的擬時間模式在心皮來源細胞軌跡中呈正相關,我們接著僅分析由Monocle3推斷的擬時間,并揭示了幾個與心臟發育相關的特征。
首先,在Ic–IIIc的路徑中,具有特異表達模式的簇1和2細胞位于子房壁的外表面(圖2B和2C),指示了這一路徑用于指定表皮命運的擬時間路徑。當我們分析沿著Ic–IIIc和Ic–IIc的擬時間路徑的基因模塊的表達動力學時,這些模塊被分為五個組(圖6B)。從d到a的四組基因在Ic–IIc路徑中呈現了四波連續的可逆表達(圖6C)。“d”組基因主要存在于簇7細胞中,主要分布在主節點Ic周圍,與“生物調控”和各種發育相關的GO術語有關,而“a”組基因主要存在于第1簇細胞中,主要分布在末端主節點IIIc周圍,富集與磷酸化和激酶相關的功能屬性(圖6B-6D)。這些觀察結果表明,子房表皮的分化軌跡沿著Ic -IIIc路徑。
值得注意的是,表皮路徑(Ic -IIIc)在心皮起源細胞軌跡的起點Ic與其他路徑是分開的,這意味著軌跡上的其他細胞可能缺乏子房表皮特征。掃描電鏡顯示,花柱表面的細胞不規則,而子房壁外表面的表皮細胞規則、緊湊、排列良好(圖6E)。此外,子房表面抗甲苯胺藍染色,而花柱和柱頭的耐染性明顯增強(圖6F),說明子房和花柱/柱頭的表皮特征不同。然后我們對雌蕊的各種斷面進行蘇丹IV染色,發現子房壁外表面的表皮角質層完好無損,但花柱部分受損,柱頭缺失(圖6G)。綜上所述,這些結果表明,Ic -IIIc的擬時間路徑特異性地描述了子房表皮的特征。
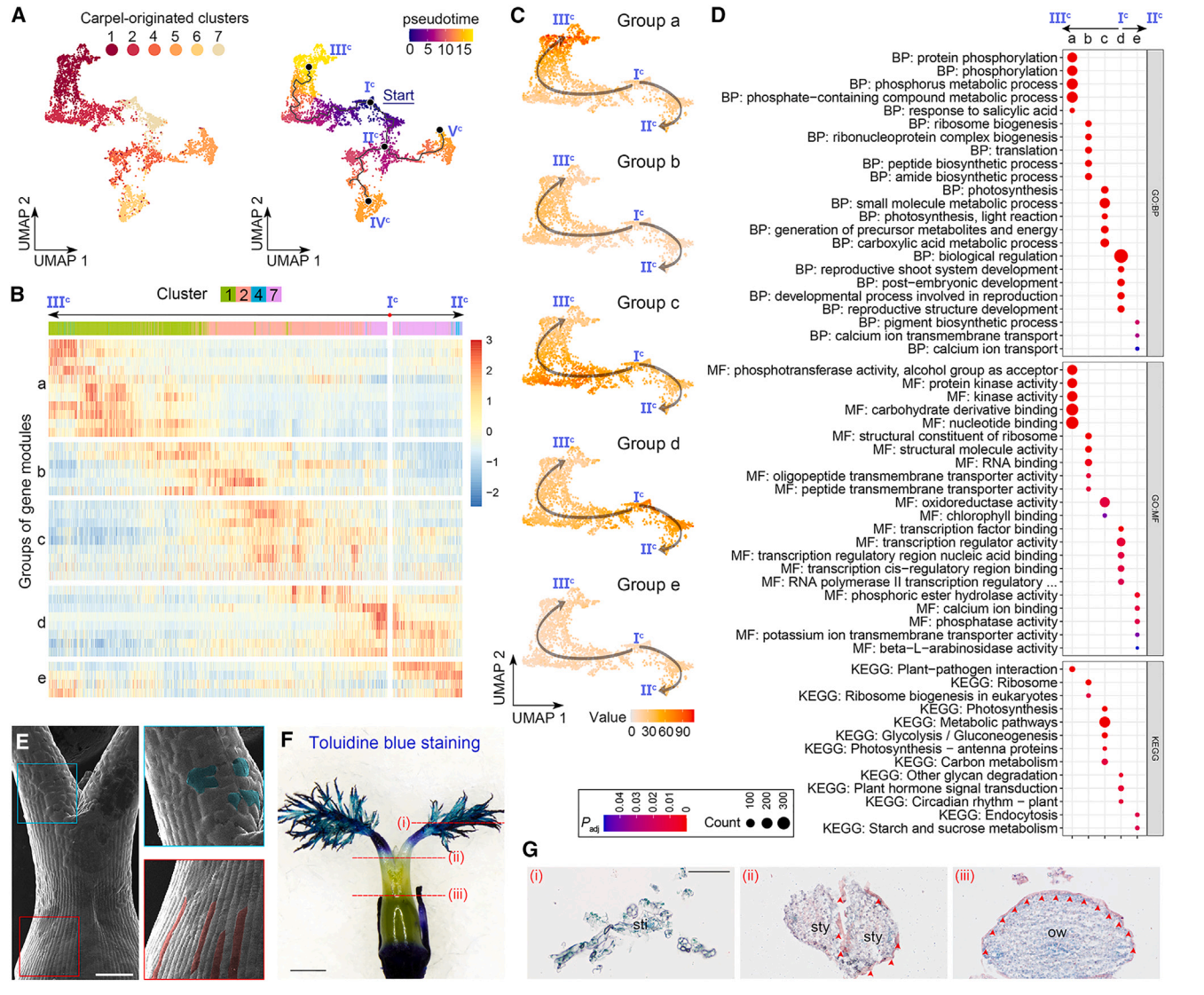
圖 6
其次,根據表達動力學,將IIc -IVc和IIc -Vc兩條偽時間路徑上的基因模塊從主節點IIc聚為“a”到“d”四組(圖6A和7A)。a組基因主要存在于簇6細胞中,在末端主節點IVc周圍富集,并與光合作用相關活動相關(圖7A-7C)。事實上,I2-KI染色檢測到一個富含淀粉的區域,表明在基柱處光合作用活躍(圖7E),這與同一區域的簇6標記的表達一致(圖2B),表明基柱的發育軌跡沿著IIc -IVc的路徑。相比之下,IIc -Vc的路徑描繪了柱頭命運的發育軌跡,因為包含柱頭細胞的簇5中的“d”組基因在節點Vc周圍占主導地位,并且富含柱頭相關的GO術語,如脂質相關功能(圖7A-7C)。
第三,b組和c組基因在分支點IIc富集,與鈣離子結合、鈣調蛋白結合、鈣離子跨膜轉運活性、信號轉導和細胞通訊等功能相關(圖7A-7C)。在柱頭整個發育軌跡的時間軸中,這些鈣相關基因在柱頭細胞中特異性表達,而d組基因在柱頭細胞中表達僅在過程的最后出現(圖7E),表明鈣相關信號在柱頭規范之前就在柱頭發育中發揮了作用。然后,我們在開花前1天使用成熟的鈣通道阻滯劑LaCl3和GdCl3處理幼小雌蕊,第二天柱頭之間的角度明顯增大(圖7F和7G)。這支持鈣信號參與柱頭發育的各個方面。
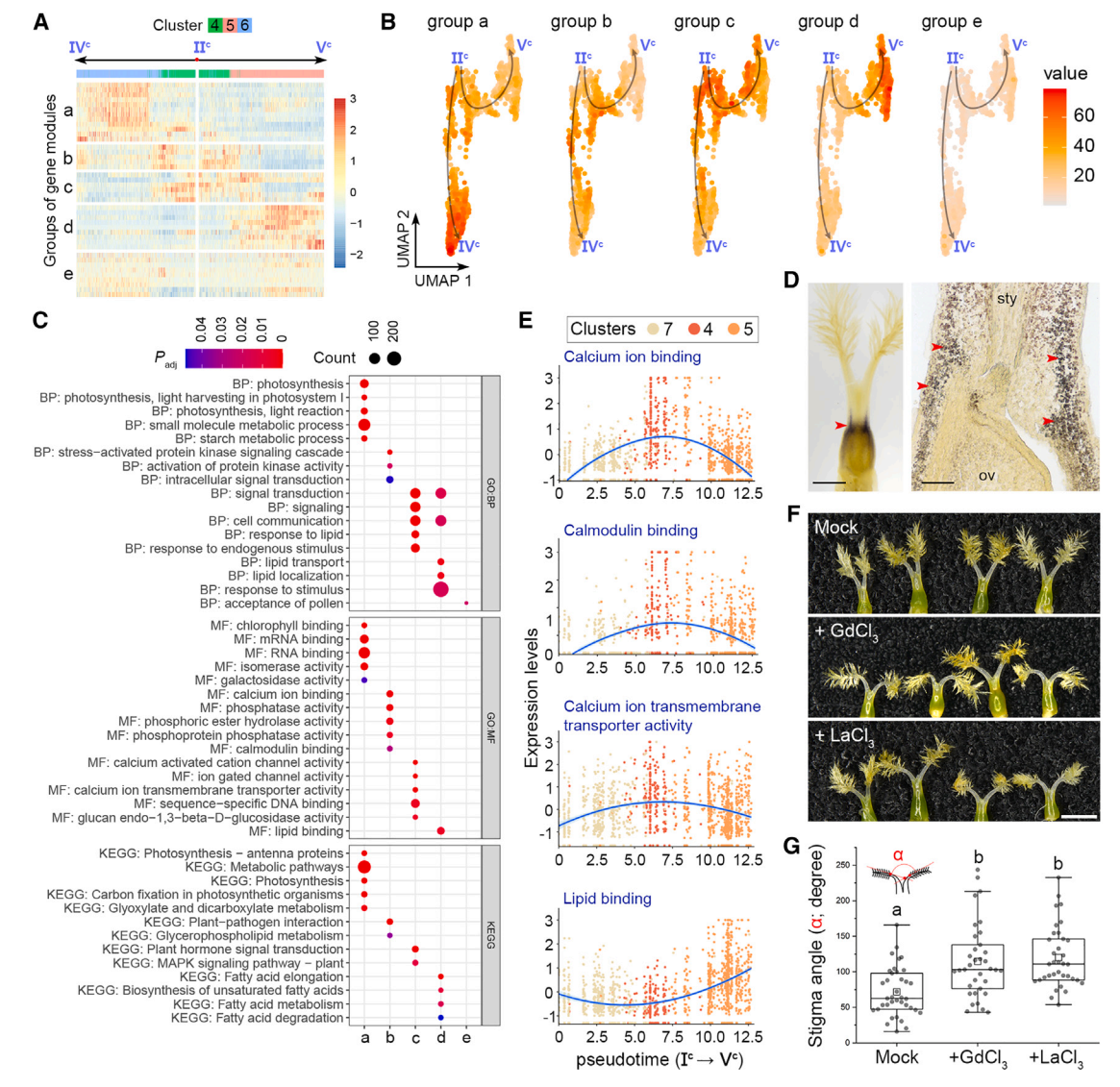 圖 7
圖 7結語
盡管近幾十年來進行了許多研究以理解植物生殖發育,但對于承載生殖子代和配子體代的關鍵轉變的柱頭的細胞分化的系統級視圖在被子植物中仍然未知。在水稻中,來自花序分枝分生組織的原生質體的單細胞測序已經揭示了早期花序和花發育的分化軌跡,然而目前不清楚發育中的柱頭中各種細胞類型如何為其在生成雌配子、作為受精的場所以及保護種子發育中的獨特和多功能角色做出貢獻。為了填補這些關鍵知識空白,本研究建立了snRNA-seq方法結合了原位雜交驗證、批量RNA-seq和軌跡分析,提供了一種整合手段,用于研究水稻花柱的細胞普查。本研究發現水稻花柱空間時間snRNA-seq細胞普查使我們能夠從單細胞水平上解剖與水稻雌蕊細胞異質性和發育軌跡相關的調控事件,這是更好地理解植物的雌性生殖發育和開花植物中相互關聯的基因調控網絡的重要一步。其中協調雌配子發育和為受精做準備在胚珠來源細胞和心皮來源細胞中得到無縫調節。進一步將RNA-seq與其他快速發展的單細胞多模學技術相結合,將使我們全面闡明植物生殖發育底層的細胞特性及其與作物改良相關的技術創新成為可能。
參考文獻:
Li C, Zhang S, Yan X, Cheng P, Yu H. Single-nucleus sequencing deciphers developmental trajectories in rice pistils. Dev Cell. 2023 Apr 24;58(8):694-708.e4. doi: 10.1016/j.devcel.2023.03.004. Epub 2023 Apr 6. PMID: 37028425.
