
1982年,Whitlock通過(guò)長(zhǎng)期的研究工作建立了骨髓長(zhǎng)期培養(yǎng)系統(tǒng)(LTBMC),為人們對(duì)B細(xì)胞前體細(xì)胞的增殖和分化進(jìn)行深入的研究提供了可能。由于B細(xì)胞前體細(xì)胞的生長(zhǎng)對(duì)于細(xì)胞基質(zhì)有嚴(yán)格的依賴性,研究者們推測(cè)骨髓基質(zhì)細(xì)胞可能分泌一種B細(xì)胞前體細(xì)胞的生長(zhǎng)刺激因子;直到1988年,Namen等應(yīng)用LTBMC獲得一株SV40病毒轉(zhuǎn)染的骨髓基質(zhì)細(xì)胞株(bone marrow stromal cell line)IXN/A6,發(fā)現(xiàn)其能分泌一種前B細(xì)胞刺激因子,起初命名為淋巴細(xì)胞生長(zhǎng)素(Lymphopoietin-1,LP-1),或小鼠前B細(xì)胞生長(zhǎng)因子(Murine pre-B cell growth factor),但后來(lái)業(yè)界將其統(tǒng)一命名為IL-7。
IL-7生物學(xué)作用
IL-7(白細(xì)胞介素-7)是一種在淋巴細(xì)胞分化、增殖和存活中起重要作用的細(xì)胞因子,也是IL-2超家族的成員之一。它由胸腺、骨髓和腸的基質(zhì)上皮細(xì)胞分泌產(chǎn)生,并通過(guò)由IL-7rα/CD 127和普通γ鏈組成的受體異二聚體復(fù)合物(Il-7R)發(fā)出信號(hào)。
IL-7具有多種生物學(xué)活性,通過(guò)與Il-7R結(jié)合從而影響各種類(lèi)型的細(xì)胞。其中IL-7R的γ鏈與IL-2、IL-4、IL-9、IL-15和IL-21等多種白介素的受體共享,并在各種細(xì)胞中表達(dá)[1]。隨著后續(xù)研究工作的深入,研究者們發(fā)現(xiàn)IL-7在許多免疫細(xì)胞的發(fā)育和維持中起著不可或缺的作用。
NK細(xì)胞發(fā)揮作用
IL-7是NK細(xì)胞增殖和促進(jìn)其分化成熟、發(fā)揮細(xì)胞毒性的重要調(diào)節(jié)因子,在體外培養(yǎng)中可以刺激NK細(xì)胞的增殖和活性,IL-7誘導(dǎo)培養(yǎng)的NK細(xì)胞在數(shù)量上與IL-2沒(méi)有明顯差異;IL-7或IL-7R的缺失可導(dǎo)致免疫細(xì)胞發(fā)育嚴(yán)重受損,尤其是B淋巴細(xì)胞。
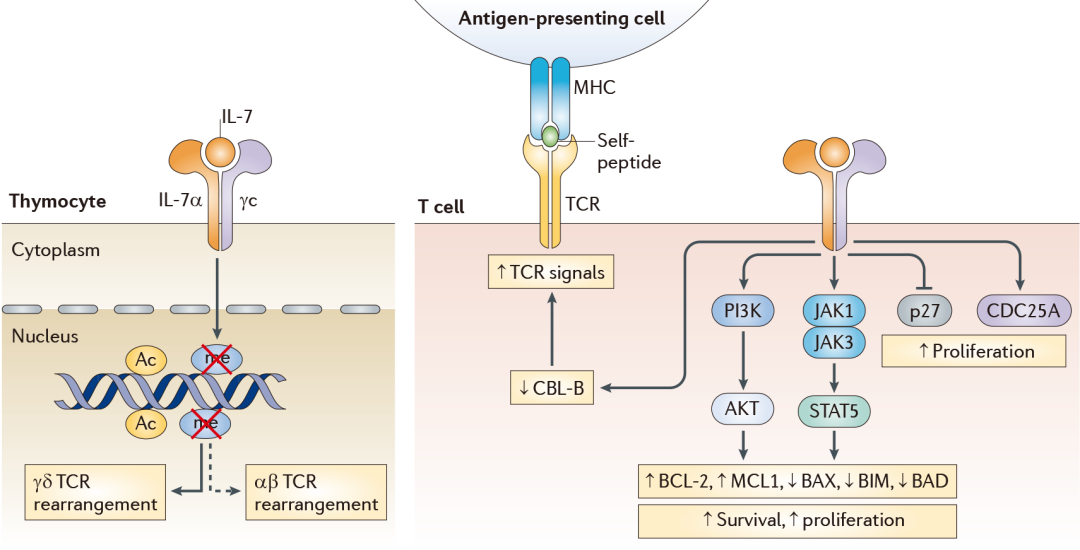
IL-7介導(dǎo)的信號(hào)通路[1]
T細(xì)胞發(fā)揮作用
幾乎所有T細(xì)胞亞群的維持和存活都需要IL-7的存在。Patel等曾報(bào)道了IL-7和前T細(xì)胞受體(pre-TCR)在成人T淋巴細(xì)胞從造血祖細(xì)胞中分化和成熟的過(guò)程中發(fā)揮著重要的作用[1]。IL-7通過(guò)調(diào)節(jié)T細(xì)胞內(nèi)在的凋亡通路,從而影響著T細(xì)胞的存活。在T細(xì)胞激活且發(fā)揮功能后,IL-7Rα開(kāi)始呈現(xiàn)表達(dá)缺失,不受TCR信號(hào)的負(fù)調(diào)節(jié)作用,其目的是避免過(guò)多活化T細(xì)胞存活,從而引起自身免疫性疾病的發(fā)生,具體機(jī)制為:外周IL-7R的表達(dá)依賴于Foxo1信號(hào)的刺激。TCR或IL-2信號(hào)通過(guò)PI3K-AKT信號(hào)通路負(fù)調(diào)控Foxo1,但是部分效應(yīng)T細(xì)胞在執(zhí)行完任務(wù)后,會(huì)變成記憶T細(xì)胞,長(zhǎng)期存活于人體,在后續(xù)的發(fā)育中,有可能發(fā)生IL-7Rα的重新表達(dá)。
樹(shù)突狀細(xì)胞發(fā)揮作用
IL-7R在樹(shù)突細(xì)胞和單核細(xì)胞上均表達(dá),且似乎在多個(gè)造血譜系中起作用[2]。在橋接固有免疫和適應(yīng)性免疫過(guò)程的樹(shù)突細(xì)胞中,IL-7R對(duì)其起免疫調(diào)節(jié)作用,Jak-Stat和PI3K Akt 信號(hào)通路均通過(guò)IL-7與IL-7R的結(jié)合而被激活[3]。這些途徑包括信號(hào)串?dāng)_、共有相互作用結(jié)構(gòu)域、反饋環(huán)、整合的基因調(diào)節(jié)、多聚化及配體競(jìng)爭(zhēng)等多個(gè)環(huán)節(jié)。IL-7信號(hào)傳導(dǎo)的一些靶標(biāo),包括Bcl2和Pyk2,這將有助于細(xì)胞的存活。
多能干細(xì)胞發(fā)揮作用
IL-7對(duì)免疫細(xì)胞的活性發(fā)揮有著重要的作用。是一種對(duì)T、B、NK細(xì)胞的生長(zhǎng)、存活及分化有重要作用的細(xì)胞因子。有小鼠基因敲除的相關(guān)研究表明,IL-7在淋巴細(xì)胞的生存中起著至關(guān)重要的作用,是一種對(duì)淋巴細(xì)胞分化、增殖、活化等過(guò)程維持平衡的重要刺激因子。El-Kassar等闡述了IL-7能一直對(duì)Notch-1信號(hào)通路(在多種細(xì)胞特化中起關(guān)鍵作用的信號(hào)途徑)產(chǎn)生影響,并且影響胸腺組織中T-B淋巴細(xì)胞系的平衡[4]。IL-7和肝細(xì)胞生長(zhǎng)因子(HGF)形成的異二聚體是前祖B細(xì)胞生長(zhǎng)刺激因子,也能有效刺激多能干細(xì)胞(IPS)向淋巴系祖細(xì)胞分化。
IL-7的臨床應(yīng)用研究
在臨床上,異常增高或不受控制的IL-7和IL-7R水平,會(huì)引起免疫病理學(xué)的改變,也是導(dǎo)致自身免疫性疾病發(fā)生的重要因素。目前已經(jīng)發(fā)現(xiàn)IL-7與自身免疫性糖尿病,類(lèi)風(fēng)濕關(guān)節(jié)炎,強(qiáng)直性脊柱炎,炎癥性腸炎病等有著緊密的關(guān)聯(lián)。
在抗腫瘤方面,IL-7是增加細(xì)胞毒性CD8+T淋巴細(xì)胞的最有效的細(xì)胞因子,它對(duì)膠質(zhì)瘤、黑色素瘤、淋巴瘤、白血病、前列腺癌和膠質(zhì)母細(xì)胞瘤等腫瘤均有一定的抑制作用。然而,也有一些研究表明IL-7也可能有促腫瘤作用,尤其是在實(shí)體瘤方面。因此,現(xiàn)今關(guān)于IL-7在腫瘤發(fā)病機(jī)制中的作用是備受爭(zhēng)議的。
最新研究(一)
今年,上海交通大學(xué)醫(yī)學(xué)院附屬瑞金醫(yī)院/國(guó)家轉(zhuǎn)化醫(yī)學(xué)研究中心醫(yī)學(xué)基因組學(xué)國(guó)家重點(diǎn)實(shí)驗(yàn)室團(tuán)隊(duì)在《Scientific Reports》期刊上發(fā)表了文章“Transgenic expression of IL-7 regulates CAR-T cell metabolism and enhances in vivo persistence against tumor cells”[5],該項(xiàng)研究工作表明:IL-7將CAR-T細(xì)胞維持在分化程度較低的T細(xì)胞狀態(tài),調(diào)節(jié)不同的代謝活動(dòng),防止CAR-T細(xì)胞耗竭,這可能是CAR-T細(xì)胞長(zhǎng)達(dá)數(shù)年維持其代謝適應(yīng)性和抗腫瘤反應(yīng)的關(guān)鍵。

最新研究(二)
2021年3月,《Science Signaling》期刊上發(fā)表了土耳其比爾肯大學(xué)Caglar Cekic等人的研究結(jié)論[6],他們發(fā)現(xiàn)IL-7通過(guò)阻斷腺苷通路的免疫抑制效應(yīng)保護(hù)CD8 +T細(xì)胞,促進(jìn)其對(duì)腫瘤細(xì)胞的持續(xù)性殺傷。

最新研究(三)
2021年,一篇以“IL-7 coupled with IL-12 increases intratumoral T cell clonality, leading to complete regression of nonimmunogenic tumors”為題的科研工作發(fā)表在《Cancer Immunology ,Immunotherapy 》期刊上發(fā)表[7]。該項(xiàng)研究結(jié)果表明,IL-7和IL-12的瘤內(nèi)雙表達(dá)與IL-12單獨(dú)表達(dá)相比,增加了免疫原性差的腫瘤中CD8+ T細(xì)胞的浸潤(rùn)。IL-7與IL-12結(jié)合后,盡管T細(xì)胞被活化,但并沒(méi)有增加CD8+ T細(xì)胞耗竭的比例,因此研究者認(rèn)為IL-7有助于維持T細(xì)胞在腫瘤微環(huán)境中的狀態(tài)。

討論:一些科研工作的結(jié)果表明,IL-7還可以促進(jìn)干細(xì)胞移植和腫瘤患者化療后的免疫重建。然而,目前呈現(xiàn)在臨床治療的根本現(xiàn)狀是IL-7帶來(lái)的免疫學(xué)效應(yīng)能否轉(zhuǎn)化為降低患者死亡率和發(fā)病率的關(guān)鍵,尚不明朗!這也是目前IL-7在臨床應(yīng)用領(lǐng)域面臨的最大障礙和挑戰(zhàn)。在不久的將來(lái),希望能在千萬(wàn)科研工作者的努力下,IL-7在免疫細(xì)胞治療領(lǐng)域可以真正惠及患者,給予腫瘤患者的康復(fù)帶來(lái)新的曙光!
同立海源IL-7產(chǎn)品
產(chǎn)品優(yōu)勢(shì):
HEK293細(xì)胞表達(dá)、GMP級(jí)生產(chǎn)
高純度、高活性、高穩(wěn)定性
ISO13485、ISO9001質(zhì)量體系認(rèn)證
數(shù)據(jù)測(cè)試
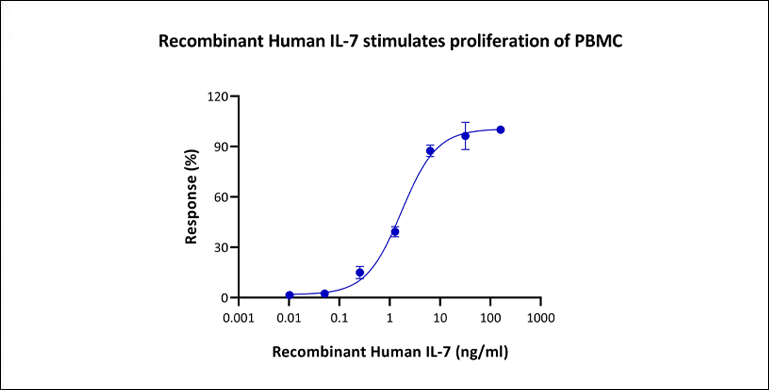
重組人IL-7蛋白(GMP-TL506)對(duì)PHA活化的PBMC細(xì)胞
增殖活性EC50為1.716ng/ml。
參考文獻(xiàn):
[1]Patel ES,Okada S,Hachey K,et al.Ragulation of in vitro human T cell development through interleukin-7 deprivation and anti-CD3 stimulation.BMC Immunol,2012,13(1):46.
[2]Barata, Durum and Seddon, Flip the coin: IL-7 and IL-7R in health and disease. Nature Immunology, 2019.
[3]Juan Huang,Zhiyao Long,Renyong Jia,et al,The broad immunomodulatory effects of IL-7 and its application in vaccines. Immunology,doi: 10.3389,2021.680442.
[4]El-Kassar N,Flomerfelt FA,Choudhury B,et al.High levels of IL-7 cause dysregulation of thymocyte development.Int Immunol,2012,24(10):661-671.
[5]Li, L., Li, Q., Yan, ZX. et al. Transgenic expression of IL-7 regulates CAR-T cell metabolism and enhances in vivo persistence against tumor cells. Sci Rep 12, 12506 (2022).
[6]Altay Koyas,Suat Tucer,et,al. Interleukin-7 protects CD8+ T cells from adenosine-mediated immunosuppression.DOI:10.1126/scisignal.abb1269.
[7]Tasaki, M., Yamashita, M., Arai, Y. et al. IL-7 coupled with IL-12 increases intratumoral T cell clonality, leading to complete regression of non-immunogenic tumors. Cancer Immunol Immunother(2021).
關(guān)于同立海源
北京同立海源生物科技有限公司,成立十余年專(zhuān)注細(xì)胞和基因治療(CGT)上游GMP級(jí)原料試劑研發(fā),致力于為生命科學(xué)提供可靠的產(chǎn)品與服務(wù)。產(chǎn)品涉及真核重組蛋白、細(xì)胞分選試劑、無(wú)血清培養(yǎng)基、細(xì)胞培養(yǎng)試劑盒、工具酶。為細(xì)胞和基因治療、mRNA開(kāi)發(fā)、抗體藥物開(kāi)發(fā)、細(xì)胞儲(chǔ)存等生物制藥和IVD領(lǐng)域提供核心原料試劑與服務(wù)。
公司建有符合cGMP標(biāo)準(zhǔn)的萬(wàn)級(jí)潔凈車(chē)間,包括哺乳動(dòng)物細(xì)胞表達(dá)蛋白質(zhì)工程平臺(tái)、細(xì)胞培養(yǎng)技術(shù)開(kāi)發(fā)平臺(tái)、體外診斷試劑生產(chǎn)平臺(tái),通過(guò)ISO13485和ISO9001雙認(rèn)證,部分產(chǎn)品已獲美國(guó)FDA DMF備案。

