隨著細胞治療領域的快速發展,In Vivo CAR-T(體內CAR-T)療法成為行業新焦點。與傳統體外制備CAR-T不同,這項技術只需向患者體內注射攜帶CAR基因的病毒載體,便能直接在體內“就地”改造T細胞,大大簡化治療流程,為患者爭取寶貴時間。
2025年,In Vivo CAR-T領域捷報頻傳:阿斯利康以總價10億美元收購EsoBiotec,將其工程化納米抗體慢病毒平臺收入囊中;艾伯維則以高達21億美元全現金收購了專注于該領域的Capstan Therapeutics。
巨頭的巨額押注,凸顯了In Vivo CAR-T的巨大潛力。相比傳統體外CAR-T,其優勢顯著:
擺脫復雜的個體化生產流程,患者無需經歷細胞采集、體外改造、擴增回輸等漫長過程。
治療成本有望大幅下降,讓更多患者受益。
專家觀點:易慕峰生物研發中心負責人郝瑞棟博士指出:“我們的全新In Vivo技術平臺,成功打破了國外企業在關鍵元件上的專利壁壘。”
臨床層面,易慕峰基于慢病毒載體的平臺已在臨床前展現出出色性能。而EsoBiotec的ESO-T01作為第1個進入人體試驗的體內BCMA CAR-T候選藥物,在復發/難治性多發性骨髓瘤患者中實現了100%的客觀緩解率,成果令人鼓舞。
表1:In Vivo與Allo CAR-T核心特點與臨床進展對比表
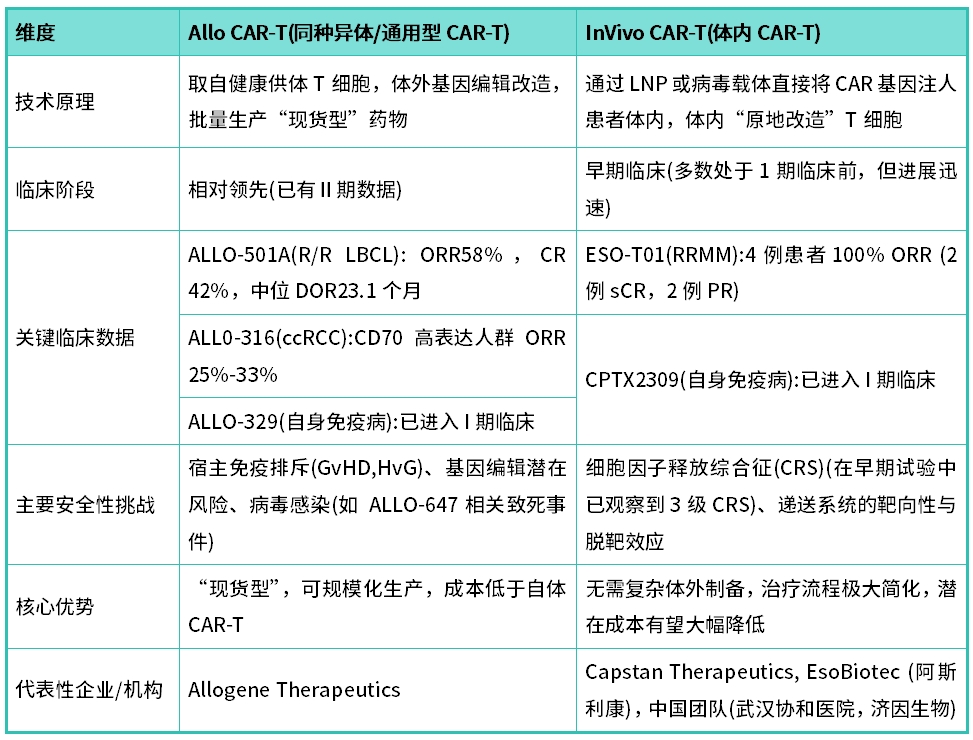
在In Vivo CAR-T開發中,遞送系統的選擇至關重要。目前,慢病毒載體因其可實現單次給藥、靶向性強、免疫原性低且臨床經驗豐富,成為主流選擇。然而,傳統的慢病毒生產工藝面臨滴度波動大、成本高、批次一致性差等挑戰,難以滿足體內治療的大規模生產需求。
破解這一瓶頸的關鍵在于穩定細胞系的開發。以深研生物的EuLV穩轉細胞系生產系統為例,通過使用可誘導的穩定生產細胞系,在化學成分確定的培養基中生產,實現了病毒產量提升近百倍、生產成本降低80%的巨大飛躍,為產業化奠定了堅實基礎。
構建包裝細胞系:將慢病毒包裝基因穩定插入宿主細胞基因組。
插入目標基因:將CAR基因穩定插入包裝細胞系,篩選出高產、穩定的單克隆。
規模化生產:在化學成分限定培養基中進行高密度懸浮培養,誘導生產慢病毒載體。
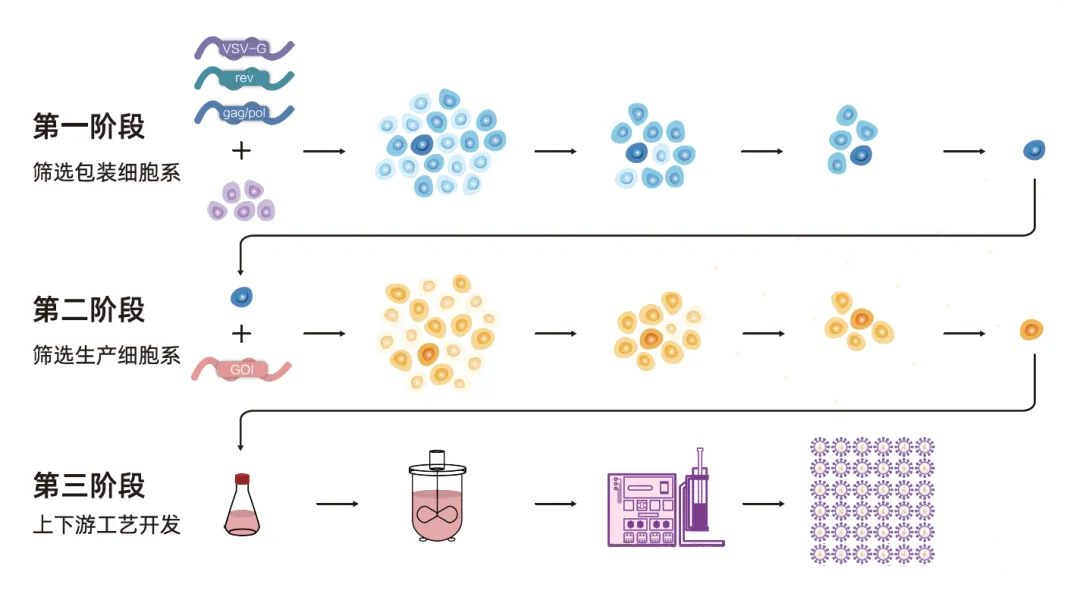
圖1:穩轉細胞系構建路線圖
在構建穩定細胞系的過程中,最關鍵的一步是篩選出高產、高穩定性的單克隆細胞。而單細胞打印技術正是在這一環節發揮著“神助攻”的關鍵作用。
這項技術已在產業界得到成功驗證。例如,國際藥企葛蘭素史克(GSK)在其發表于《Molecular Therapy Methods & Clinical Development》(2020)的研究中,詳細闡述了如何利用Cytena單細胞打印機,高效構建用于慢病毒載體生產的穩轉細胞系。
該研究通過單細胞打印篩選出的高產單克隆,在搖瓶規模下生產的未濃縮慢病毒載體功能性滴度即可穩定超過1×10? TU/mL,與高效瞬時轉染的產量相當(圖2)。
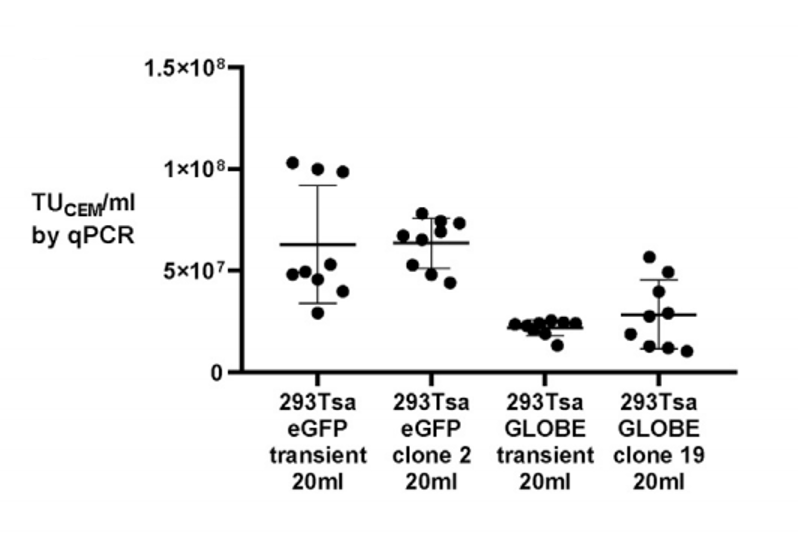
圖2:在搖瓶中通過瞬時轉染和穩定生產細胞系獲得慢病毒載體滴度圖。各點表示9個搖瓶中每個的滴度
更重要的是,這些由單克隆衍生的細胞系展現出卓越的遺傳穩定性——在連續傳代培養超過20個代次后,其載體滴度和整合的載體基因拷貝數均未發生顯著衰減(圖3)。
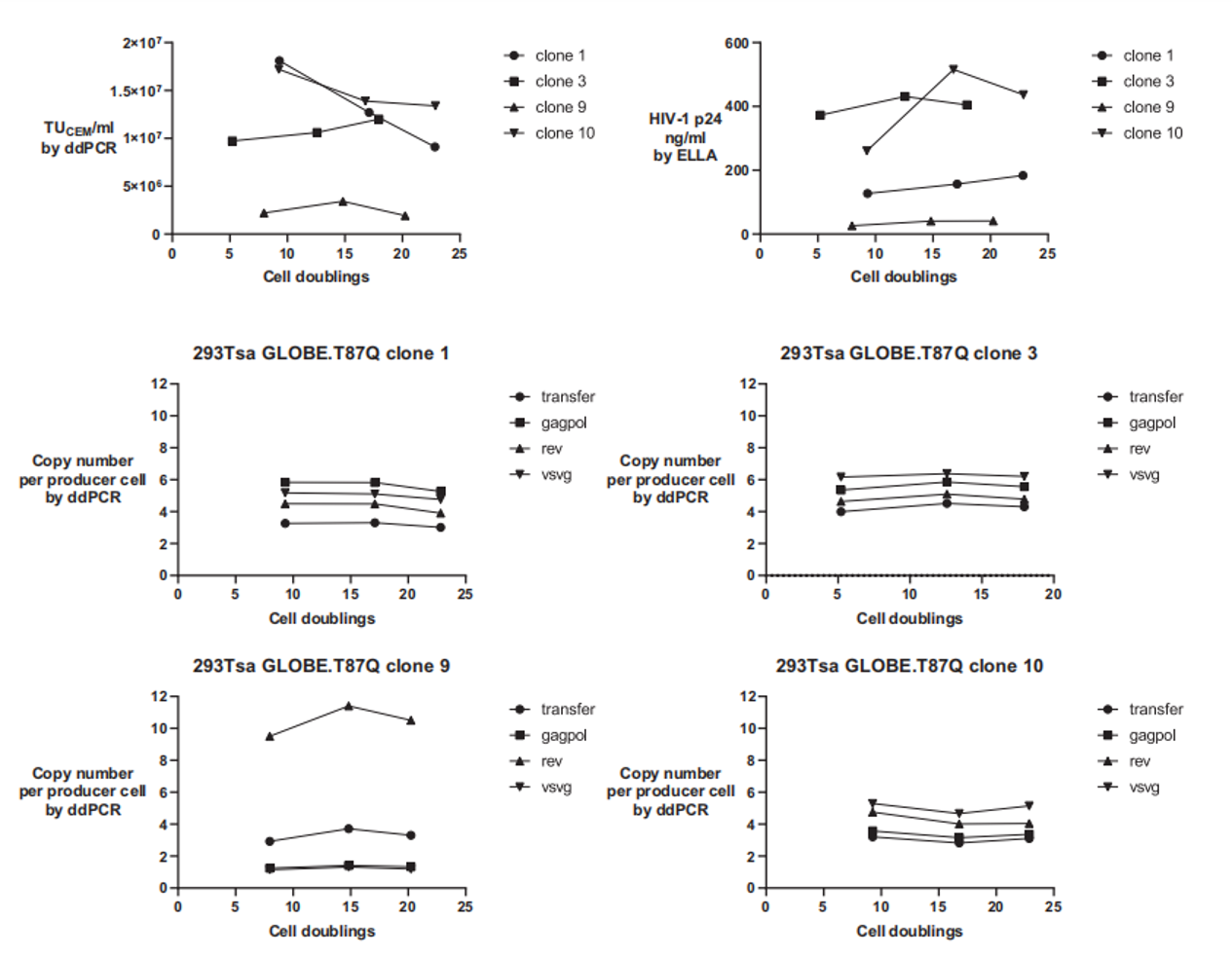
圖3:克隆在超過20個細胞倍增的過程中,功能滴度(TU/mL)和物理滴度(p24)保持穩定。
最終,該研究成功將篩選出的克隆放大至50升一次性攪拌罐生物反應器進行生產,單個批次即可收獲高達2×10¹¹總功能性TU的慢病毒載體(圖4),理論上足以滿足10名患者的治療需求。這一案例充分證明了基于單細胞打印的克隆篩選策略,是實現穩定、高產、可規模化慢病毒生產工藝的基石。
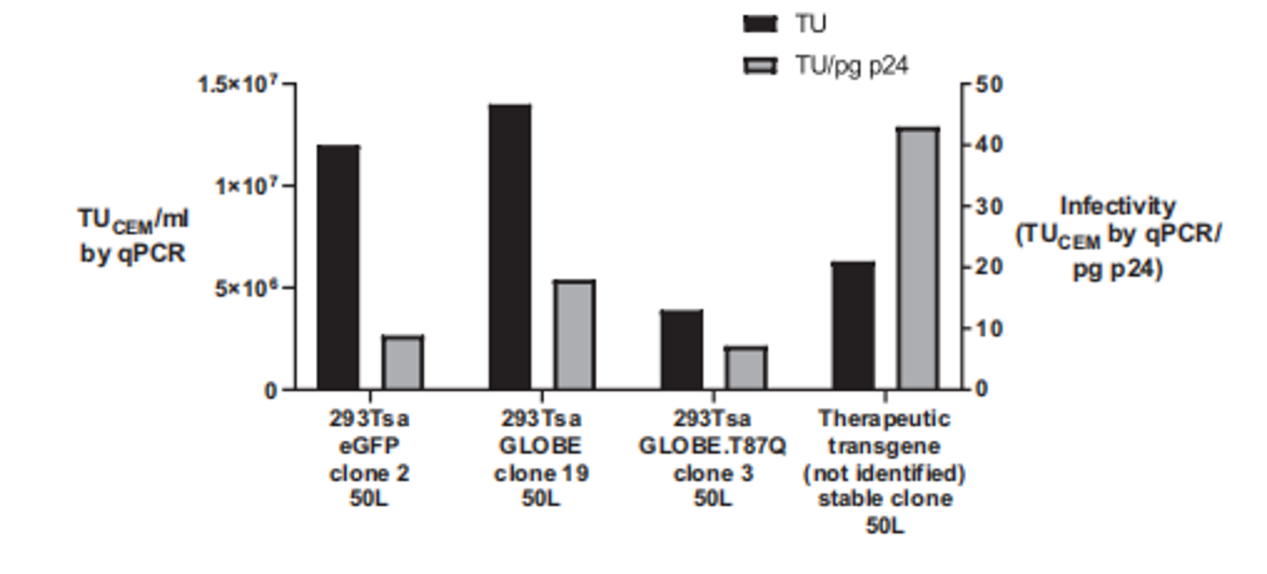
圖4:48小時后收獲50L批次的結果圖。未濃縮載體的功能滴度范圍為0.4 ~ 1.4 107 TUCEM/mL,感染性范圍為7 ~ 43 TUCEM/pg p24。
可設定細胞直徑、圓度、熒光強度等多參數,真正篩選出“強壯合格”的細胞,提高單克隆形成率。
分選一個96孔板僅需1-2分鐘,單細胞率大于95%。
設備無需復雜維護清洗,采用一次性無菌打印芯片,杜絕交叉污染。
可調整液滴位置,確保液滴滴入孔板中央,細胞沉降到孔底后能輕松拍到Day0的單細胞圖片,避免ghost well問題。
分選過程自動拍攝多張噴嘴圖片,完整記錄單克隆來源,滿足監管機構對單克隆源性的嚴苛要求。
隨著生物制藥行業對細胞系單克隆性的要求日益嚴格,單細胞打印技術的重要性將愈發凸顯。從GSK等企業的成功實踐可以看出,單細胞打印技術是產業化工藝中確保克隆源性、合規性與一致性的關鍵環節。它與慢病毒生產技術的深度融合,正推動細胞治療工藝向更高效、規范、可追溯的方向發展。未來,我們有望見證更多基于In Vivo CAR-T的治療方案獲批上市,為全球癌癥患者帶來新的希望。而單細胞打印技術,將繼續作為幕后功臣,在這一進程中扮演不可或缺的角色。
-
2025 ASGCT | 易慕峰In Vivo體內CAR-T技術平臺重磅亮相
-
In Vivo與Allo CAR-T:誰先攻克商業化堡壘?
-
體內細胞療法工藝新突破:EuLV穩轉細胞系慢病毒載體系統高效突破LVV生產瓶頸
-
Chen, Y.H., et al. (2020). Rapid Lentiviral Vector Producer Cell Line Generation Using a Single DNA Construct. Mol Ther Methods Clin Dev.
