絕對定量與相對定量概述
當對實時熒光定量 PCR (qPCR) 的結果進行計算時,可以采用絕對或相對定量。
| 絕對定量 (數字 PCR 法) |
絕對定量(標準曲線法) | 相對定量 | |
|---|---|---|---|
| 概述 | 使用數字 PCR 進行絕對定量時,無需已知的標準品。能夠以數字 PCR 重復數確定的精確度對目標分子直接進行定量。 | 使用標準曲線法進行絕對定量時,可以基于已知數量對未知數量進行定量。首先創建標準曲線;然后比較未知數量與標準曲線并推斷出數值。 | 在相對定量中,您可以分析特定樣品相對于參考樣品(比如,未處理的對照樣品)某個基因表達量的變化。 |
| 示例 |
確定異質混合物中存在的稀有等位基因拷貝數。 以基因組 DNA 為靶標,統計樣品中的細胞等價物的數量。 確定指定樣品中存在的病毒拷貝的絕對數量,而無需參考標準品。 |
將病毒拷貝數與疾病狀態建立關聯。 |
測量基因表達對藥物的應答。 在此示例中,您可以比較經化學處理樣品中的特定目標基因的基因表達水平與未處理樣品中的基因表達水平。 |
使用數字 PCR 法進行絕對定量
數字 PCR 的工作原理在于將樣品分割到許多單獨的實時熒光定量 PCR 反應中;這些反應部分包含了目標分子(陽性),而其他不包含(陰性)。PCR 分析后,一部分陰性結果用于生成樣品中目標分子精確數量的絕對結果,而無需參考標準品或內源性對照品。
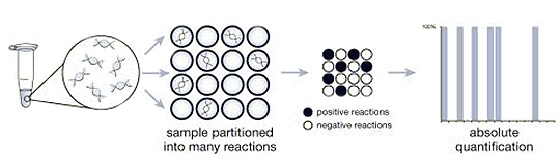
圖 1: 數字 PCR 使用陽性(白色)與陰性(黑色)PCR 反應的比例來計算目標分子的數量。
使用標準曲線法進行絕對定量
用于絕對定量的標準曲線法與用于相對定量的標準曲線法類似,只是標準品的絕對量必須首先通過其他獨立方法獲取。
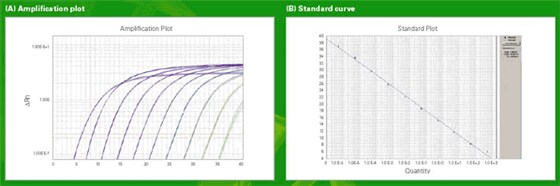
圖 2: 用于絕對定量的擴增圖和標準曲線
關鍵指南
下面的指南對于絕對定量中標準曲線的正確使用十分關鍵:
- 來自單一、純凈物種的DNA或RNA是十分重要的。例如,從大腸桿菌制備的質粒DNA通常都會存在RNA的污染,這會增加A260的讀數而增加質粒的拷貝數計算結果。
- 準確的移液是必需的因為標準品需要經過不同的數量級的順序稀釋。質粒DNA或體外轉錄的RNA必須被濃縮以便獲取準確的A260測量值。濃縮的DNA或RNA隨后必須被稀釋106–1012倍以獲得與生物學樣品中目標分子相似的濃度。
- 稀釋的標準品的穩定性也需要引起注意,特別是對于 RNA。將稀釋的標準品分裝至多份,儲存在 –80 °C 條件下,并僅在使用前才進行解凍。
一般無法使用 DNA 作為 RNA 絕對定量的標準品,因為對于逆轉錄過程的效率沒有對照。
標準品
標準品的絕對量必須首先通過其他獨立的方法獲取。質粒 DNA 和體外轉錄的 RNA 通常用于制備絕對標準品。濃度可在 A260 處測量得到,并通過使用 DNA 或 RNA 的分子量轉化成拷貝數。
相對定量
相對定量的計算方法
相對定量可根據從所有實時熒光定量 PCR 儀器獲取的數據而進行。用于相對定量的計算方法有:
- 標準曲線法
- 比較 CT 法
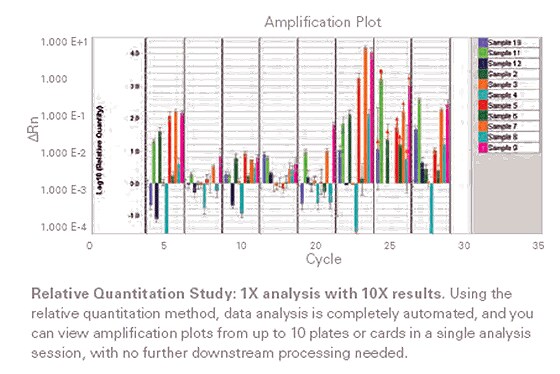
圖3: 相對定量
|
概述
|
||
| 數字 PCR 法 | 標準曲線法 | 比較 CT 法 |
|---|---|---|
| 核酸定量采用很多技術復制 PCR 應用中廣泛使用的限制樣品稀釋原理。 根據陰性反應數與總反應數的比率可確定絕對定量。此分析類型與 Ct 和 ΔCt 比較不同,相反,它允許對每個檢測靶標單獨定量,無需參考標準品。 | 因采用的是相對于基礎樣品(稱為校準品)的表達量,例如未經處理的對照品,因此用于相對定量的標準曲線容易繪制。 對于所有的實驗樣品,您可以從標準曲線確定靶標量,然后除以校準品的靶標量。 因此,校準品便成為 1× 樣品,而所有其他的量則都為以 n 倍校準品來表示。 |
此方法可在單個樣品中比較一個靶基因與另一個靶基因的 Ct 值(使用公式:2ΔΔCT)——例如,一個內部對照基因或參考基因(例如管家基因)。 |
|
產品優勢 |
||
| 無需依賴參考物或標準品。
通過增加 PCR 平行樣的總數可實現所需的精度。 高度耐受抑制劑。 能夠分析復雜混合物。 與傳統 qPCR 不同,數字 PCR 對出現的拷貝數呈線性反應,可以檢測到較小倍數變化的差異 |
在不同的反應管中進行目標分子和內源性對照的擴增時,采用標準曲線法進行分析,所需優化和驗證操作最少。 | 您無需標準曲線并且可以提高通量,因為標準曲線樣品不再需要孔。這樣就可以消除創建標準曲線樣品時出現的稀釋錯誤。
您可以在同一管內對靶標和內源性對照品進行擴增,可提高通量并減少移液錯誤。 當 RNA 位于模板中時,在同一管內執行擴增可針對 RNA 完整性和逆轉錄效率等變量進行部分歸一化。 |
實驗驗證 |
||
| 與已知拷貝數且表征良好的樣品進行并行比較,對數字 PCR 的結果進行驗證。 | 參見上文的優點。 |
您必須運行驗證實驗,以表明靶標和內源性對照品擴增的效率大致相同。 |
關鍵指南 |
||
| 在整個實驗設置過程中,請務必盡量使用低吸附性塑料器具。由于數字 PCR 強調有限稀釋檢測法,粘附至中等配置設備的任何樣品將會丟失并使結果偏離。我們建議使用 2.0 mL 低吸附管進行稀釋并使用低吸附移液器吸頭。 請務必了解需要檢測的樣品的數字區域。如果不清楚,請查閱用戶指南,確定已知物種 (gDNA) 的拷貝數,或者使用多次稀釋的樣品/檢測試劑盒組合執行初步篩查實驗,以確定能夠確保獲得有意義數據的最佳數字濃度。 樣品不應長時間儲存在低濃度條件下,也不應進行過多次凍融操作。尚未證明載體對于可重復性的重要性與使用非粘附塑料器具進行試驗設置相同。請認真制定稀釋計劃,以盡量減小稀釋方案造成的變異性。 |
RNA或DNA儲存液的準確稀釋是十分重要的,但用于表達稀釋的單位是無關的。如果對來自對照細胞系的總RNA進行了2倍的稀釋后進行標準曲線的繪制,則單位應該是稀釋值1、0.5、0.25、0.125等。如果使用相同的 RNA 或 DNA 儲存液進行不同板上的標準曲線繪制,則可在不同板之間比較確定的相對定量。 您可以使用 DNA 標準曲線進行 RNA 的相對定量。這么做需要假設靶標在所有樣品中的逆轉錄效率都是相同的,但并不需要知道效率的精確值。 在采用內源性對照進行定量均一化時,應該對目標分子和內源性參考都進行標準曲線的繪制。對于每一個實驗樣品,目標分子和內源性對照的量都是根據合適的標準曲線而確定的。因此,目標分子的量除以內源性對照的量便是均一化后的目標分子值。同樣的,其中的一個實驗樣品便是校準品,或 1× 樣品。每一個均一化的目標分子值除以校準品的均一化值后便是相對的表達水平。 |
為了有效地利用比較 CT 法,目標分子(基因)和對照(內源性對照)的擴增效率應當近似相同。 |
內源性對照 |
||
| 數字 PCR 不依賴內源性對照品進行參考測量。 | 對于內源性對照進行擴增可用于對加入至反應的樣品 RNA 或 DNA 的量進行標準化。對于基因表達定量,研究者采用過 ?-肌動蛋白、甘油醛-3-磷酸脫氫酶 (GAPDH)、核糖體 RNA (rRNA) 或其他 RNA 作為內源性對照。 | |
|
標準品 |
||
| 因為數字 PCR 通過陰性與總平行樣的比例確定分子絕對計數,所有無需標準品。 | 由于樣品量會除以校準品的量,所以標準曲線中的單位便被去除了。因此,對于標準品來說,只需知道其相對稀釋比。對于相對定量,任何含有合適目標分子的 RNA 或 DNA 儲存液都可用于制備標準品。 |
