 期刊:Kidney Int
期刊:Kidney Int
影響因子:14.8
主要技術(shù):SnRNA-seq
導(dǎo)語(yǔ)
慢性同種異體移植功能障礙(CAD)是導(dǎo)致同種異體腎移植損失的主要原因,其組織學(xué)特征為間質(zhì)纖維化和腎小管萎縮。通過(guò)snRNA-seq和轉(zhuǎn)錄組分析,確定了CAD腎同種異體移植中纖維化形成細(xì)胞的起源、功能異質(zhì)性和調(diào)控。從腎移植活檢中分離單個(gè)細(xì)胞核,并成功地分析了來(lái)自5名CAD腎移植受者的23,980個(gè)細(xì)胞核和來(lái)自3名正常同種異體移植功能患者的17,913個(gè)細(xì)胞核。揭示了兩種不同的CAD纖維化狀態(tài);低和高細(xì)胞外基質(zhì)(ECM)具有不同的腎細(xì)胞亞群,免疫細(xì)胞類型和轉(zhuǎn)錄譜。大量細(xì)胞分析證實(shí)蛋白水平ECM沉積增加。近端腎小管細(xì)胞轉(zhuǎn)變?yōu)閾p傷的混合腎小管(MT1)表型,由活化的成纖維細(xì)胞和肌成纖維細(xì)胞標(biāo)記物組成,產(chǎn)生臨時(shí)的ECM,激活炎癥細(xì)胞,并作為纖維化的主要驅(qū)動(dòng)因素。高ECM狀態(tài)的MT1細(xì)胞實(shí)現(xiàn)了復(fù)制性去分化和腎源性轉(zhuǎn)錄信號(hào)的修復(fù)。低ECM狀態(tài)下的MT1顯示細(xì)胞凋亡減少,循環(huán)小管細(xì)胞減少,以及嚴(yán)重的代謝功能障礙,限制了修復(fù)的潛力。活化的B、T和漿細(xì)胞在高ECM狀態(tài)下增加,而巨噬細(xì)胞亞型在低ECM狀態(tài)下增加。移植后數(shù)年檢測(cè)到腎實(shí)質(zhì)細(xì)胞和供體來(lái)源的巨噬細(xì)胞之間的細(xì)胞間通信,在損傷的增殖中起著關(guān)鍵作用。因此確定了新的分子靶點(diǎn),旨在改善或防止腎移植受體的同種異體移植纖維生成。
技術(shù)服務(wù)
SnRNA-seq
研究結(jié)果
1. 纖維化和正常移植物活檢中細(xì)胞類型的鑒定
使用Banff標(biāo)準(zhǔn),活檢樣本被分類為IFTA或正常/非特異性。41,893個(gè)單核的UMAP整合產(chǎn)生了18個(gè)主要的細(xì)胞簇。在纖維化和正常之間的1755個(gè)差異表達(dá)基因中,1006個(gè)DEG在纖維化中上調(diào),118個(gè)與人類核心基質(zhì)數(shù)據(jù)庫(kù)重疊。在纖維化同種異體移植活檢中,除了免疫細(xì)胞的不同類型和轉(zhuǎn)錄譜外,還鑒定了ECM基因譜的定性和定量差異。纖維化活檢分為兩種狀態(tài),低ECM和高ECM。核心染色體基因在高ECM狀態(tài)下比低ECM狀態(tài)下更豐富。FN1、COL1A1和VCAN在高ECM中存在差異表達(dá)。為了驗(yàn)證蛋白水平上的基因表達(dá),腎活檢的成像細(xì)胞計(jì)數(shù)(IMC)證實(shí)了ECM沉積的存在和水平。COL1A1和VIM的表達(dá)從正常<低ECM<高ECM增加。GO分析顯示,高ECM中炎癥反應(yīng)上調(diào),與較高比例的免疫細(xì)胞相一致。纖維化中上調(diào)基因的通路和富集分析在細(xì)胞形態(tài)發(fā)生、傷口愈合和上皮細(xì)胞分化中具有重要意義。
2. 移植腎的細(xì)胞分布
近端腎小管(PT)細(xì)胞在正常腎移植物中大量存在。與正常移植物相比,高ECM組PTs顯著降低,低ECM組PTs略有降低。與正常移植物相比,兩種纖維化狀態(tài)下成纖維細(xì)胞(FB)亞簇FB1升高。內(nèi)皮細(xì)胞(EC)亞簇EC2在高ECM狀態(tài)下更為豐富。與正相比,混合管狀(MT)亞簇MT1在纖維化中的比例過(guò)高。免疫細(xì)胞從正常到低ECM到高ECM顯著增加。低ECM和高ECM顯示了不同的氧化石墨烯富集項(xiàng)和途徑。KCNIP4在纖維化狀態(tài)特異性的小管簇中上調(diào)。KCNIP4在促炎、促纖維化狀態(tài)下上調(diào),這種狀態(tài)在急性腎損傷后持續(xù)存在。低和高ECM狀態(tài)表現(xiàn)出不同的細(xì)胞分布和轉(zhuǎn)錄譜,支持纖維化狀態(tài)的異質(zhì)性。
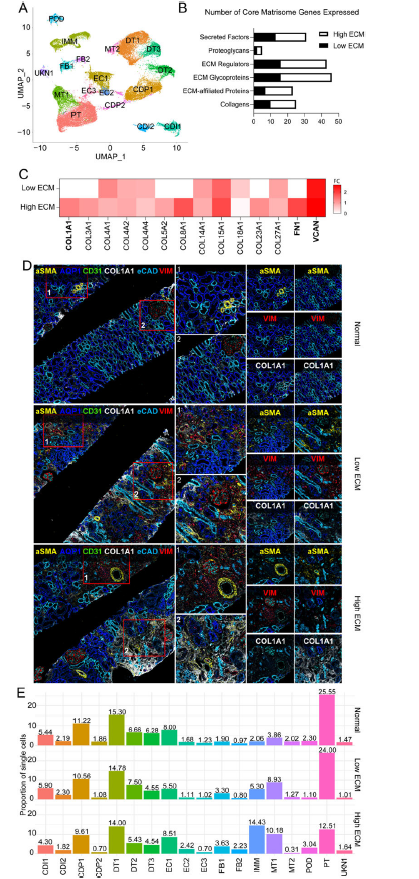
Fig 1. 正常/非特異性和纖維化人腎移植物的snRNA-seq分析
2. 小管上皮細(xì)胞損傷和移植物纖維化
兩種纖維化狀態(tài)下PT生理通路均下調(diào)。脂質(zhì)和脂肪酸代謝改變?cè)诘虴CM中更為顯著。細(xì)胞周期阻滯與腎損傷有關(guān),在腎小管細(xì)胞保護(hù)和不適應(yīng)修復(fù)中起著重要作用。所鑒定的小管細(xì)胞簇(PT, MT1, MT2)在三組之間存在與細(xì)胞循環(huán)比例相關(guān)的差異,與正常相比,低ECM時(shí)略有下降,高ECM時(shí)略有增加。與高ECM和正常ECM相比,低ECM顯示G2M細(xì)胞周期調(diào)節(jié)因子的表達(dá)減少。同種異體纖維化移植物的DEG分析顯示,MT1過(guò)表達(dá)的基因富集于肌動(dòng)蛋白絲基礎(chǔ)過(guò)程、細(xì)胞形態(tài)發(fā)生、受體酪氨酸激酶和VEGF信號(hào)傳導(dǎo)。高ECM的特征是細(xì)胞形態(tài)發(fā)生、白細(xì)胞分化和WNT信號(hào)傳導(dǎo)。
在纖維化同種異體移植物中,MT1下調(diào)氨基酸降解,高ECM中T細(xì)胞的活化和分化富集。MT1是上皮細(xì)胞向間質(zhì)轉(zhuǎn)化(EMT)的中間轉(zhuǎn)錄狀態(tài)。對(duì)于正常移植物,細(xì)胞軌跡終止于FB1,而纖維化移植物的軌跡延伸至FB2簇。這些離散的偽時(shí)間軌跡表明,基因表達(dá)的變化說(shuō)明了兩種不同的FB譜系起源于并結(jié)束于PT,導(dǎo)致從PT到FB2集群的功能轉(zhuǎn)變。轉(zhuǎn)錄組學(xué)分析顯示,MT1共表達(dá)PT和損傷25個(gè)marker。高ECM狀態(tài)下的MT1表達(dá)更高水平的損傷marker。移植物損傷和正常PT標(biāo)記物的正常表達(dá)可能是持續(xù)的亞臨床免疫反應(yīng)和慢性暴露于鈣調(diào)磷酸酶抑制劑的結(jié)果。在高ECM的MT1中,增殖標(biāo)記物(MKI67)和凋亡標(biāo)記物(CASP3)的共同上調(diào),受損PT細(xì)胞亞群經(jīng)歷了損傷誘導(dǎo)的復(fù)制。與低ECM和正常相比,高ECM MT1的SLC34A1表達(dá)減少,表明損傷的PT細(xì)胞去分化。在早期腎臟發(fā)育期間正常表達(dá)的腎源性特征與高ECM相關(guān),而在低ECM中沒(méi)有觀察到。MT2細(xì)胞不像MT1細(xì)胞那么豐富,主要存在于正常的同種異體移植物中。

Fig 2. 混合管狀細(xì)胞群細(xì)胞周期及基因表達(dá)分析
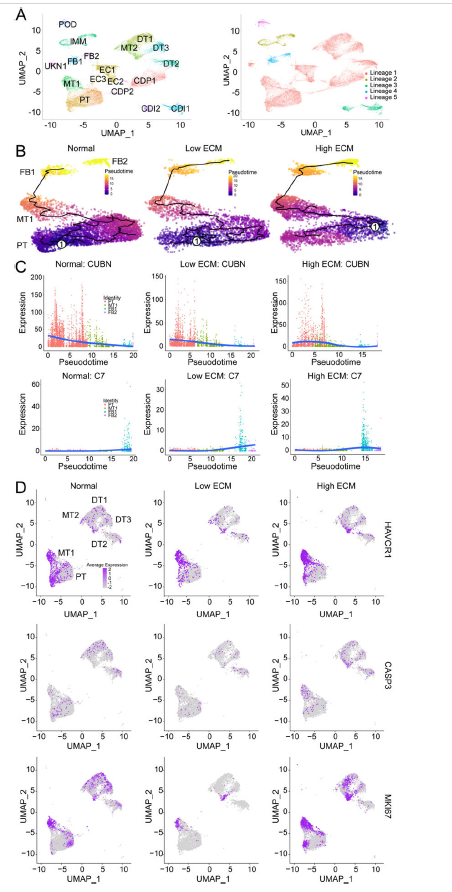
Fig 3. 近端小管細(xì)胞和混合小管細(xì)胞簇基因表達(dá)動(dòng)態(tài)變化的擬時(shí)間和軌跡分析
3. 腎移植物中的成纖維細(xì)胞亞型
鑒定出兩種不同的成纖維細(xì)胞簇(FB1, FB2)。FB1在纖維化腎臟中更豐富,富含肌成纖維細(xì)胞標(biāo)記物。低ECM中FB1的GO分析顯示細(xì)胞連接、局灶黏附和VEGF信號(hào)通路上調(diào),而高ECM中ECM組織、平滑肌收縮和傷口愈合上調(diào)。FB2在高ECM中占主導(dǎo)地位,由PDGFR-β表達(dá)定義,并在周細(xì)胞標(biāo)記物中富集。FB2相關(guān)信號(hào)通路包括RhoA、NOTCH和整合素激酶信號(hào)。在高ECM中,F(xiàn)B2通路與肌動(dòng)蛋白絲為基礎(chǔ)的過(guò)程、局灶黏附以及細(xì)胞運(yùn)動(dòng)和黏附的正向調(diào)節(jié)有關(guān)。FB1-2在高ECM中比低ECM中轉(zhuǎn)錄活性更強(qiáng)。譜系圖譜分析確定了FB在正常和纖維化狀態(tài)下的重編程軌跡。正常移植物中的FBs沿偽時(shí)間軌跡是均勻的,而纖維化移植物中的FBs則是不均勻的。這一數(shù)據(jù)支持FB在纖維化移植物中的功能表型轉(zhuǎn)變。
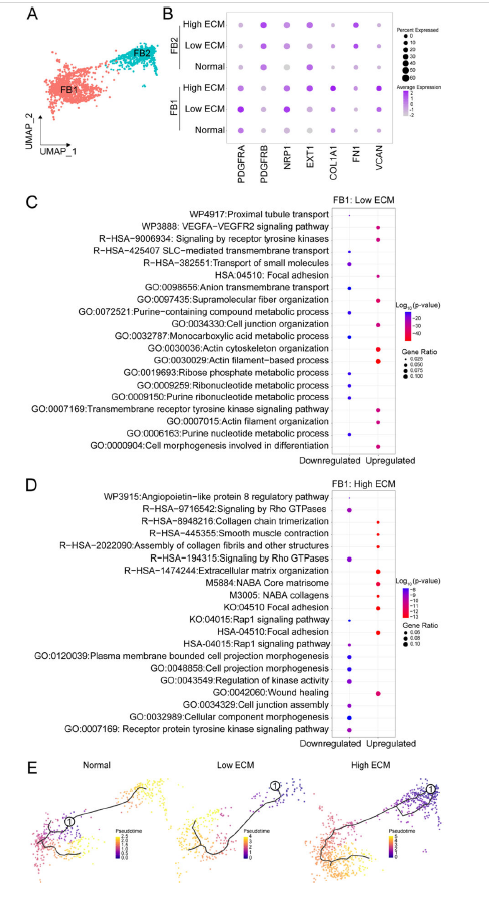
Fig 4. 成纖維細(xì)胞簇的基因表達(dá)及軌跡分析
4. 衰竭腎臟的免疫系統(tǒng)
總共分析了2,655個(gè)免疫細(xì)胞,并在研究組中確定了12個(gè)免疫亞群。正常同種異體移植物的免疫細(xì)胞最少。低ECM的骨髓細(xì)胞比例最高,包括各種巨噬細(xì)胞(MΦ1, MΦ2),經(jīng)典和漿細(xì)胞樣樹(shù)突狀細(xì)胞(cDC, pDC)和肥大細(xì)胞。高ECM的B細(xì)胞、血漿細(xì)胞、T細(xì)胞和Treg細(xì)胞比例最高。免疫細(xì)胞(T (CD4+, CD8+), B (CD20+)和MΦ (CD68+))的相對(duì)比例和空間分布通過(guò)福爾馬林固定石蠟包埋活檢的IMC染色進(jìn)行評(píng)估。
高ECM的T細(xì)胞簇富集了與B和T細(xì)胞活化、NF-kB信號(hào)、TCR信號(hào)和Th17細(xì)胞分化相關(guān)的DEGs,這與MT1簇富集的活性增加相匹配。B細(xì)胞通路相關(guān)基因包括B細(xì)胞活化、白細(xì)胞趨化、內(nèi)吞作用以及NF-kB和FC受體介導(dǎo)的刺激信號(hào)通路的調(diào)控。高ECM的漿細(xì)胞具有活躍的轉(zhuǎn)錄譜。
鑒定出三個(gè)巨噬細(xì)胞簇(MΦ1-3),并以常見(jiàn)的巨噬細(xì)胞標(biāo)志物(CSF1R, MANBA, PLXDC2, RTN1, GRK3)為特征。MΦ1s通過(guò)抗原加工和遞呈上調(diào)、HLA II類基因上調(diào)和Th1/Th2/Th17細(xì)胞分化進(jìn)行分類。MΦ2s(以STAB1, F13A1, CD163, NRP1為特征)顯示MHC ii類介導(dǎo)的抗原呈遞和巨噬細(xì)胞M2相關(guān)的吞噬。MΦ1-2在高ECM腎移植物中也過(guò)表達(dá)CD74。
低ECM擁有最大的MΦ1和MΦ2群。在兩種纖維化狀態(tài)下,MΦ2的表達(dá)譜與細(xì)胞粘附和內(nèi)吞作用調(diào)節(jié)有關(guān),而IFN-α和-γ反應(yīng)是高ECM所特有的。
使用三組性別不匹配病例的XY染色體相關(guān)基因表達(dá)特征來(lái)評(píng)估供體與受體免疫細(xì)胞對(duì)同種異體移植物的貢獻(xiàn)。免疫細(xì)胞主要來(lái)自受體,小部分來(lái)自供體。沒(méi)有證據(jù)表明受體存在非免疫細(xì)胞。對(duì)于一些樣本,根據(jù)性別特異性基因的表達(dá)將免疫細(xì)胞群分為供體/受體特異性免疫細(xì)。移植后60個(gè)月,供體免疫細(xì)胞在腎移植中被鑒定出來(lái)。對(duì)樣本KUT040中特定細(xì)胞類型的供體和受體標(biāo)記的免疫細(xì)胞之間的DEGs進(jìn)行了評(píng)估。這項(xiàng)原理驗(yàn)證分析顯示,基于供體/受體來(lái)源的免疫細(xì)胞的差異貢獻(xiàn),支持常駐巨噬細(xì)胞在腎移植中介導(dǎo)和加劇免疫介導(dǎo)的炎癥中的重要作用。
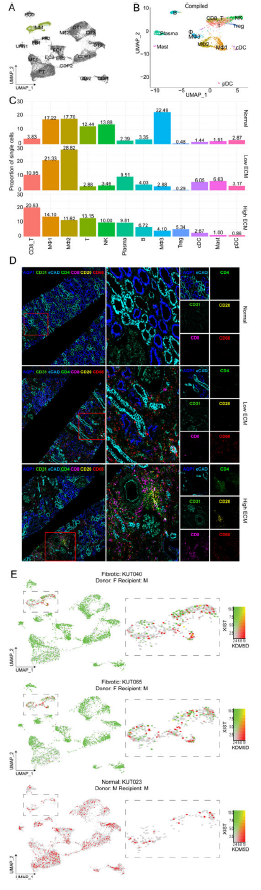
Fig 5. 人腎移植中的免疫細(xì)胞
5. 纖維化過(guò)程中的旁分泌信號(hào)
配體受體(LR)分析集中在細(xì)胞比例有顯著差異的簇上,并在腎纖維化中具有重要意義。它們的成纖維細(xì)胞受體具有共同的功能作用,包括成纖維細(xì)胞激活和ECM擴(kuò)展。
PDGFC是一種強(qiáng)效的促纖維化絲裂原,在纖維化移植物中分泌,支持成纖維細(xì)胞向肌成纖維細(xì)胞的轉(zhuǎn)分化。NOTCH信號(hào)通路的上調(diào)也是共有的。TLRs通過(guò)DLL1觸發(fā)巨噬細(xì)胞中的NOTCH信號(hào),DLL1是高ECM分泌的主要NOTCH配體。對(duì)于低ECM, FB1-MΦ3 LRs也參與PI3K-Akt-mTOR信號(hào)傳導(dǎo)。對(duì)于低ECM, MT1-MΦ3和MT1-MΦ1 LRs參與趨化性和管狀/組織形態(tài)發(fā)生。細(xì)胞極性調(diào)節(jié)劑CELSR1-PSAP和成纖維細(xì)胞增殖和激活調(diào)節(jié)劑FGFR2-MAPK1等相互作用進(jìn)一步支持低ECM中的EMT。在高ECM中,MT1-MΦ1(和FB1-MΦ1)相互作用反映了細(xì)胞因子介導(dǎo)的和NIK/NF-kB信號(hào)通路,與增加的免疫細(xì)胞豐度和激活一致。H&E和IHC染色進(jìn)一步證實(shí)了LR與浸潤(rùn)細(xì)胞和受損腎臟結(jié)構(gòu)的相互作用。低ECM腎實(shí)質(zhì)顯示纖維化斑塊,而高ECM顯示更緊密的纖維化區(qū)域。間質(zhì)間存在和相對(duì)豐富的肌成纖維細(xì)胞在纖維化發(fā)病過(guò)程中起著關(guān)鍵作用。
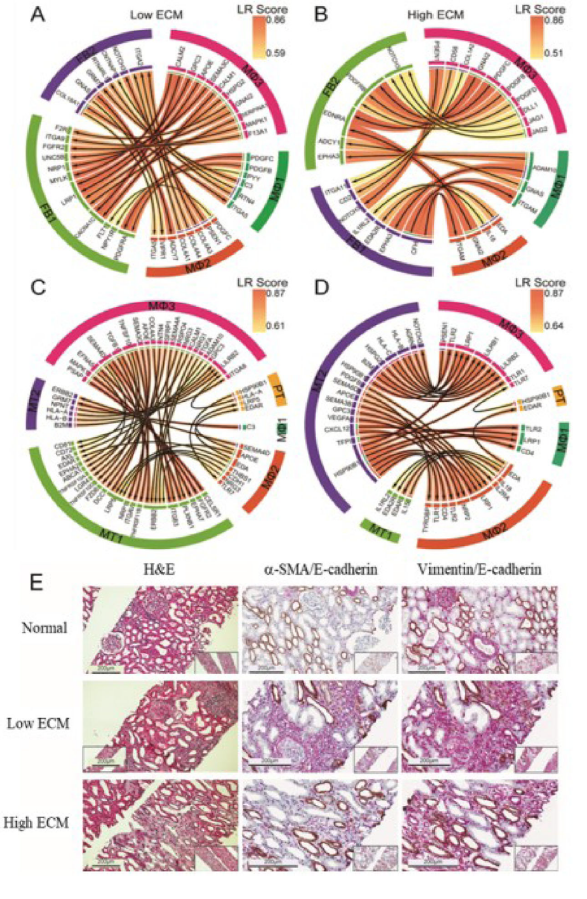
Fig 6. 細(xì)胞-細(xì)胞相互作用和染色組織空間驗(yàn)證
參考文獻(xiàn):
McDaniels JM, Shetty AC, Kuscu C, Kuscu C, Bardhi E, Rousselle T, Drachenberg C, Talwar M, Eason JD, Muthukumar T, Maluf DG, Mas VR. Single nuclei transcriptomics delineates complex immune and kidney cell interactions contributing to kidney allograft fibrosis. Kidney Int. 2023 Jun;103(6):1077-1092. doi: 10.1016/j.kint.2023.02.018. Epub 2023 Feb 28. PMID: 36863444; PMCID: PMC10200746.
