2021年11月澳大利亞Victor Chang心臟研究所Richard P. Harvey團(tuán)隊(duì)與Vaibhao Janbandhu等人合作在Cell Stem Cell上發(fā)表題目為“Hif-1a suppresses ROS-induced proliferation of cardiac fibroblasts following myocardial infarction”的心血管文章,該研究發(fā)現(xiàn)HIF-1a能夠抑制心肌梗死后ROS增加介導(dǎo)的心臟成纖維細(xì)胞增殖所致心肌纖維化擴(kuò)張的現(xiàn)象。該發(fā)現(xiàn)為心血管疾病的治療提供了新的藥物靶點(diǎn)和研究方向。
缺氧誘導(dǎo)因子1(HIF-1)通路一直在心血管生物學(xué)領(lǐng)域中發(fā)揮重要作用。妊娠期生理性缺氧激活局部HIF-1通路,對(duì)心臟的腔室和室間隔形態(tài)發(fā)育至關(guān)重要。成人心臟經(jīng)歷周期性的缺氧,包括生理上在高海拔和運(yùn)動(dòng)期間以及病理上在缺血期間、心肌細(xì)胞肥大、炎癥和纖維化期間的缺氧,這些情況可能與ROS水平升高和氧化損傷有關(guān)。
機(jī)體通過HIF-1通路適應(yīng)缺氧微環(huán)境,HIF-1α屬于bHLH-PAS (basic-helix-loop-helix-Per-Arnt-Sim) 家族的轉(zhuǎn)錄因子。缺氧條件下HIF-1a亞基穩(wěn)定并易位到細(xì)胞核,異二聚后激活下游基因通路,減少氧消耗和活性氧(ROS)生成,并恢復(fù)氧遞送。
HIF-1在心臟中的作用的研究主要集中在心肌細(xì)胞上,且其在ECM重構(gòu)和缺血預(yù)適應(yīng)以及動(dòng)脈粥樣硬化進(jìn)程中的作用已被證實(shí)。但HIF-1在心臟成纖維細(xì)胞中的功能尚未被闡明。心臟成纖維細(xì)胞是一種異質(zhì)性的基質(zhì)細(xì)胞群,通過控制細(xì)胞外基質(zhì)的沉積和周轉(zhuǎn)來促進(jìn)心臟的生物力學(xué)完整性,并介導(dǎo)心臟修復(fù)和再生中的適應(yīng)性纖維化。心臟成纖維細(xì)胞幾乎與所有形式的心血管病理表型相關(guān)如:ECM分泌與收縮、纖維化與疤痕形成、心力衰竭等。
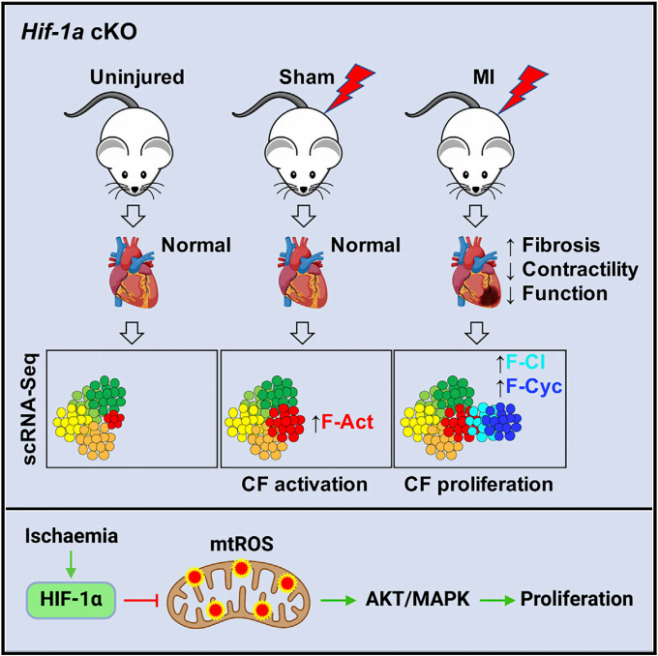
?
亮點(diǎn)要素
研究思路
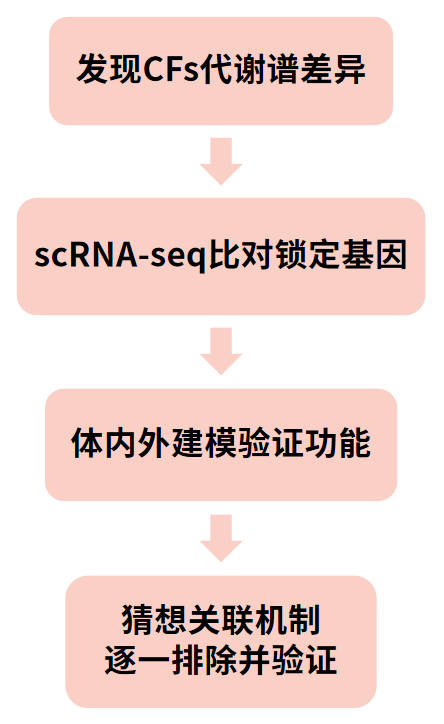
-
通過對(duì)未損傷的小鼠S+P+陽性的CFs采用流式等分析,發(fā)現(xiàn)該種類細(xì)胞在缺氧狀態(tài)下的代謝更傾向于糖酵解途徑而非常規(guī)的線粒體氧化磷酸化途徑,由此發(fā)現(xiàn)CFs不同于CMs的代謝譜差異。(現(xiàn)象挖掘)
-
HIF-1a在缺氧狀態(tài)下CFs中高表達(dá),其靶基因能在正常的氧化磷酸化中促進(jìn)糖酵解途徑,通過scRNA-seq結(jié)果與HIF-1靶基因數(shù)據(jù)庫的比對(duì)確定HIF-1的靶基因是同樣在缺氧CFs中高表達(dá)的MEIS1。(鎖定目標(biāo))
-
體外利用與CFs類似的cCFU-Fs成纖維細(xì)胞系,驗(yàn)證線粒體質(zhì)量低的細(xì)胞具有和CFs類似的增殖能力;體內(nèi)構(gòu)建CFs特異性Hif-1a敲除小鼠驗(yàn)證其在CFs穩(wěn)態(tài)和心臟疾病中的作用。(體內(nèi)外驗(yàn)證)
-
通過整理并利用qRT-PCR逐一驗(yàn)證與HIF-1相關(guān)的機(jī)制如糖酵解、血管生成、氧化還原穩(wěn)態(tài)等,最終將HIF-1作用機(jī)制確定為調(diào)節(jié)線粒體氧化應(yīng)激。(關(guān)聯(lián)機(jī)制驗(yàn)證)
-
通過ROS探針等驗(yàn)證在缺氧CFs中HIF-1α調(diào)節(jié)氧化應(yīng)激降低線粒體ROS,進(jìn)而抑制由ROS介導(dǎo)PI3K/AKT/mTOR及MAPK、ERK1/2等通路激活導(dǎo)致的CFs增殖。(機(jī)制串聯(lián))
?
研究?jī)?nèi)容
首先分離正常小鼠心臟中 SCA1+/PDGFRa+/CD31-的CFs,在低氧狀態(tài)下通過Pim染色流式分析發(fā)現(xiàn)S+P+細(xì)胞缺氧程度高于其他非心肌細(xì)胞群,其氧消耗及ATP水平遠(yuǎn)低于其他非心肌細(xì)胞群。但其葡萄糖消耗速率及細(xì)胞內(nèi)乳酸水平卻更高,提示S+P+細(xì)胞的代謝更傾向于糖酵解途徑而非常規(guī)的線粒體氧化磷酸化途徑,與之相對(duì)應(yīng)的S+P+細(xì)胞的線粒體質(zhì)量同樣偏低。HIF-1a及其靶基因在S+P+細(xì)胞中高表達(dá),已知HIF-1a的靶基因能在氧化磷酸化中促進(jìn)糖酵解,隨后通過已發(fā)表的scRNA-seq結(jié)果與HIF-1靶基因數(shù)據(jù)庫的比對(duì)確定HIF-1a的靶基因MEIS1。又進(jìn)一步對(duì)線粒體質(zhì)量差異的細(xì)胞進(jìn)行增殖能力的對(duì)比,發(fā)現(xiàn)低線粒體質(zhì)量的細(xì)胞增殖能力更強(qiáng),這也與缺氧狀態(tài)下CFs的增殖現(xiàn)象相符合。
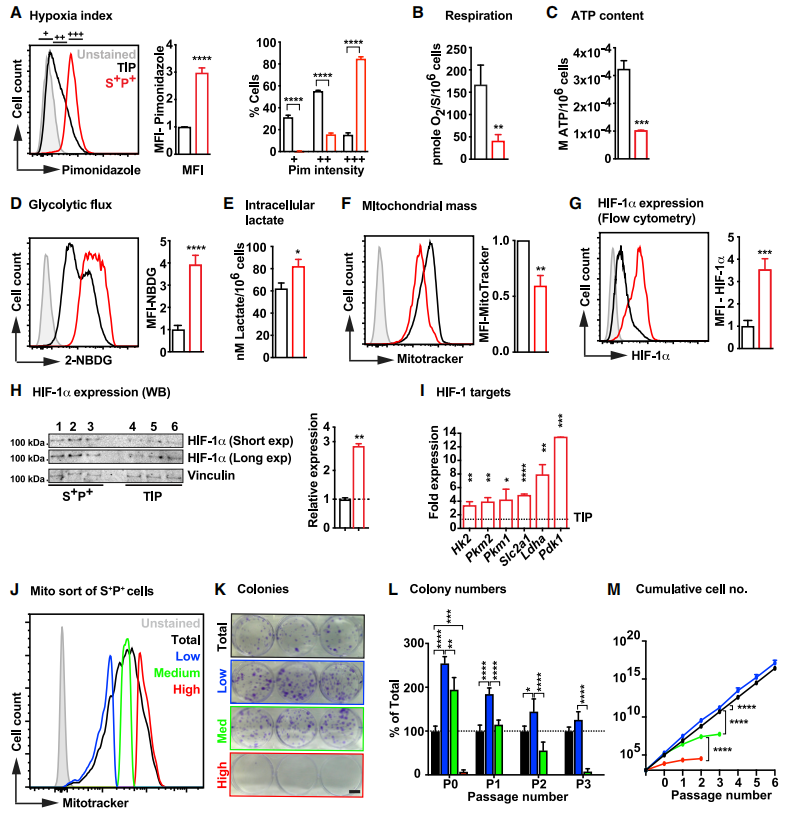
圖1.成年小鼠心臟中S+P+細(xì)胞的代謝譜
為了探索HIF-1a在心臟成纖維細(xì)胞穩(wěn)態(tài)和疾病中的作用,研究者構(gòu)建了CF特異性HIF-1a他莫昔芬誘導(dǎo)的條件性敲除小鼠并對(duì)其心臟中CF進(jìn)行測(cè)序。發(fā)現(xiàn)cKO小鼠下調(diào)的差異基因與發(fā)表的HIF-1靶基因存在交集,且GOterm分析顯示,HIF-1相關(guān)靶點(diǎn)參與了增殖等細(xì)胞功能的調(diào)控,其他少數(shù)上調(diào)的基因與炎癥、蛋白水解和應(yīng)激等途徑有關(guān)。接下來為了研究cKO小鼠在心臟損傷后CFs的增殖情況,研究者構(gòu)建了心肌梗死模型并利用EdU追蹤增殖細(xì)胞。MI手術(shù)3天時(shí)在梗死區(qū)觀察到EdU+細(xì)胞,7天時(shí)延伸至梗死邊界區(qū),而譜系陰性小鼠無變化。提示CFs中Hif-1a的缺失可導(dǎo)致心肌梗死后成纖維細(xì)胞增殖增加。
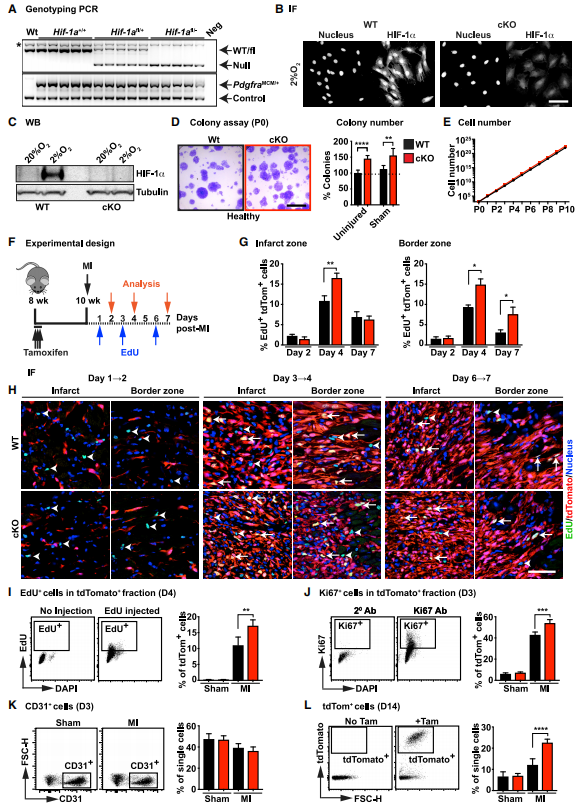
圖2.心肌梗死后hif-1a缺失的CFs的增殖能力有缺陷
對(duì)MI及假手術(shù)第3天的cKO小鼠心臟成纖維細(xì)胞進(jìn)行scRNA-seq測(cè)序,發(fā)現(xiàn)假手術(shù)組cKO小鼠CFs同樣存在激活現(xiàn)象,驗(yàn)證了CFs存在全身因素的敏感性。測(cè)序的另一發(fā)現(xiàn)是成纖維細(xì)胞前體減少,代表損傷的中間體和激活體增加,證明更多的CF進(jìn)入細(xì)胞周期。同時(shí)由于中間體和激活體增多,相關(guān)的蛋白合成基因上調(diào),編碼細(xì)胞信號(hào)傳導(dǎo)負(fù)調(diào)控因子的基因下調(diào),導(dǎo)致CF開始增殖。對(duì)心肌梗死后第14天的cKO小鼠左心室進(jìn)行qPCR,發(fā)現(xiàn)細(xì)胞外基質(zhì)、重構(gòu)蛋白酶和纖維化介質(zhì)相關(guān)基因顯著上調(diào),證明心臟纖維化反應(yīng)增加。
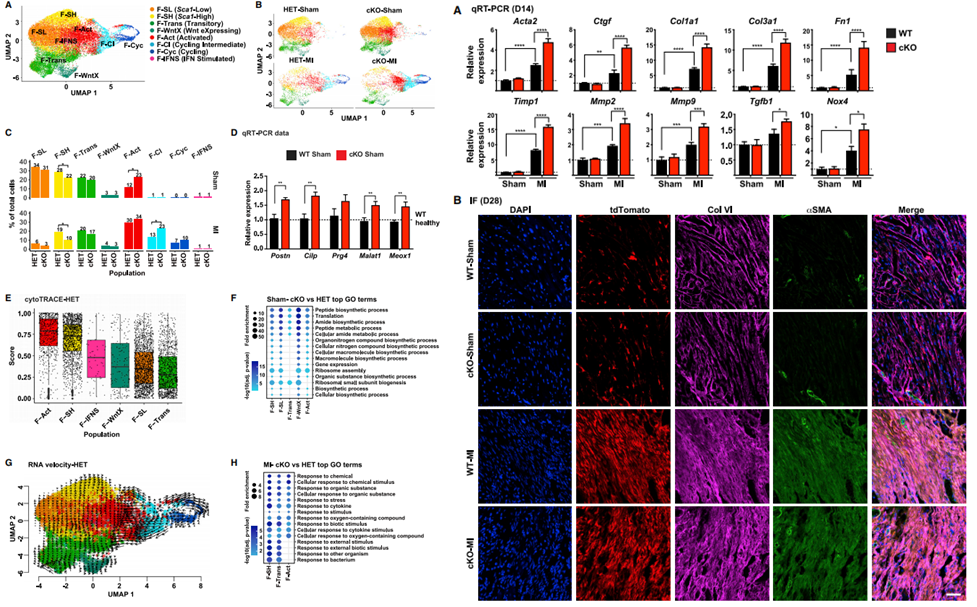
圖3.HIF-1a缺失的CFs在心梗后重入細(xì)胞周期并加重心梗后纖維化
為了更直觀的展現(xiàn)cKO小鼠CFs的動(dòng)態(tài),研究者運(yùn)用前沿3D技術(shù)構(gòu)建了3D工程化心肌微組織。體外培養(yǎng)顯示cKO小鼠CFs顯著擴(kuò)張并伴隨著膠原沉積,但并不影響心肌組織的面積。隨后又探究了3D心臟體系CFs動(dòng)作電位的傳導(dǎo)情況,與WT相比cKO心臟束的傳導(dǎo)速率較慢、動(dòng)作電位持續(xù)時(shí)間更長(zhǎng),并表現(xiàn)出收縮力的損害。cKO小鼠CFs在這種缺乏血管、免疫和其他心肌細(xì)胞類型的簡(jiǎn)單3D體系中的影響與體內(nèi)研究基本一致。
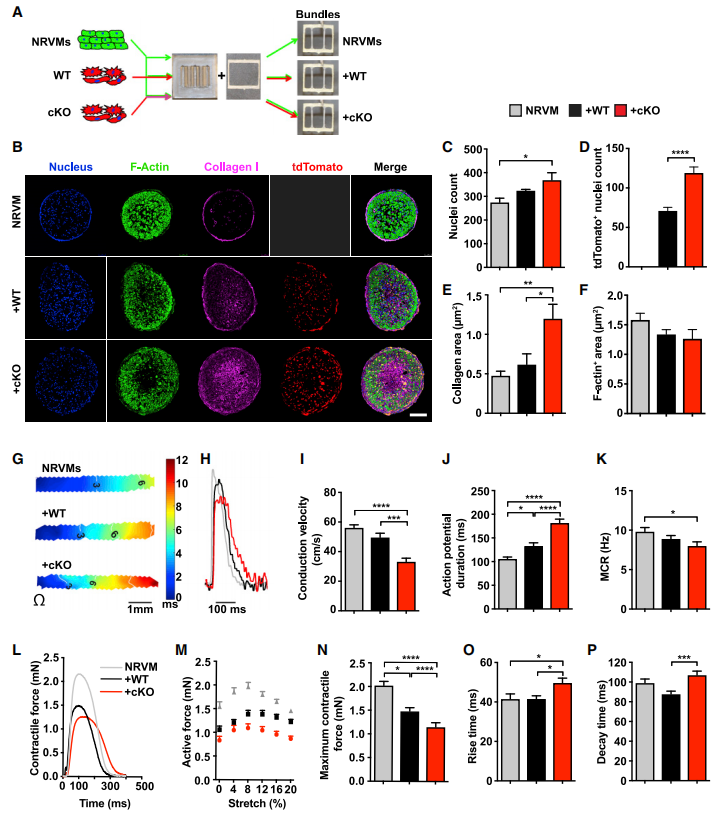
圖4.Hif-1a缺失的CFs在體外顯著惡化了3D心肌束的電位傳導(dǎo)和機(jī)械力
機(jī)制研究,在應(yīng)對(duì)缺氧時(shí),Hif-1a通過確保有效利用現(xiàn)有的氧氣和能量底物,同時(shí)最小化線粒體氧化應(yīng)激來調(diào)節(jié)代謝。研究者對(duì)MI術(shù)后第1天純化的cKO小鼠CF進(jìn)行qRT-PCR檢測(cè),發(fā)現(xiàn)與糖酵解、血管生成和氧化還原穩(wěn)態(tài)有關(guān)的HIF-1靶基因的表達(dá)顯著降低。鑒于心肌梗死后cKO心臟中控制氧化還原穩(wěn)態(tài)的HIF-1a靶點(diǎn)下調(diào)有助于減少線粒體ROS,并且已知正常生理產(chǎn)生的ROS可以作為干細(xì)胞/祖細(xì)胞增殖和分化的信號(hào)。研究者大膽假設(shè)ROS的增加是cKO小鼠CFs增殖和纖維化增加的原因并進(jìn)行驗(yàn)證,線粒體特異性ROS探針證明梗死后的ROS增加定位于線粒體中并伴隨CF的顯著增殖。接下來利用線粒體氧化劑MitoPQ(ROS促進(jìn)劑)在體處理后CF顯著增殖,而線粒體抗氧化劑MitoT(ROS抑制劑)治療后CF增殖及總數(shù)均減少。已有研究表明,ROS與PI3K/AKT/mTOR、MAPK、ERK1/2通路的激活有關(guān)。MitoT處理后,心梗cKO小鼠的CF中pERK1/2和pAKT降低到與心梗WT小鼠相同的水平。這些數(shù)據(jù)證明了ROS與AKT和ERK1/2信號(hào)通路的關(guān)系及其在CF增殖中作用機(jī)制。
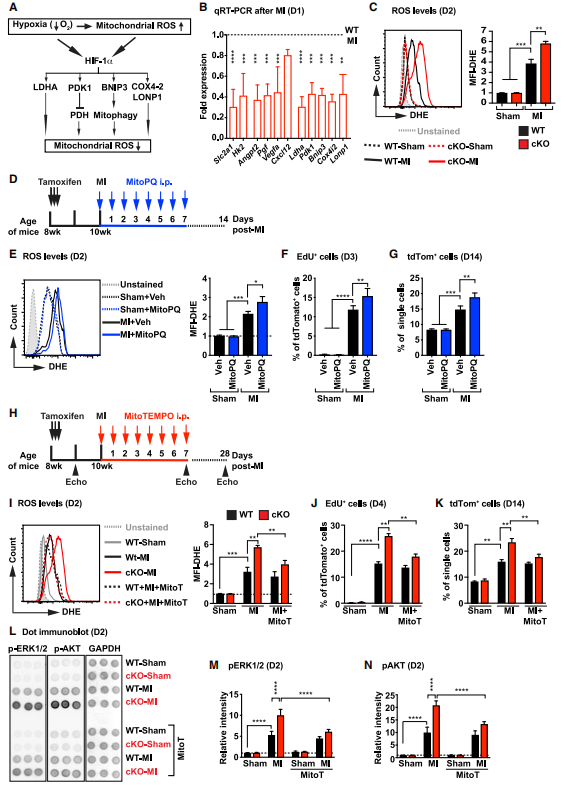
圖5.Hif-1a介導(dǎo)的氧化還原調(diào)節(jié)控制心肌梗死后CFs的增殖
通過研究線粒體抗氧化劑MitoT為未來心臟病治療提供解決思路。MI術(shù)后28天的小鼠心臟瘢痕面積增加、活心肌體積減少。MitoT的治療挽救了心梗cKO小鼠的心臟心室重構(gòu)、CF增殖及ECM擴(kuò)張。心臟超聲顯示MI術(shù)后第7天和第28天,cKO小鼠心臟功能明顯惡化,包括面積變化減少、左室射血分?jǐn)?shù)和心輸出量減少,左室收縮末期和舒張量增加。cKO-MI小鼠的心重體重比也顯著升高,體現(xiàn)出CF增殖及ECM的擴(kuò)張。MitoT的治療能夠逆轉(zhuǎn)不良的心功能參數(shù)和HW/BW比值并使其恢復(fù)到WT小鼠MI術(shù)后心臟相似的水平,該發(fā)現(xiàn)或可為心臟病治療研究提供新的思路。
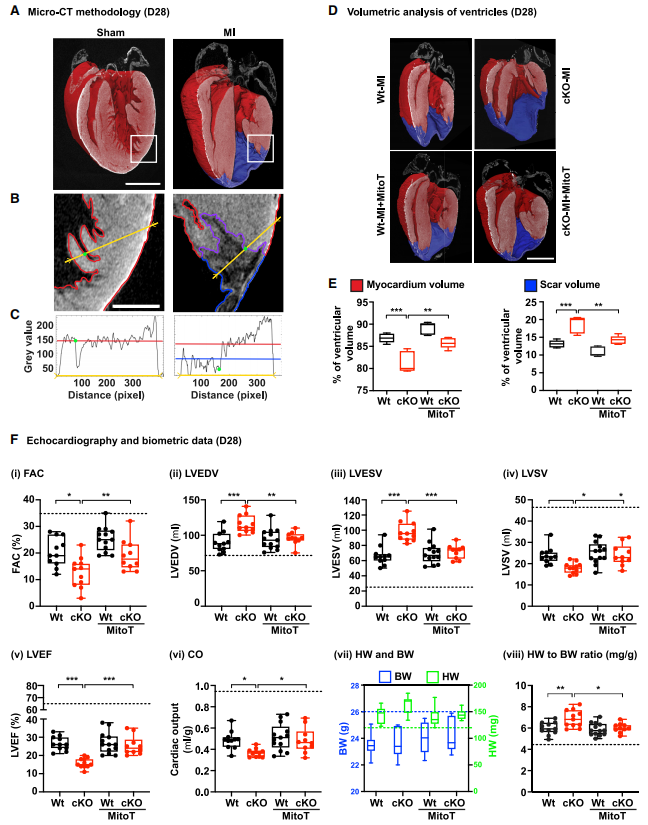
圖6.MitoT治療挽救了心肌梗死后cKO小鼠的心臟結(jié)構(gòu)和功能缺陷
和元生物具有多年豐富的動(dòng)物實(shí)驗(yàn)和心血管動(dòng)物模型構(gòu)建的實(shí)操經(jīng)驗(yàn),并兼具出色的基因操作與病毒構(gòu)建等技術(shù)。同時(shí)依托公司的檢測(cè)平臺(tái)、病理平臺(tái)、細(xì)胞平臺(tái)等專業(yè)實(shí)驗(yàn)平臺(tái),可為您提供從心血管動(dòng)物模型到基因干預(yù)、病理檢測(cè)、細(xì)胞功能學(xué)研究等一站式心血管研究服務(wù)體系,您可體驗(yàn)文中涉及到的心血管前沿研究手段與支持。歡迎掃描下方二維碼了解更多實(shí)驗(yàn)服務(wù)詳情。
