

影響因子:6.2
伯豪技術(shù)服務(wù):單細(xì)胞轉(zhuǎn)錄組測序
研究背景
胃癌(GC)是全球癌癥相關(guān)死亡的第三大原因,預(yù)后普遍較差。胃癌干細(xì)胞(GCSCs)因其自我更新能力、異質(zhì)性分化潛能以及對化療和靶向治療的強(qiáng)耐藥性,被認(rèn)為是腫瘤發(fā)生、進(jìn)展、復(fù)發(fā)和治療抵抗的關(guān)鍵驅(qū)動因素。盡管靶向Wnt/β-catenin信號通路(GCSCs干性和耐藥性的核心調(diào)控通路)是極具前景的策略,但目前缺乏臨床可用的有效抑制劑。
主要技術(shù)
單細(xì)胞轉(zhuǎn)錄組測序
(技術(shù)服務(wù)由伯豪生物提供)
實驗材料
人類GC細(xì)胞系(MGC-803、SGC-7901、BGC-823、MKN-45);4至6周齡雄性裸鼠。
結(jié)論
通過高通量篩選臨床獲批藥物庫,發(fā)現(xiàn)抗生素藥物氯福克酚(Clofoctol, CFT) 能高效抑制β-catenin表達(dá),顯著削弱GCSCs干性,并通過結(jié)合RanBP2蛋白誘導(dǎo)TNF介導(dǎo)的程序性壞死,為胃癌治療提供了新的候選策略。
實驗結(jié)果
1. 高通量篩選鑒定CFT為強(qiáng)效β-catenin抑制劑
篩選策略: 使用實時定量PCR(RT-qPCR)檢測206種FDA批準(zhǔn)的無明確靶點藥物對胃癌細(xì)胞系MGC-803中β-catenin mRNA水平的影響。
關(guān)鍵發(fā)現(xiàn):
10種藥物(4.85%)能將β-catenin mRNA抑制至對照組50%以下(圖1A, B)。
CFT表現(xiàn)出最強(qiáng)的抑制效果,顯著降低多個GC細(xì)胞系(MGC-803, SGC-7901, BGC-823, MKN-45)的β-catenin mRNA和蛋白水平(圖1C,附圖S1A)。
細(xì)胞效應(yīng)初探:
常規(guī)培養(yǎng)下,CFT(≤10 μM)在前48小時對細(xì)胞活力和凋亡無顯著影響(附圖S1B-D)。
營養(yǎng)應(yīng)激增強(qiáng)CFT效應(yīng): 在低血清(1% FBS)模擬的微環(huán)境壓力下,CFT處理7天后顯著抑制GC細(xì)胞增殖,誘導(dǎo)S期阻滯并促進(jìn)細(xì)胞凋亡(圖1D-F,附圖S2A-C)。
協(xié)同化療: CFT與5-氟尿嘧啶(5-Fu)聯(lián)用表現(xiàn)出顯著的協(xié)同抗腫瘤效應(yīng)(附圖S2E, F)。
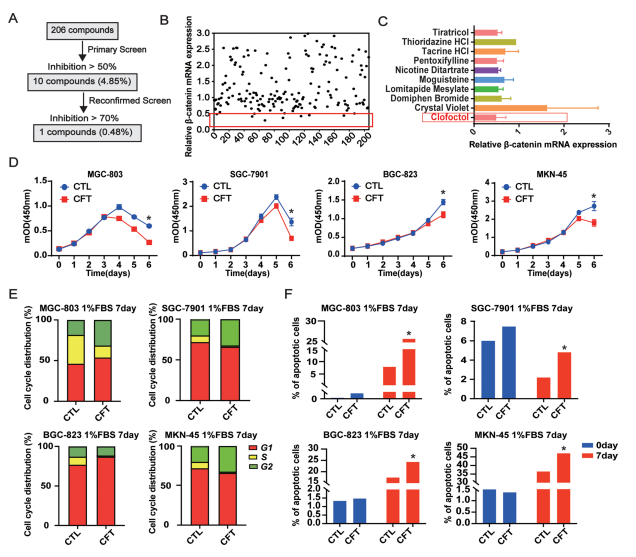
圖1. CFT在低血清培養(yǎng)基中抑制β-catenin和細(xì)胞生長
2. CFT有效抑制GCSCs干性及致瘤性
干性標(biāo)志物下調(diào): CFT處理顯著降低干性相關(guān)基因(Nanog, Oct4, Survivin, Sox2, Lgr5)的mRNA表達(dá)(圖2A)。
自我更新能力受損:
體外球體形成: CFT處理顯著降低GC細(xì)胞形成腫瘤球體的頻率和能力(圖2B,附圖S3A, B)。
集落形成: CFT處理顯著減少GC細(xì)胞的貼壁依賴性集落形成單位(CFU)(圖2D)。
GCSCs標(biāo)志物減少: 流式細(xì)胞術(shù)(FCM)分析顯示,CFT處理顯著降低CD44?/CD133?雙陽性細(xì)胞群以及高醛脫氫酶活性(ALDH?)細(xì)胞群的比例(圖2E, F,附圖S4A, B)。
體內(nèi)致瘤性減弱:
有限稀釋實驗: 將不同數(shù)量(10?, 10?, 10?)的GC細(xì)胞皮下接種裸鼠,CFT處理組形成的腫瘤更少、更小,表明CFT降低了具有腫瘤起始能力的細(xì)胞比例(圖2G)。
次級移植瘤實驗: 將CFT處理組來源的原代腫瘤細(xì)胞再次接種小鼠,形成的次級腫瘤數(shù)量和體積顯著小于對照組,證明CFT處理可長期抑制腫瘤再生能力(圖2H)。
遷移侵襲抑制: CFT通過下調(diào)上皮間質(zhì)轉(zhuǎn)化(EMT)相關(guān)蛋白抑制GC細(xì)胞的遷移和侵襲能力(附圖S5A-D)。
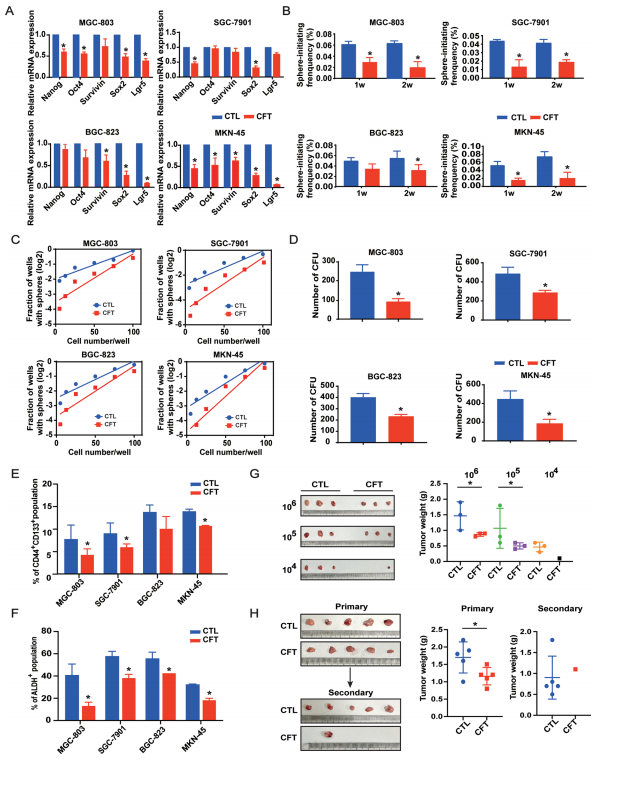
圖2. CFT在體內(nèi)和體外抑制GC細(xì)胞干性
3. CFT選擇性殺傷GCSCs并誘導(dǎo)凋亡/壞死
模型建立: 從4株GC細(xì)胞系和2例GC患者原代細(xì)胞中分離培養(yǎng)GCSCs。
選擇性殺傷:
CFT(10 μM)能顯著抑制6種不同來源GCSCs的活力,而同等劑量對普通GC細(xì)胞或正常細(xì)胞(HUVEC, 293T, GES-1, H9)影響甚微(圖3A-C,附圖S6A, B)。
GCSCs通常對化療藥5-Fu和順鉑(Cis)耐藥,但CFT對其表現(xiàn)出強(qiáng)效殺傷作用(圖3A)。
誘導(dǎo)細(xì)胞死亡:
FCM(Annexin V/PI)和Calcein-AM/PI活死染色證實CFT顯著增加GCSCs的凋亡/死亡細(xì)胞比例(圖3D, E,附圖S6C, D)。
人凋亡抗體芯片: CFT處理改變多個凋亡相關(guān)蛋白表達(dá),包括Caspase-3、HSP27、CytoC、FasL、Survivin和XIAP(圖3F,附圖S6E)。
活性氧積累: CFT誘導(dǎo)GCSCs內(nèi)活性氧(ROS)顯著累積(附圖S6F)。
體內(nèi)抗GCSCs活性:
裸鼠移植瘤模型: 將SGC-7901來源的GCSCs接種裸鼠,腫瘤體積達(dá)50 mm³后腹腔注射CFT(30 mg/kg/天,連續(xù)11天)。CFT顯著抑制腫瘤生長,且不顯著影響小鼠體重(圖4A-D)。
機(jī)制驗證:
免疫組化/免疫熒光:CFT處理組腫瘤中Cleaved Caspase-3表達(dá)升高(凋亡增加),CD44?/CD133?細(xì)胞比例降低(干性減弱)(圖4E-G)。
單細(xì)胞RNA測序(scRNA-seq): 分析CFT處理組腫瘤細(xì)胞組成,發(fā)現(xiàn)具有高干性基因(NEAT1, COL7A1, MALAT1, IMMP2L)特征的細(xì)胞簇(Cluster 5)比例顯著減少,且該簇細(xì)胞處于分化早期(圖4H-K,附圖S7C-E)。
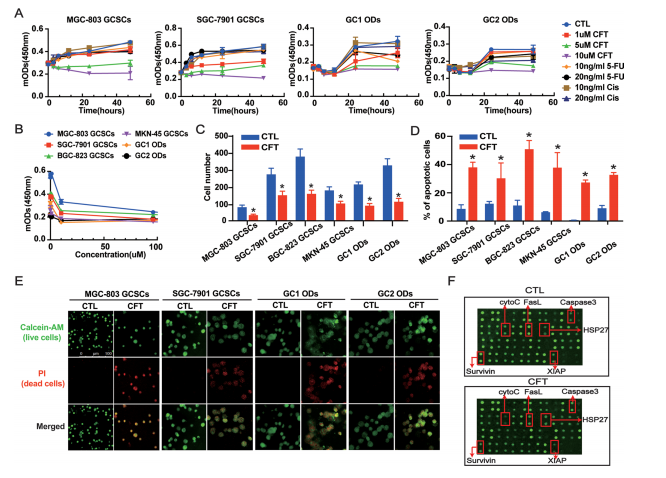
圖3. CFT抑制GCSC活率并誘導(dǎo)凋亡
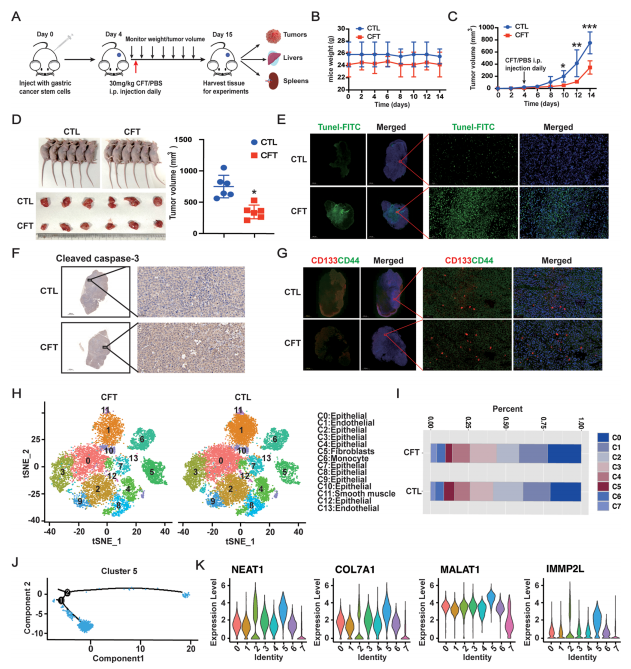
圖4. CFT在體內(nèi)誘導(dǎo)GCSC凋亡
4. 分子機(jī)制:靶向RanBP2調(diào)控SerpinE1/β-catenin軸與TNF壞死通路
RNA-seq揭示關(guān)鍵通路:
CFT顯著下調(diào)SerpinE1(與GC不良預(yù)后正相關(guān))表達(dá)(圖5B,附圖S9A-D)。
CFT顯著上調(diào)TNF表達(dá),并富集到“細(xì)胞因子-受體相互作用”、“凋亡”和“壞死性凋亡”相關(guān)通路(圖5D-F,附圖S8C-F)。
蛋白互作(PPI)網(wǎng)絡(luò)分析確認(rèn)TNF是調(diào)控凋亡/壞死網(wǎng)絡(luò)的核心節(jié)點(圖5G)。
qRT-PCR驗證CFT上調(diào)多個壞死性凋亡相關(guān)基因(TNF, IL6, IL18等)(圖5H, I)。
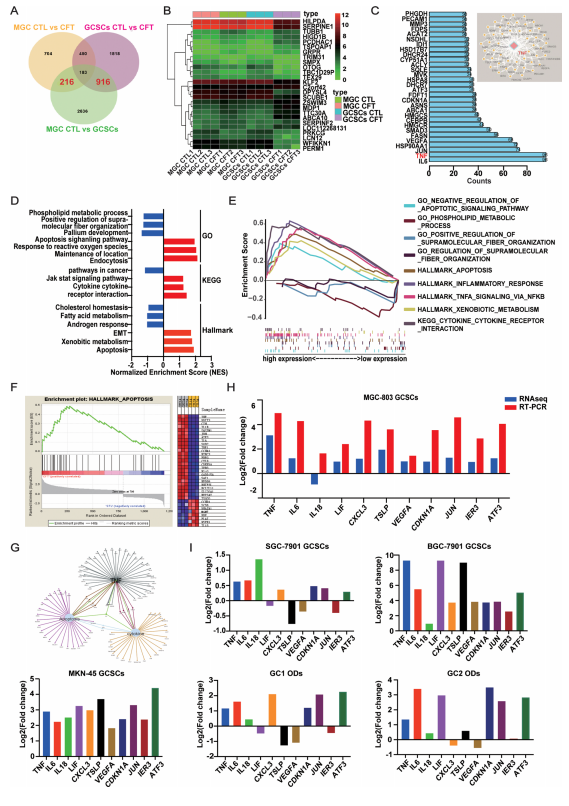
圖5. SerpinE和TNF是CFT的靶點
SerpinE1是CFT抑制干性的關(guān)鍵下游因子:
回補(bǔ)實驗:在GC細(xì)胞中過表達(dá)SerpinE1,可部分逆轉(zhuǎn)CFT對β-catenin的下調(diào)作用(圖6A,附圖S9E-G)。
過表達(dá)SerpinE1顯著上調(diào)干性基因(Nanog, Oct4等)表達(dá),并增強(qiáng)集落形成、球體形成和致瘤能力,而CFT處理能拮抗這些效應(yīng)(圖6B-G,附圖S9H, I)。
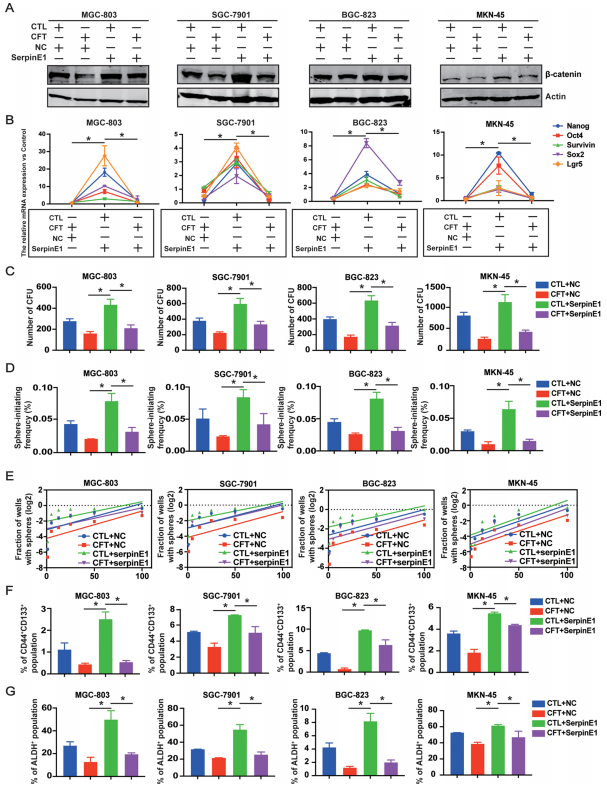
圖6. SerpinE1與CFT介導(dǎo)的GC細(xì)胞干性抑制有關(guān)
CFT激活TNF介導(dǎo)的程序性壞死(Necroptosis):
CFT顯著上調(diào)GCSCs中TNF mRNA和磷酸化RIPK1、RIPK3、MLKL蛋白水平(圖7B, C)。
使用特異性RIPK1抑制劑Necrostatin-1 (Nec-1) 可劑量依賴性地阻斷CFT誘導(dǎo)的TNF上調(diào)和細(xì)胞凋亡/壞死(圖7D, E),證明CFT通過TNF-RIPK1/RIPK3/MLKL通路誘導(dǎo)GCSCs壞死性凋亡。
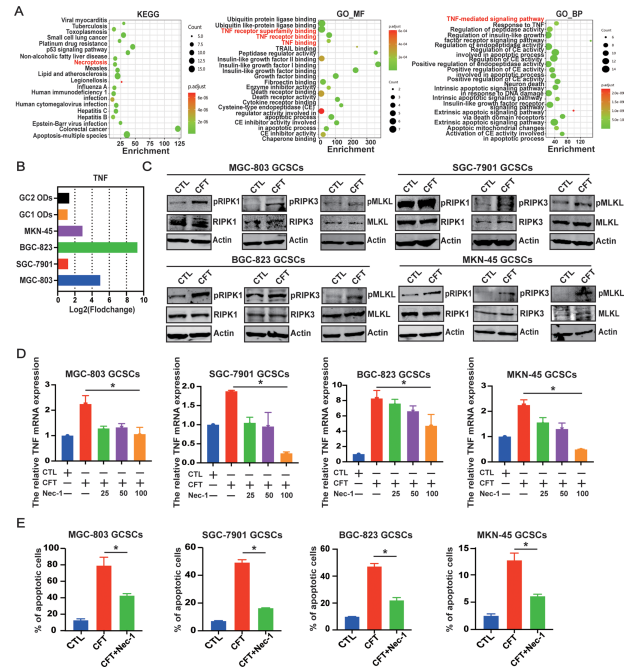
圖7. CFT誘導(dǎo)TNF介導(dǎo)的GCSC壞死性凋亡
CFT直接靶向結(jié)合RanBP2:
網(wǎng)絡(luò)藥理學(xué)與分子對接: 預(yù)測出25個CFT潛在靶點,PPI網(wǎng)絡(luò)分析及GC表達(dá)數(shù)據(jù)提示RanBP2(SUMO E3連接酶)是關(guān)鍵候選靶點(圖8A,附圖S10A-H)。
分子對接: CFT通過氫鍵與RanBP2的PHE-110殘基穩(wěn)定結(jié)合(圖8B)。
DARTS驗證: CFT結(jié)合可保護(hù)RanBP2蛋白免受蛋白酶降解(圖8C)。
分子動力學(xué)(MD)模擬: 模擬CFT-RanBP2復(fù)合物100 ns動態(tài),顯示復(fù)合物RMSD、Rg、RMSF值穩(wěn)定,結(jié)合自由能分解確認(rèn)PHE-110等殘基對結(jié)合貢獻(xiàn)大,證實兩者結(jié)合穩(wěn)定(圖8D-H,附圖S10I)。
功能驗證: 敲低RanBP2:
特異性降低SUMO1(而非SUMO2/3/4)蛋白水平(附圖S10K)。
逆轉(zhuǎn)CFT對SerpinE1、β-catenin和SUMO1的下調(diào)作用(圖8I),證明RanBP2是CFT發(fā)揮功能的上游靶點。
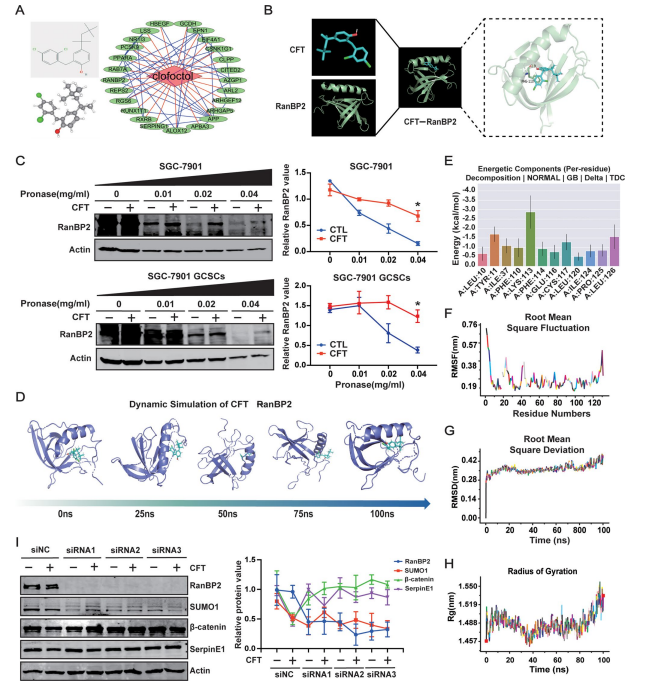
圖8. CFT與RanBP2結(jié)合調(diào)控靶蛋白
5. 機(jī)器學(xué)習(xí)構(gòu)建CFT療效預(yù)測模型
模型構(gòu)建:基于RNA-seq數(shù)據(jù),應(yīng)用Lasso回歸(LR)、支持向量機(jī)(SVM)和隨機(jī)森林(RF)三種機(jī)器學(xué)習(xí)算法篩選特征基因。
核心基因:整合分析得到77個候選基因,進(jìn)一步結(jié)合TCGA胃癌轉(zhuǎn)錄組數(shù)據(jù),最終確定13個基因構(gòu)成預(yù)測模型(附圖S11A-C)。
預(yù)后價值:
根據(jù)風(fēng)險評分將TCGA胃癌患者分為高風(fēng)險組和低風(fēng)險組。高風(fēng)險組患者總生存期(OS)顯著短于低風(fēng)險組(P=0.00336)(附圖S11D)。
多因素Cox回歸確認(rèn)年齡、腫瘤分期和風(fēng)險評分是獨立預(yù)后因素(附圖S11F)。
風(fēng)險評分對3年內(nèi)預(yù)后具有良好預(yù)測價值(ROC曲線下面積AUC=0.627)(附圖S11E, I)。
列線圖整合風(fēng)險評分與臨床特征,可直觀預(yù)測患者生存(附圖S11G, H)。
總結(jié)
靶點結(jié)合:CFT直接結(jié)合SUMO E3連接酶RanBP2。
干性抑制:通過RanBP2下調(diào)SerpinE1表達(dá),進(jìn)而抑制β-catenin信號通路,削弱GCSCs干性、自我更新和致瘤能力。
誘導(dǎo)死亡:通過RanBP2激活TNF介導(dǎo)的RIPK1/RIPK3/MLKL依賴性程序性壞死途徑,選擇性殺傷耐藥性GCSCs。
預(yù)測工具:基于13個基因的機(jī)器學(xué)習(xí)模型可預(yù)測胃癌患者預(yù)后及潛在CFT治療反應(yīng)。
臨床轉(zhuǎn)化價值:
老藥新用:CFT作為已獲批的抗菌藥物,其安全性已知,重新定位用于胃癌治療可加速臨床轉(zhuǎn)化。
靶向GCSCs:CFT能有效清除對傳統(tǒng)化療耐藥的GCSCs,為克服胃癌復(fù)發(fā)和轉(zhuǎn)移提供了新策略。
聯(lián)合治療:CFT與化療藥物(如5-Fu)聯(lián)用展現(xiàn)協(xié)同效應(yīng),具有臨床聯(lián)合用藥潛力。
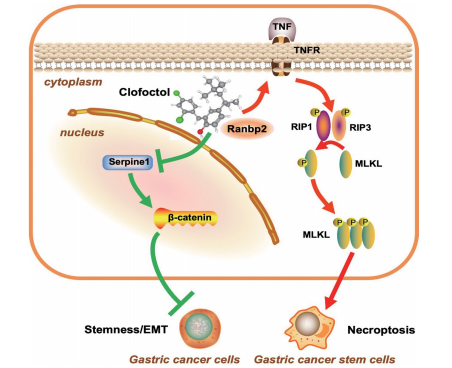
圖9. 機(jī)制圖:CFT與RanBP2結(jié)合,誘導(dǎo)壞死性凋亡,抑制干性
參考文獻(xiàn):
Liu Y, Ma Y, Zhou B, et al. Clofoctol impairs the stemness of gastric cancer and induces TNF-mediated necroptosis by directly binding to RanBP2. Cell Mol Life Sci. 2025;82:194.
